|
||||||||||||||||||||||||||||||||||||
| [
Sadržaj
] [ Indeks autora ]
|
||||||||||||||||||||||||||||||||||||
| UDK 616.127-002-07 COBISS.SR-ID 191805193 |
strana 38. |
|||||||||||||||||||||||||||||||||||
|
Pregledni članak / Paper review NOVINE U ESC VODIČU ZA MIOKARDITIS
I PERIKARDITIS IZ 2025. GODINE: INTEGRATIVNI PRISTUP INFLAMATORNIM
MIOPERIKARDNIM SINDROMIMA I IMPLIKACIJE ZA KLINIČKU PRAKSU |
||||||||||||||||||||||||||||||||||||
|
Sažetak: UVOD: Miokarditis predstavlja inflamatorno oboljenje
miokarda koje može imati veoma heterogenu kliničku prezentaciju, od
asimptomatskih oblika do fulminantne srčane insuficijencije i iznenadne
srčane smrti. Cilj ovog preglednog rada je prikaz savremenih
dijagnostičkih i terapijskih pristupa prema najnovijim ESC preporukama,
uz integraciju kliničkih iskustava i naglašavanje potrebe za daljim
istraživanjima. PREGLED LITERATURE: Evropsko kardiološko
udruženje (ESC) objavilo je 2025. godine prve integrisane smernice koje
objedinjeno obrađuju dijagnostiku i terapiju miokarditisa i
perikarditisa, uvodeći novi koncept inflamatornog mioperikardnog
sindroma (IMPS). Ovaj krovni termin prepoznaje čestu kliničku
isprepletanost ova dva entiteta i njihov zajednički patofiziološki
mehanizam. U radu se analiziraju ključne novine u klasifikaciji,
dijagnostici, genetskoj obradi i terapijskom pristupu, uz poseban osvrt
na revidirane kriterijume kardiomagnetne rezonance-CMR (Lake Louise
kriterijumi), proširene indikacije za endomiokardnu biopsiju (EMB) i
inovacije u terapiji perikarditisa, uključujući interleukin 1
inhibitore. Promenjena je paradigma za dijagnozu miokarditisa Diskusija
obuhvata poređenje ESC preporuka sa američkim ACC/AHA smernicama, kao i
doprinose domaće literature, posebno radove iz oblasti dijastolnog stres
testa i inflamatornih kardiomiopatija. Pandemija COVID-19 dodatno je
skrenula pažnju na miokarditis kao potencijalnu komplikaciju virusnih
infekcija. ZAKLJUČAK: Savremeni pristup miokarditisu menja
paradigmu uvodeći koncept Inflamatornog mioperikardnog sindroma i
podrazumeva integrisanu dijagnostiku i terapiju u skladu sa najnovijim
ESC smernicama, uz prepoznavanje inflamatornog mioperikardnog sindroma
kao klinički značajnog entiteta. Unapređenja u primeni kardiomagnetne
rezonance, šire indikacije za endomiokardnu biopsiju i uvođenje ciljane
terapije, uključujući interleukin-1 inhibitore, omogućavaju precizniju
dijagnozu i individualizovan terapijski pristup. Uprkos napretku,
heterogenost kliničke slike i dalje predstavlja izazov u svakodnevnoj
praksi. Neophodna su dodatna istraživanja radi boljeg razumevanja
patofiziologije i optimizacije lečenja ovih bolesnika. Ključne reči: miokarditis, perikarditis, inflamatorni mioperikardni sindrom, ESC smernice, magnetna rezonanca srca, COVID-19, endomiokardna biopsija. |
||||||||||||||||||||||||||||||||||||
| UVOD ESC smernice
iz 2025. godine predstavljaju prekretnicu u pristupu inflamatornim
oboljenjima srca, ujedinjujući miokarditis i perikarditis u jedan
vodič [1]. Ova odluka proističe iz sve jasnijeg razumevanja da su
ova dva entiteta funkcionalno, anatomski i patofiziološki usko
povezana, te da njihov odvojen pristup često vodi fragmentisanju
dijagnostike i terapije. Novi koncept inflamatornog mioperikardnog
sindroma (IMPS) predstavlja krovni terminobuhvata klinički kontinuum
od i obuhvata klinički kontinuum od izolovanog miokarditisa, preko
kombinovanog mioperikarditisa i perimiokarditisa, do izolovanog
perikarditisa, uključujući i složene mešovite oblike do hronične
inflamatorne kardiomiopatije i konstriktivnog perikarditisa
[2-5,6-8, ]. Takav integrativni pristup ima za cilj unapređenje
saradnje između stručnjaka i usmeravanje budućih istraživanja.
Uveden je i termin inflamatorna kardiomiopatija, koji se odnosi na
hronični miokarditis povezan sa srčanom disfunkcijom i
remodelovanjem komora sa hipokinetičkim fenotipom, sa ili bez
dilatacije. Uloga kardio-magnetne rezonance (CMR) sada je centralna
u dijagnostici [9- 11 ]. U domaćoj literaturi, između ostali radovi
autora ovog preglednog rada sa saradnicima su doprineli razumevanju
aspekta dijastolne disfunkcije i ehokardiografskih parametara kod
inflamatornih kardiomiopatija [12–14], dok se endomiokardna biopsija
preporučuje u visoko rizičnim slučajevima [1,15-21]. Smernice navode incidenciju perikarditisa od 3 do 32 slučaja na 100.000 stanovnika godišnje, dok je incidencija miokarditisa između 6 i 8 slučajeva na 100.000 stanovnika [1,15]. Veće stope su zabeležene kod muškaraca i mlađih odraslih osoba. Poseban izazov predstavlja činjenica da veliki broj subkliničkih i blagih slučajeva, uključujući one dijagnostikovane u sklopu MINOCA-e (infarkt miokarda sa neobstruktivnim koronarnim arterijama), ostaje nedijagnostikovan [6,9], što može dovesti do potcenjivanja stvarne incidence i prevalence hroničnih oblika bolesti. IMPS se klasifikuje na sledeće kliničke entitete: Izolovani perikarditis, Izolovani miokarditis, Mioperikarditis (dominantan perikarditis sa blagim miokardnim oštećenjem), Perimiokarditis (dominantan miokarditis sa perikardnim znakovima) i Hronična inflamatorna kardiomiopatija (hronični miokarditis sa strukturnim remodelovanjem, disfunkcijom i aritmogenim supstratom) [1]. ETIOLOGIJA I PATOFIZIOLOGIJA Etiologija miokarditisa i perikarditisa je heterogena. U
razvijenim zemljama dominiraju virusne infekcije (enterovirusi,
adenovirusi, parvovirus B19, humani herpes virus 6, virus influence,
hepatitisa C) [5,16,17] dok u endemskim područjima tuberkuloza
ostaje značajan uzrok perikarditisa, posebno kod predisponiranih
osoba sa HIV infekcijom. Bakterijski uzroci (difterija, borelioza,
stafilokokne infekcije) su ređi. Autoimuni mehanizmi mogu dovesti do
inflamacije u okviru sistemskih bolesti (lupus, sarkoidoza,
vaskulitisi), dok toksični agensi (antraciklini, alkohol, kokain) i
lekovi (inhibitori kontrolnih tačaka-point check inhibitors) takođe
mogu biti uzrok miokarditisa. Genetska osnova je jako važna za
prijemčvost virusne infekcije i težinu kliničke slike, pri čemu su
varijante mutacija u sarkomernim i dezmozomskim genima povezane sa
miokarditisom, a autoinflamatorne bolesti sa rekurentnim
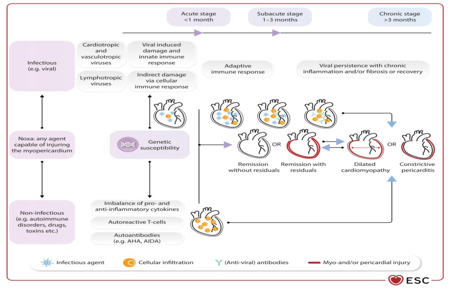
perikarditisom [6,8,15]. Slika 1. Stadijumi inflamatornog mioperikardijalnog sindroma. AHA – anti-srčana antitela; AIDA – antitela na interkalarni disk. preuzeto sa Eur Heart J, Volume 46, Issue 40, 21 October 2025, Pages 3952–4041, https://doi.org/10.1093/eurheartj/ehaf192
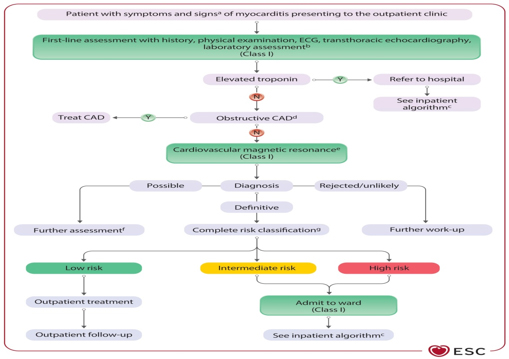
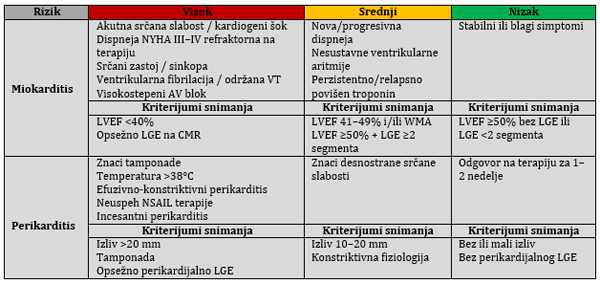
KLINIČKA PREZENTACIJA Klinička prezentacija IMPS je veoma varijabilna. Prema vremenskom toku, miokarditis se deli na: Akutni (≤4 nedelje); Subakutni (4-12 nedelja) i Hronični (>3 meseca, perzistentna inflamacija i remodelovanje). Miokarditis se klinički manifestuje od blagih simptoma u heterogenim formama: asimtomatski blagi miokarditis, bol u grudima, perimiokarditis, srčana insuficijencija, aritmijski tip, iznenadna smrt i fulminantni miokarditis sa fulminantnom srčanom insuficijencijom kardiogenim šokom [6,18-20]. Miokarditis se smatra komplikovanim kada postoji LVEF <50%, akutna srčana insuficijencija, ventrikularne aritmije ili visokostepeni AV blok. Komplikovani oblici mogu pratiti ventrikularne aritmije, AV blokove i značajno sniženje EF [7–9, 18-20] (Slika 2). Slika 2. Dijagnostički algoritam i trijaža za
ambulantne pacijente sa miokarditisom. preuzeto sa Eur Heart J,
Volume 46, Issue 40, 21 October 2025, Pages 3952–4041,
https://doi.org/10.1093/eurheartj/ehaf192
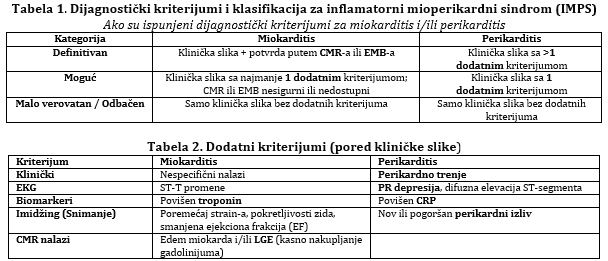
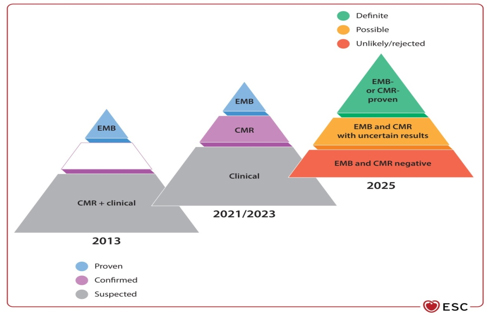
Termin fulminantni miokarditis [21] rezervisan je za bolesnike sa kardiogenim šokom i najtežim oblikom bolesti, koji često zahteva intenzivno lečenje i mehaničku cirkulatornu podršku. Perikarditis se klinički manifestuje kao suvi, eksudaztiv, kao preteća i akutna tamponada srca i ili revrezibilna parcijalna kosntrikcija te hronični konstriktivni oblik [2,4]. Pravovremena diferencijacija između inflamatornih i neinflamatornih fenotipova je ključna. DIJAGNOSTIČKI PRISTUP ESC 2025 preporuke SADA MENJAJU suštinu DIJAGNOSTIKE I STADIJUME U DIJAGNOSTIČKOM PROCESU - dolazi do procene patradigme za dijagnozu, zahvaljujući ogromnoj ulozi kardio-magnetne rezonance (CMR) koja postaje zlatni standard za dijagnozu miokarditisa, dok je sada smanjena uloga endomiokardne biopsije za teže i nejasne, visokorizične slučajeve i zbog odredjivanja adekvatne terapije po patodistološkom tipu sa imunohistohemijom i PCR dijagnozom prisustva virusa u miokardu. RANIJE su bili: suspektan, potvrđen i dokazan a SADA: malo verovatan/odbačen, moguć i definitivan (Slika 3 i Tabela 1 i 2). Tabela 1. Dijagnostički kriterijumi i
klasifikacija za inflamatorni mioperikardni sindrom (IMPS)
CMR – Magnetna rezonanca srca; EMB – Endomiokardna biopsija; LGE – Kasno nakupljanje gadolinijuma (ukazuje na fibrozu ili upalu) Slika 3. Promena paradigme u kliničkoj dijagnozi miokarditisa
CMR, kardiovaskularna magnetna rezonanca; EMB, endomiokardijalna biopsija. I EMB i CMR mogu pružiti konačnu kliničku dijagnozu, ali sa različitim indikacijama. Osnovni dijagnostički elementi: Tabela 3. Algoritam za procenu rizika (risk stratification) i trijažu pacijenata sa sumnjom na miokarditis i perikarditis u ambulantnim uslovima. Hospitalizacija se preporučuje za sve pacijente sa miokarditisom i visokorizičnim perikarditisom.
Invazivna dijagnostika – Endomiokardijalna biopsija (EMB): Endomiokardijalna biopsija (EMB): zlatni standard kod teških formi [17,21,22] i definitivnu dijagnozu i etiološku klasifikaciju. Indikacije su proširene u odnosu na ranije smernice i rezervisane su za visokorizične slučajeve (Tabela 4). Obavezna je molekularno-biološka (PCR) analiza na viruse pre započinjanja imunosupresivne terapije [21-23]. TABELA 4. Indikacije za endomiokardijalnu biopsiju (EMB) prema ESC 2025 [21]
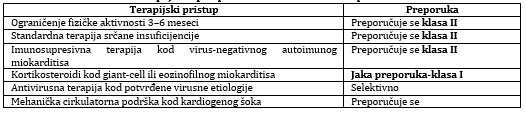
GENETSKO TESTIRANJE Sve je više dokaza o povezanosti miokarditisa sa naslednim kardiomiopatijama. ESC 2025 preporučuje genetsko testiranje kod selektovanih pacijenata sa familijarnim oblicima i rekurentnim perikarditisom [1]. Studije ističu genetske mutacije u dezmozomskim genima kod nasledne predispozicije [1] kod selektovanih pacijenata sa visokim dijagnostičkim prinosom, kao što su: Porodična anamneza kardiomiopatija ili iznenadne srčane smrti, a ritmijska prezentacija bolesti , prisustvo septalnog ili "ring-like" LGE na CMR, trajna sistolna disfunkcija bez oporavka i slučajevi rekurentni miokarditisa ili perikarditis (genetski uzrok se nalazi kod oko 15% bolesnika sa rekurentnim perikarditisom) [1]. TERAPIJA MIOKARDITISA Terapijski pristup je individualizovan i zavisi od etiologije,
kliničke prezentacije i hemodinamskog statusa. Lečenje je
individualizovano prema etiologiji i hemodinamskom statusu [1,6]
(Tabela 5). Kod stabilnih pacijenata primenjuju se analgetici i
NSAID uz kolhicin [1,31]; kod srčane insuficijencije važe standardne
HF smernice (ACEi, ARNI, BB, MRA, SGLT2i) [6,29]. Imunosupresija je
rezervisana za virus negativne oblike [21] ili specifične entitete
poput giant cell i eozinofilnog miokarditisa [22-24]. Kod
fulminantnog miokarditisa preporučuje se mehanička cirkulatorna
podrška (VA ECMO) [1,20]. Sistematizovano je lečenje miokardita
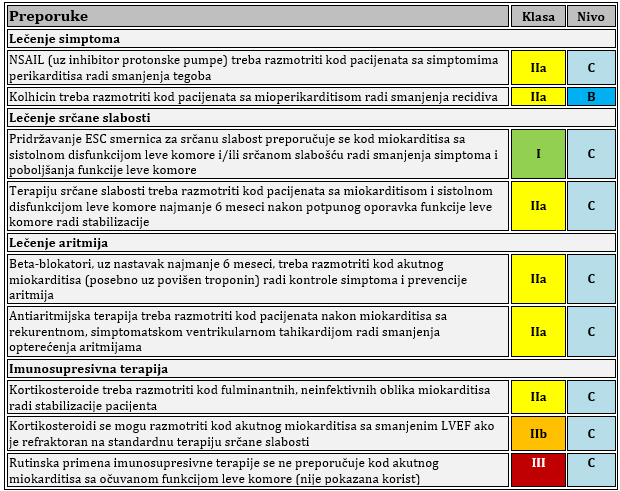
prikazano od 1 do 5 : Tabela 5. Terapijske preporuke za miokarditis prema ESC 2025
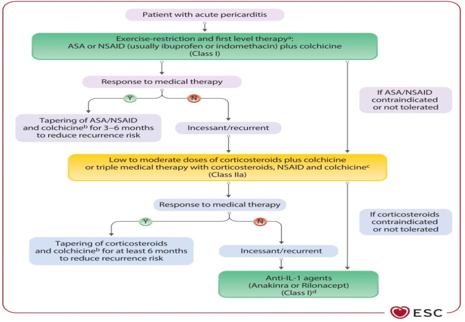
TERAPIJA PERIKARDITISA Prva linija terapije: Aspirin ili NSAID u kombinaciji s
akolhicinom tokom najmanje 3 do 6 meseci (preporuka IA) [1-4]; SLIKA 4. Predloženi algoritam medikamentne terapije za perikarditis kod odraslih (ne uključujući interventne procedure i perikardiektomiju). preuzeto sa Eur Heart J, Volume 46, Issue 40, 21 October 2025, Pages 3952–4041, https://doi.org/10.1093/eurheartj/ehaf192
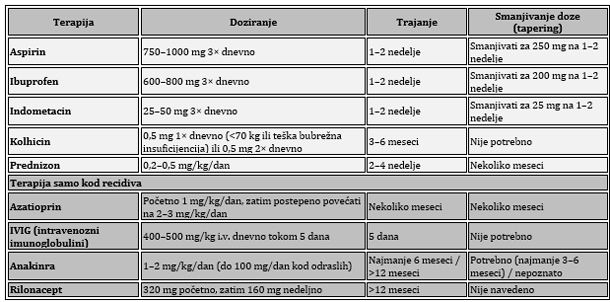
ASA – acetilsalicilna kiselina (aspirin); IL-1 – interleukin-1; CRP – C-reaktivni protein; CMR – magnetna rezonanca srca; LOE (level of evidence) – nivo dokaza; N (no) – ne; NSAID – nesteroidni antiinflamatorni lekovi (NSAIL); Y (yes) – da; A-ASA (aspirin) je prva opcija ako su pacijenti već na antiagregacionoj terapiji aspirinom. Ibuprofen se obično preferira kao prvi NSAIL. Isprobati više od jednog sredstva kako bi se procenio odgovor. Uz primenu aspirina/NSAIL uvek se preporučuje gastroprotekcija inhibitorom protonske pumpe; B-Kolhicin se preporučuje radi sprečavanja recidiva (ponovnog javljanja). Razmotriti primenu od najmanje 3 meseca za prvu epizodu perikarditisa i najmanje 6 meseci za neprekidne/recidivirajuće slučajeve. Kolhicin se isključuje kao poslednji lek tek nakon stabilne remisije; Postepeno smanjivanje doze (tapering) se preporučuje radi smanjenja perzistencije ili recidiva simptoma. Smanjivanje doze je sporije kod kortikosteroida. Postepeno smanjivanje doze kolhicina se obično ne sprovodi zbog trajanja terapije od preko 3–6 meseci. Pod odgovorom na terapiju podrazumevamo kliničku remisiju; C-Niska doza do umerena doza kortikosteroida (npr. prednizon 0,2–0,5 mg/kg dnevno ili ekvivalentne doze alternativnog kortikosteroida); D-Klasa I, nivo dokaza A; Klasa IIa, nivo dokaza C bez obzira na nivoe C-reaktivnog proteina, ukoliko postoji CMR dokaz inflamacije perikarda. TABELA 6. terapijski protokol za lečenje perikarditisa. preuzeto sa Eur Heart J, Volume 46, Issue 40, 21 October 2025, Pages 3952–4041, https://doi.org/10.1093/eurheartj/ehaf192
TABELA 7. ZBIRNE PREPORUKE ESCESC ZA TERAPIJU MIOPERIKARDNOG INFLAMATORNOG SINDROMA
ESC – Evropsko kardiološko društvo; HF – srčana slabost; LV – leva komora; LVEF – ejekciona frakcija leve komore; NSAIL – nesteroidni antiinflamatorni lekovi; VT – ventrikularna tahikardija POSEBNE POPULACIJE Post-COVID miokarditis: Može nastati kao posledica direktne
virusne infekcije, sistemskog inflamatornog odgovora ili imunološke
disfunkcije(25-26). Dijagnoza se često postavlja CMR-om, a terapija
je uglavnom suportivna. Post COVID miokarditis i postvakcinalni
oblici analizirani su u više studija [23–28]. Retki slučajevi
postvakcinalnog miokarditisa nakon mRNA vakcina, najčešće kod mlađih
muškaraca nekoliko dana nakon druge doze. Klinička slika je obično
blaga, a prognoza povoljna. Korist od vakcinacije daleko je veća od
rizika [27-30]. PROGNOZA I PRAĆENJE Prognoza zavisi od početne kliničke prezentacije i etiologije. Najvažniji prediktor nepovoljnog ishoda je biventrikularna disfunkcija. Većina pacijenata sa blagim oblikom bolesti ima dobar oporavak. Kod manjeg broja pacijenata može doći do razvoja dilatativne kardiomiopatije i hronične srčane insuficijencije. [14, 15]. Praćenje pacijenata nakon akutnog miokarditisa je sistematsko tokom prvih 6 do 24 meseca i uključuje: kliničke kontrole, EKG, Holter monitoring, biomarkere (troponin, CRP)i ehokardiografiju, test opterećenja i CMR u odabranim slučajevima [1]. Prognoza zavisi od stepena disfunkcije leve komore i prisustva fibroze na CMR u [6, 10, 11]. Dijastolna disfunkcija može perzistirati i nakon kliničkog oporavka [12–14]. DISKUSIJA ESC smernice iz 2025. godine donose značajan konceptualni
napredak uvođenjem IMPS, ali i određene dileme. Najveće rasprave
izazivaju:Centralna uloga CMR-a: Iako je CMR postao nezaobilazan,
oslanjanje na njega kao "novi zlatni standard" nosi rizik od
preterane dijagnostike i ograničene dostupnosti. Kontroverzna
preporuka o beta-blokatorima[1,6]: Preporuka za primenu
beta-blokatora kod svih pacijenata sa miokarditisom najmanje 6
meseci, bez obzira na EF, zasnovana je na ograničenim dokazima i
predstavlja najdiskutovaniju tačku vodiča. Kontroverze se odnose i
na pristup genetskom testiranju – ograničeno u ESC u, šire u ACC/AHA
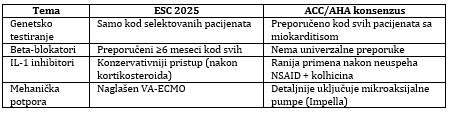
vodičima [3, 4]. Tabela 8. Poređenje ESC 2025 i ACC/AHA smernica2024
ESC 2025 donosi koncept IMPS, naglašava ulogu CMR a i proširuje
indikacije za EMB [1,10,17]. U kontekstu domaće prakse, radovi
autora ovog prtegleda literature Dr Dušana Bastaća značajno
dopunjuju praznine u praktičnoj primeni dijagnostičkih metoda u
inflamatornom miperikardnom sindromu u Srbiji [12–14]. Njegova
istraživanja o dijastolnom stres testu i ehokardiografskim markerima
ukazuju da dijastolna disfunkcija i povišen pritisak punjenja leve
komore (LV filling pressure)mogu perzistirati i nakon oporavka
sistolne funkcije (LVEF), što se uklapa u koncept inflamatorne
kardiomiopatije i fenotip HFpEF (srčana insuficijencija sa očuvanom
ejekcionom frakcijom) kod ovih pacijenata. Ovo naglašava potrebu za
pažljivim, multimodalnim praćenjem, čak i kod bolesnika sa
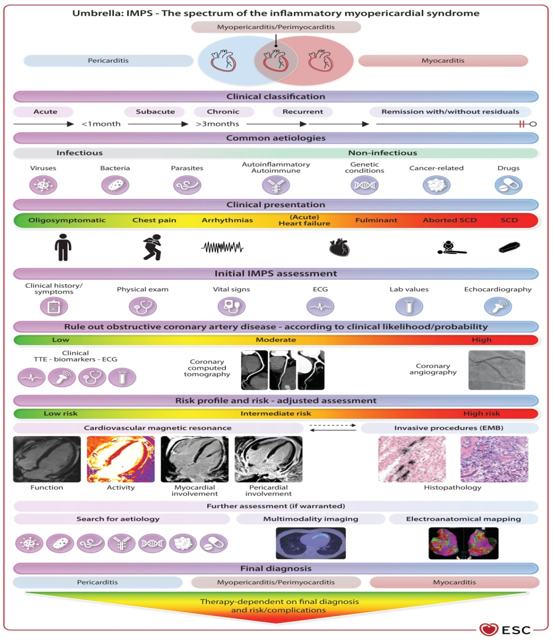
normalizovanom Slika 5. CENTRALNA ILUSTRACIJA ESC SMERNICA O MIOKARDITISU I PERIKARDITISU. preuzeto sa Eur Heart J, Volume 46, Issue 40, 21 October 2025, Pages 3952–4041, https://doi.org/10.1093/eurheartj/ehaf192
ZAKLJUČAK ESC preporuke i smernice iz 2025. godine predstavljaju najkompletniji do sada dokument koji spaja miokarditis i perikarditis u jedinstven koncept – inflamatorni mioperikardijalni sindrom (IMPS),što je prikazano na grafiku (Slika 5): Centralna ilustracija ESC smernica o miokarditisu i perikarditisu. Naglasak je na multimodalnom pristupu dijagnostici, sa centralnom ulogom kardiomagnetne rezonance CMR-a, racionalnoj primeni endomiokardne biopsije (EMB), selektivnoj upotrebi imunosupresije i personalizaciji terapije. Uprkos značajnom napretku, veliki broj preporuka i dalje se zasniva na ekspertskom konsenzusu, što naglašava potrebu za daljim visokokvalitetnim istraživanjima, naročito u oblastima kao što su optimalna upotreba beta-blokatora, novi antivirusni lekovi , genetsko testiranje i biološka terapija. Integracija domaćih kliničkih iskustava pokazuje da se smernice dobro uklapaju u postojeću praksu, ali i da otvaraju nova pitanja i mogućnosti za dalja istraživanja u cilju poboljšanja ishoda pacijenata sa inflamatornim bolestima srca. REFERENCE : 1. European Society of Cardiology. ESC Guidelines for the
Management of Myocarditis and Pericarditis. Eur Heart J. 2025. |
||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||
| Elektronska verzija objavljena: 22.4.2026. | ||||||||||||||||||||||||||||||||||||
| [
Sadržaj
] [ Indeks autora ]
|
||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||