|
|
|
|
UVOD Sindrom
iritabilnog creva (IBS) predstavlja hronični poremećaj interakcije
između gastrointestinalnog trakta i centralnog nervnog sistema, koji
se klinički manifestuje rekurentnim bolom u trbuhu udruženim sa
promenama u učestalosti i/ili konzistenciji stolice. Prema
savremenoj klasifikaciji funkcionalnih gastrointestinalnih
poremećaja, IBS pripada grupi poremećaja interakcije creva i mozga,
kod kojih su simptomi prisutni u odsustvu strukturnih, biohemijskih
ili inflamatornih promena koje bi ih u potpunosti objasnile.
Dijagnoza se postavlja na osnovu kliničkih kriterijuma, uz
isključivanje alarmnih znakova koji bi upućivali na organsku
patologiju [1]. Iako se tradicionalno označava kao „funkcionalni“
poremećaj, savremena istraživanja ukazuju da IBS nije sinonim za
odsustvo patofizioloških promena, već odražava poremećaj regulacije
na više nivoa – neuralnom, imunološkom, mikrobiološkom i
neuroendokrinom. Upravo odsustvo jasnih morfoloških nalaza često je
dovodilo do potcenjivanja težine sindroma, iako je njegov uticaj na
kvalitet života uporediv sa hroničnim inflamatornim bolestima creva
i drugim dugotrajnim oboljenjima [2].
IBS je hronično stanje sa fluktuirajućim tokom, karakterisano
periodima pogoršanja i remisije. Simptomi često uključuju nadimanje,
osećaj nepotpunog pražnjenja, urgentnost ili naprezanje pri
defekaciji, a njihova izraženost ne mora korelirati sa objektivnim
nalazima. Upravo nesrazmera između subjektivnog intenziteta tegoba i
minimalnih laboratorijskih ili endoskopskih promena predstavlja
jedan od dijagnostičkih i terapijskih izazova u svakodnevnoj
kliničkoj praksi.
Posebnu dimenziju sindroma čini visoka učestalost
ekstraintestinalnih manifestacija. Kod obolelih se češće registruju
hronični bolni sindromi, uključujući fibromijalgiju, hronični
karlični bol i tenzionu glavobolju, kao i sindrom hroničnog umora,
poremećaji temporomandibularnog zgloba, nekardijalni bol u grudima i
urinarne tegobe. Anksiozni i depresivni poremećaji takođe su češći u
ovoj populaciji. Ova komorbidnost ukazuje na zajedničke mehanizme
centralne senzibilizacije i poremećaja obrade bola, što dodatno
potvrđuje sistemsku prirodu poremećaja.
Savremeni pristup IBS-u pomera fokus sa isključivo
gastrointestinalnih simptoma ka širem konceptu poremećaja regulacije
osovine mozak–crevo. Interakcija između enteričnog nervnog sistema,
autonomne regulacije, mikrobiote, imunološkog odgovora i psiholoških
faktora oblikuje individualni fenotip bolesti. Ovakvo razumevanje
ima neposredne terapijske implikacije, jer objašnjava zašto
univerzalni terapijski pristup često daje ograničene rezultate i
zašto je personalizacija lečenja od posebnog značaja [3]. Uprkos
tome što IBS ne povećava mortalitet niti dovodi do progresivnog
oštećenja creva, njegov javnozdravstveni značaj je veliki. Sindrom
je povezan sa učestalim konsultacijama lekara, dijagnostičkim
procedurama i smanjenom radnom produktivnošću. Psihološki teret,
stigmatizacija i hronična priroda simptoma dodatno utiču na kvalitet
života pacijenata. [4] Razumevanje IBS-a zahteva integrativni
pristup koji objedinjuje kliničke kriterijume, epidemiološke podatke
i savremena saznanja o patofiziološkim mehanizmima. U tom kontekstu,
sindrom iritabilnog creva treba posmatrati ne kao jedinstvenu
bolest, već kao heterogeni klinički entitet sa različitim
dominantnim mehanizmima, što otvara prostor za precizniji
dijagnostički i terapijski pristup.
Epidemiologija
Sindrom iritabilnog creva predstavlja jedan od najčešćih poremećaja
digestivnog sistema u opštoj populaciji. Studije zasnovane na
populaciji često procenjuju prevalenciju sindroma iritabilnog creva
od 10% do 15%, i incidencu IBS na 1-2% godišnje. Prevalencija se
značajno razlikuje među zemljama. Najniža prevalencija je u
Francuskoj (1,1%), a najviša u Meksiku (35,5%); prevalencija od 7,1%
je pronađena u SAD/Evropi/Australiji/Novom Zelandu. Približno 50%
ljudi sa IBS-om prijavljuje simptome koji počinju pre 35. godine
života. Adolescentkinje i mlade odrasle žene najčešće su pogođene
IBS-om. U zapadnim zemljama, žene imaju 2-3 puta veću verovatnoću
da razviju IBS nego muškarci, iako na indijskom potkontinentu
muškarci predstavljaju 70-80% pacijenata sa IBS-om [5]. Razlike u
prevalenciji delimično su posledica metodoloških faktora,
uključujući upotrebu različitih verzija Roma kriterijuma, ali i
kulturnih i zdravstvenih obrazaca koji utiču na javljanje lekaru.
Geografske varijacije su izražene, sa višom prevalencijom u
pojedinim delovima Azije i u nekim evropskim zemljama, dok su u
drugim regionima zabeležene niže stope. Razlozi ove razlike
verovatno uključuju hormonske faktore, razlike u percepciji i obradi
bola, kao i obrasce traženja zdravstvene zaštite. Sindrom se
najčešće dijagnostikuje kod osoba mlađih od 50 godina, dok je
prevalencija niža u starijoj populaciji. Ova razlika može odražavati
spontanu remisiju simptoma kod dela pacijenata, ali i promene u
percepciji tegoba ili obrascima javljanja lekaru. Najveća
prevalencija je primećena kod obrazovanih, bogatih, studenata i
mlađih osoba. [6]. Međutim, IBS je univerzalno prisutan poremećaj,
bez obzira na etničku ili kulturnu pripadnost, što potvrđuje njegov
multifaktorski karakter.
Porodična agregacija IBS-a ukazuje na genetsku komponentu, ali i na
uticaj zajedničkih faktora sredine. Studije pokazuju da je sindrom
približno dvostruko češći kod rođaka prvog stepena srodstva u
poređenju sa opštom populacijom. Ipak, precizan doprinos genetskih
faktora u odnosu na naučene obrasce ponašanja i zajedničke stresore
ostaje predmet istraživanja.
Značajan epidemiološki entitet predstavlja postinfektivni IBS. Nakon
akutnog gastroenteritisa, rizik razvoja hroničnih simptoma
kompatibilnih sa IBS-om višestruko je povećan. Ovaj rizik je posebno
izražen kod težih infekcija, produženog trajanja simptoma i
prisustva psiholoških stresora u periodu oporavka. Pokrenut
bakterijskim ili virusnim infekcijama, uključuje perzistentnu upalu
niskog stepena, izmenjenu propustljivost creva i izmenjenu
mikrobiotu i jasno demonstrira vezu između inflamacije, imunološke
aktivacije i dugotrajnih promena u neuromišićnoj funkciji creva [7].
Psihosocijalni faktori imaju i epidemiološki značaj. Hronični stres,
traumatska iskustva u detinjstvu i nepovoljni životni događaji
povezani su sa većim rizikom razvoja IBS-a i težim tokom bolesti.
Ovi faktori ne deluju izolovano, već kroz modulaciju osovine
mozak–crevo i percepcije visceralnih signala. [8].
Prirodni tok IBS-a je varijabilan. U populacionim studijama
prevalencija pokazuje relativnu stabilnost tokom vremena, ali kod
10–40% pacijenata dolazi do remisije simptoma tokom višegodišnjeg
praćenja. Sindrom retko prelazi u organsku bolest i nije povezan sa
povećanim mortalitetom, ali je povezan sa značajnim smanjenjem
kvaliteta života i povećanom potrošnjom zdravstvenih resursa. [9]
Etiopatogeneza
Etiopatogeneza sindroma iritabilnog creva (IBS) nije u potpunosti
razjašnjena, ali se danas smatra rezultatom kompleksne interakcije
genetskih, neurobioloških, imunoloških, mikrobioloških i
psihosocijalnih faktora. Savremeni koncept zasniva se na
biopsihosocijalnom modelu, prema kojem genetska predispozicija, u
kombinaciji sa faktorima sredine – poput akutnih gastrointestinalnih
infekcija, hroničnog stresa i nepovoljnih događaja u ranom
detinjstvu – dovodi do poremećaja regulacije osovine mozak–crevo.
IBS se stoga posmatra kao poremećaj regulacije, a ne strukture, pri
čemu se patofiziološki mehanizmi razlikuju po intenzitetu i
kombinaciji među pojedinim podtipovima pacijenata [10].
Jedan od centralnih mehanizama je visceralna hipersenzitivnost.
Kod približno 60% pacijenata dokazan je snižen prag percepcije
mehaničkih i hemijskih stimulusa u digestivnom traktu. Periferna
senzibilizacija enteričnih neurona, ali i pojačana centralna obrada
bola, dovode do intenzivnije percepcije inače fizioloških stimulusa.
Slikovne studije centralnog nervnog sistema ukazuju na povećanu
aktivaciju prednjeg cingularnog korteksa i amigdale – regija
uključenih u emocionalnu obradu bola – uz smanjenu aktivaciju
prefrontalnog korteksa, koji učestvuje u kognitivnoj modulaciji. Ove
promene ukazuju na centralnu amplifikaciju visceralnih signala i
objašnjavaju zašto bol kod IBS-a nije proporcionalan objektivnim
nalazima [11].
Imunološka aktivacija niskog intenziteta predstavlja drugi
važan mehanizam. Posebno je izražena kod postinfektivnog IBS-a, gde
je dokumentovana povećana infiltracija T limfocita i mastocita u
crevnoj sluzokoži. Mastociti, putem oslobađanja histamina, proteaza
i citokina, doprinose senzibilizaciji perifernih neurona i
poremećaju barijerne funkcije epitela. Povećana koncentracija
luminalnih proteaza dodatno pojačava aktivaciju enteričnog nervnog
sistema. Ova mikroinflamacija, iako blaga, može imati dugotrajan
efekat na neuromišićnu funkciju creva [12].
Poremećaji serotoninskog sistema takođe imaju značajnu
ulogu. Serotonin (5-HT), koji se sintetiše u enteroendokrinim
ćelijama, ključan je regulator motiliteta, sekrecije i senzorne
funkcije creva. Kod pacijenata sa IBS-om opisan je poremećen
metabolizam serotonina, što doprinosi promenama tranzita. Motorički
poremećaji uključuju pojačanu aktivnost na gladno i postprandijalno,
kao i izmenjen odgovor na stres. Ubrzan tranzit prisutan je kod
približno polovine pacijenata sa dijarejnim podtipom (IBS-D), dok je
usporen tranzit karakterističan za deo pacijenata sa konstipacionim
podtipom (IBS-C). Kod oko četvrtine bolesnika sa IBS-D utvrđeno je
povećano prisustvo žučnih kiselina u kolonu, što doprinosi povećanoj
sekreciji i motilitetu, dok njihovo smanjeno fenotipa [13].
Mikrobiota predstavlja još jedan ključni element u
patogenezi. Meta-analize su pokazale izmenjen sastav crevne
mikrobiote kod pacijenata sa IBS-om u poređenju sa zdravim
kontrolama, uz smanjenu raznovrsnost i promene u zastupljenosti
pojedinih bakterijskih rodova. Disbioza može uticati na sintezu
serotonina, modulaciju imunološkog odgovora, produkciju
kratkolančanih masnih kiselina i integritet epitelne barijere.
Studije koje pokazuju poboljšanje simptoma nakon primene određenih
antibiotika ili probiotika dodatno podržavaju ulogu mikrobiote u
razvoju sindroma. Povećana intestinalna permeabilnost, dokumentovana
kod dela pacijenata, predstavlja važnu kariku između stresa,
mikrobiote i imunološke aktivacije, omogućavajući povećani prolaz
antigena i senzibilizaciju imunološkog sistema[14].
Psihološki faktori i stres imaju značajan modulacioni
efekat. Hronični stres, traumatska iskustva u detinjstvu i
maladaptivni obrasci suočavanja, poput straha od katastrofe i
stalnog straha i opreza od opasnosti, povezani su sa povećanom
percepcijom simptoma. Aktivacija ose
hipotalamus–hipofiza–nadbubrežna žlezda dovodi do oslobađanja
kortikotropin-oslobađajućeg faktora (CRF), koji utiče na autonomnu
regulaciju, motilitet, sekreciju i imunološki odgovor.
Eksperimentalni modeli pokazuju da akutni stres povećava visceralnu
osetljivost i propustljivost creva. Dominacija simpatičkog nad
parasimpatičkim nervnim sistemom češće se registruje kod pacijenata
sa izraženijim simptomima, iako uzročni odnos ostaje nedovoljno
razjašnjen [15].
Genetska predispozicija predstavlja dodatni faktor rizika.
Studije blizanaca pokazuju veću podudarnost simptoma IBS-a kod
monozigotnih u odnosu na dizigotne blizance. Genomske analize
identifikovale su varijante gena povezane sa funkcijom jonskih
kanala, autonomnom regulacijom, kontraktilnošću glatkih mišića i
mehaničkom osetljivošću. Kod manjeg broja pacijenata opisane su
mutacije gena za enzim saharoza–izomaltaza, koje dovode do
malapsorpcije ugljenih hidrata i kliničke slike slične IBS-u.
U celini posmatrano, IBS predstavlja heterogeni sindrom u kome se
neuralni, imunološki, mikrobiološki i psihoneuroendokrini mehanizmi
međusobno prepliću. Različite kombinacije i dominacija pojedinih
patofizioloških puteva verovatno objašnjavaju kliničku raznolikost
sindroma i različit terapijski odgovor. Ovakvo razumevanje
etiopatogeneze otvara prostor za personalizovani terapijski pristup,
zasnovan na identifikaciji dominantnog mehanizma kod pojedinačnog
pacijenta.
Dijagnostički pristup
Savremeni dijagnostički pristup sindromu iritabilnog creva (IBS)
zasniva se na konceptu postavljanja pozitivne kliničke dijagnoze, a
ne isključivo na principu dijagnoze isključenja. Ovakav pristup ima
za cilj da smanji nepotrebne dijagnostičke procedure, skrati vreme
do započinjanja terapije i umanji anksioznost pacijenata.
Lečenje sindroma iritabilnog creva (IBS) zahteva temeljnu anamnezu i
kliničku procenu, rezultate prethodnih dijagnostičkih testova i
pažljivo praćenje. Polovina pacijenata sa IBS-om ima
ekstraintestinalne simptome (glavobolja 23–45%, bol u leđima 27–81%,
umor 36–63%, mijalgija 29–36%, dizurični simptomi 21–61%).
Ekstraintestinalni simptomi su češći kod žena, posebno tokom
menstruacije. U zavisnosti od težine simptoma i težine bolesti,
pacijenti su podeljene u tri grupe prema skali težine simptoma IBS-a
.Pacijenti u grupi sa blagim simptomima se obično leče na nivou
primarne zdravstvene zaštite. Njihov kvalitet života nije značajno
smanjen. Grupa sa umerenim simptomima se leči na nivou sekundarne
zdravstvene zaštite, a grupa sa teškim simptomima se obično leči na
tercijarnom nivou [16].
Dijagnoza se postavlja na osnovu Roma IV kriterijuma koji
podrazumevaju kontinuirane tegobe pacijenta u poslednja 3 meseca,
koje su se prvi put pojavile najmanje 6 meseci ranije. Osetljivost i
specifičnost dijagnostičkih kriterijuma su 62,7% i 97,1%,
respektivno.
To je rekurentni bol u trbuhu, prisutan u proseku najmanje jedan dan
nedeljno u poslednja 3 meseca i povezan sa najmanje dva od sledećih
kriterijuma: 1, pražnjenje stolice, 2. promena učestalosti stolice,
3. promena konzistencije stolice. Slika 1 [9].
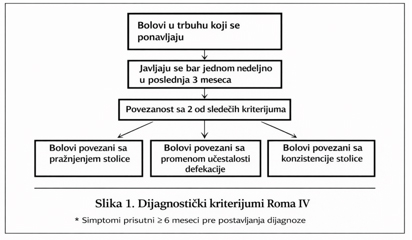
Slika 1. Dijagnostički kriterijum Roma IV
Drugi simptomi pored bola su: 1.abnormalna učestalost stolice (<
3 stolice nedeljno ili > 3 stolice dnevno), 2. naprezanje tokom
defekacije, urgentnost defekacije ili osećaj 3. nepotpunog
pražnjenja creva, iscedak sluzi [17]
Prema preovlađujućim simptomima koji prate hronični bol u trbuhu u
poslednja 3 meseca, razlikujemo četiri podtipa IBS-a:
- IBS sa pretežno zatvorom (IBS-C) – više od25%
pražnjenja creva sa rezultatom 1 ili 2 na Bristolskoj skali
stolice i manje od 25% pražnjenja creva sa rezultatom 6 ili 7 na
Bristolskoj skali stolice,
- IBS sa pretežno dijarejom (IBS-D) – više od 25%
pražnjenja creva sa rezultatom 6 ili 7 na Bristolskoj skali
stolice i manje od 25% pražnjenja creva sa rezultatom 1 ili 2 na
Bristolskoj skali stolice,
- Mešoviti IBS (IBS-M) – više od 25% pražnjenja creva
sa rezultatom 1 ili 2 na Bristolskoj skali stolice i više od 25%
pražnjenja creva sa rezultatom 6 ili 7 na Bristolskoj skali
stolice Skala stolice Bristolska skala stolice,
- Neopredeljeni IBS (IBS-U) – ispunjava dijagnostičke
kriterijume za sindrom iritabilnog creva koji se ne može
klasifikovati ni u jedan od navedenih podtipova . Slika 2 [9].
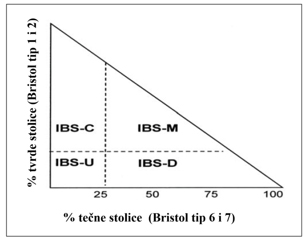
Slika 2. Podtipovi sindroma iritabilnog creva
Ključna komponenta inicijalne procene jeste
identifikacija alarmnih simptoma koji mogu ukazivati na organsku
bolest. U njih spadaju: neobjašnjeni gubitak telesne mase,
gastrointestinalno krvarenje, anemija, noćni simptomi, porodična
anamneza kolorektalnog karcinoma ili inflamatorne bolesti creva, kao
i početak simptoma nakon 50. godine života. Prisustvo ovih znakova
zahteva proširenu dijagnostiku, uključujući endoskopske i radiološke
metode.
Kod pacijenata bez alarmnih simptoma preporučuje se ograničena
inicijalna laboratorijska obrada. Ona obično uključuje kompletnu
krvnu sliku, C-reaktivni protein (CRP) ili sedimentaciju eritrocita,
kao i serološko testiranje na celijakiju, posebno kod bolesnika sa
dijarejskim simptomima. Fekalni kalprotektin predstavlja koristan
neinvazivni biomarker u diferencijaciji IBS-a od inflamatorne
bolesti creva, jer normalne vrednosti sa visokom verovatnoćom
isključuju aktivnu inflamaciju [1].
Endoskopska evaluacija nije rutinski indikovana kod mlađih
pacijenata bez alarmnih znakova. Međutim, kolonoskopija se
preporučuje kod osoba starijih od 50 godina u skladu sa skrining
preporukama za kolorektalni karcinom, kao i kod pacijenata sa
perzistentnim ili atipičnim simptomima. Kod pacijenata sa hroničnom
dijarejom treba razmotriti biopsiju kolona radi isključivanja
mikroskopskog kolitisa, čak i u odsustvu makroskopskih promena.
Diferencijalna dijagnoza IBS-a zavisi od
dominantnog kliničkog fenotipa. Kod IBS-D treba isključiti
inflamatornu bolest creva, celijakiju, infekcije, kao i
malapsorpciju žučnih kiselina. Kod IBS-C
diferencijalno-dijagnostički dolaze u obzir primarni poremećaji
motiliteta, hipotiroidizam i lekovima indukovana konstipacija.
Sindrom bakterijskog prerastanja tankog creva (SIBO) ostaje
kontroverzna dijagnoza, ali se može razmatrati kod izraženog
nadimanja i refraktornosti na standardnu terapiju.
Važan aspekt dijagnostičkog procesa jeste procena psihosocijalnih
faktora. Anksioznost, depresija i hronični stres ne predstavljaju
samo komorbiditet, već mogu modulirati intenzitet simptoma i
terapijski odgovor. Strukturisana procena psihološkog opterećenja
može pomoći u individualizaciji terapijskog pristupa.
Preterana dijagnostika može imati negativne posledice, uključujući
povećanje zdravstvenih troškova i pojačavanje zdravstvene
anksioznosti. Stoga je racionalan, postepeni pristup od posebne
važnosti. Nakon pažljivo uzete anamneze, fizikalnog pregleda i
osnovnih laboratorijskih testova, kod pacijenata bez alarmnih
znakova može se postaviti pouzdana dijagnoza IBS-a i započeti
terapija bez dodatnih invazivnih procedura.
Savremeni dijagnostički koncept IBS-a time odražava razumevanje
sindroma kao poremećaja regulacije, u kojem je klinički obrazac
simptoma od presudnog značaja. Ovakav pristup omogućava bržu
identifikaciju podtipa bolesti, smanjuje nepotrebne intervencije i
predstavlja osnov za personalizovani terapijski plan.
Terapija sindroma iritabilnog creva
Terapijski pristup sindromu iritabilnog creva (IBS) zasniva se na
kombinaciji edukacije pacijenta, dijetetskih mera, farmakoterapije
i, po potrebi, psiholoških intervencija. Zbog heterogenosti
patofizioloških mehanizama, terapija mora biti individualizovana i
usmerena prema dominantnom podtipu bolesti (IBS-C, IBS-D, IBS-M,
IBS-U), kao i prema izraženosti bola, nadimanja i psihosocijalnih
faktora.
Opšti principi terapije
Osnov lečenja čini detaljna edukacija pacijenta. Objašnjenje
benignog toka bolesti i uloge osovine mozak–crevo smanjuje
anksioznost i poboljšava terapijsku saradnju. Važno je naglasiti da
IBS ima hroničan, fluktuirajući tok i da je cilj terapije kontrola
simptoma i poboljšanje kvaliteta života, a ne trajno izlečenje.
Dijetetske mere: pretpostavka da su simptomi
IBS povezani sa ishranom, eliminacione dijete i dodavanje
dijetetskih vlakana retko poboljšavaju simptome na duži rok.Ishrana
po principu FODMAP dijete, koja ograničava fermentabilne
oligosaharide, disaharide, monosaharide i polihidroksialkohole u
ishrani, može poboljšati simptome kod jednog od pet pacijenata
smanjujući nadimanje i bol [18].
Individualna procena intolerancije na laktozu, fruktozu i druge
fermentabilne ugljene hidrate može biti korisna. Preterano
restriktivne dijete treba izbegavati zbog rizika od nutritivnih
deficita i negativnog uticaja na mikrobiotu.
Promene načina života (redovna fizička
aktivnost, adekvatan san i upravljanje stresom) mogu doprineti
ublažavanju simptoma. Kod pacijenata sa umerenim i teškim simptomima
često je potrebna kombinacija farmakološkog i nefarmakološkog
pristupa [9].
Farmakoterapija se bira prema dominantnom simptomu i podtipu
bolesti.
Farmakološko lečenje IBS sa konstipacijom (IBS-C)
Ciljevi terapije su povećanje učestalosti i poboljšanje
konzistencije stolice, uz redukciju bola i nadimanja.
Vlakna (psilijum, metilceluloza, kalcijum polikarbofil)
predstavljaju terapiju prve linije. Meta-analize pokazuju umerenu
efikasnost. Pšenične mekinje nisu pokazale značajnu korist.
Osmotski laksativi (PEG, magnezijumove mineralne vode) poboljšavaju
konzistenciju stolice i smanjuju naprezanje, ali imaju ograničen
efekat na bol i nadimanje. Laktuloza i sorbitol se ne preporučuju
zbog nadimanja. Stimulativni laksativi (sena, bisakodil) se koriste
kratkotrajno.
Kod pacijenata sa perzistentnim simptomima primenjuju se
sekretagogi i prosekretorni lekovi:
Lubiproston (agonist ClC-2 kanala) poboljšava konzistenciju
stolice i smanjuje bol; najčešći neželjeni efekti su mučnina i
dijareja.
Plekanatid (agonist gvanilat ciklaze C) povećava sekreciju i
istovremeno smanjuje visceralnu osetljivost; efikasan deluje i na
bol.
Tenapanor (inhibitor Na+/H+ izmene) povećava sadržaj vode u
stolici i smanjuje abdominalni bol.
Tegaserod (5-HT4 agonist) može se razmotriti kod žena mlađih
od 65 godina bez kardiovaskularnog rizika.
Prokinetik prucaloprid selektivni agonist 5-HT4 receptora ,
stimuliše peristaltiku kolona, posebno kada postoje simptomi
hronične opstipacije i loš odgovor na prethodne lekove
Kod izraženog bola i visceralne hipersenzitivnosti, naročito uz
anksioznost ili depresiju, mogu se primeniti SSRI -selektivni
inhibitori preuzimanja serotonina ili SNRI - inhibitori preuzimanja
serotonina i noradrenalina, dok TCA - triciklični antidepresivi mogu
biti korisni kod bola uz spor tranzit.
Farmakološko lečenje IBS sa dijarejom (IBS-D)
Dominantni simptomi su učestale, tečne stolice, urgentnost i bol.
Loperamid je terapija prve linije. Poboljšava konzistenciju
stolice i smanjuje urgentnost, ali ima ograničen efekat na bol.
Eluksadolin (μ-opioidni agonist i δ-antagonist) smanjuje
dijareju i bol. Kontraindikovan je kod pacijenata bez žučne kese i
kod osoba sa povećanim rizikom od pankreatitisa.
Kod pacijenata sa sumnjom na malapsorpciju žučnih kiselina korisni
su sekvestranti žučnih kiselina (holestiramin).
Rifaksimin, neapsorptivni antibiotik, efikasan je u redukciji
nadimanja i globalnih simptoma; efekat može biti prolazan i terapija
se može ponoviti kod relapsa.
Kod teških i refraktornih oblika mogu se primeniti 5-HT3
antagonisti (alosetron, ondansetron, ramosetron), koji smanjuju
bol, urgentnost i učestalost stolica. Njihova primena zavisi od
regulatornih ograničenja zbog retkog rizika od ishemijskog kolitisa.
Antispazmodici (mebeverin, pinaverin, alverin, ulje
peperminta) ublažavaju bol delovanjem na glatku muskulaturu.
Uloga neuromodulatora: Centralni neuromodulatori (SSRI ,
SNRI, TCA ) danas se definišu kao „modulatori osovine crevo–mozak“.
Koriste se u nižim dozama nego u psihijatriji i imaju za cilj
smanjenje visceralne hipersenzitivnosti i modulaciju centralne
obrade bola.Meta-analize pokazuju da neuromodulatori dovode do
poboljšanja simptoma kod približno jednog od četiri do pet
pacijenata. TCA su pokazale najveću efikasnost u redukciji
abdominalnog bola.
Terapija IBS-M (mešoviti tip)
IBS-M karakteriše smenjivanje dijareje i konstipacije, što zahteva
fleksibilan pristup. Terapija se prilagođava dominantnom simptomu u
datom periodu, uz izbegavanje preterane farmakološke intervencije
koja može dovesti do oscilacija u tranzitu.
Antispazmodici i neuromodulatori imaju centralnu ulogu, jer bol i
nadimanje predstavljaju zajednički imenitelj različitih faza
bolesti. Neuromodulatori utiču na visceralnu senzitivnost i vreme
tranzita: TCA produžavaju tranzit, SSRI ga skraćuju, dok SNRI deluju
pretežno analgetski.
Probiotici (posebno bifidobakterije) mogu smanjiti nadimanje
i bol. Meta-analize potvrđuju globalno poboljšanje simptoma kod
približno jednog od tri lečena pacijenta.
Terapija IBS-U (neklasifikovani tip)
Kod pacijenata koji ne ispunjavaju kriterijume za jasnu
klasifikaciju, terapija je simptomatska i individualizovana. Fokus
je na kontroli bola, nadimanja i regulaciji stolice, uz naglašenu
ulogu dijetetskih i psiholoških intervencija.
Zaključne osnove farmakološkog terapijskog pristupa:
• Lečenje IBS zahteva stepenasti pristup:
• Edukacija i dijetetske mere
• Terapija prema dominantnom simptomu
• Uvođenje sekretornih modulatora ili selektivnih lekova kod
perzistentnih simptoma
• Neuromodulatori kod izraženog bola i hipersenzitivnosti
• Psihološke intervencije kod refraktornih oblika [1]
Nefarmakološko lečenje sindroma iritabilnog creva
S obzirom na centralnu ulogu osovine crevo–mozak u patogenezi
sindroma iritabilnog creva (IBS), psihološke intervencije
predstavljaju važan terapijski modalitet, naročito kod pacijenata sa
izraženom visceralnom hipersenzitivnošću, anksioznošću, depresivnim
simptomima ili hroničnim stresom. Njihova primena zasniva se na
dokazima o centralnoj modulaciji bola i uticaju stresa na motilitet,
permeabilnost i imunološku aktivaciju creva.
Psihološke terapije obuhvataju kognitivno-bihejvioralnu
terapiju (KBT), hipnoterapiju usmerenu na creva, relaksacione
tehnike, programe upravljanja stresom i druge strukturisane
intervencije. Meta-analize pokazuju da psihološki tretman značajno
smanjuje rizik perzistencije simptoma.
Kognitivno-bihejvioralna terapija je najopsežnije proučena
metoda. Usmerena je na prepoznavanje i modifikaciju maladaptivnih
misli i ponašanja koji pojačavaju percepciju bola i održavaju
začarani krug anksioznosti i visceralne hipersenzitivnosti.
Randomizovane studije potvrđuju njenu superiornost u odnosu na
kontrolne intervencije.
Hipnoterapija usmerena na gastrointestinalni trakt deluje
putem centralnih mehanizama modulacije visceralne percepcije.
Studije pokazuju klinički značajno poboljšanje simptoma nakon 6–12
nedelja terapije. Relaksacione tehnike mogu poboljšati kvalitet
života, iako je njihov efekat na osnovne simptome IBS-a manje
konzistentan.
Zbog hroničnog toka bolesti, mnogi pacijenti pribegavaju
komplementarnoj medicini. Akupunktura, prema dostupnim
analizama, verovatno nije superiorna u odnosu na placebo. Dokazi za
lečenje biljem su ograničeni, iako pojedina istraživanja
ukazuju na moguću korist individualizovanih pristupa.
Terapija IBS-a mora biti personalizovana.
Osnovu čine edukacija pacijenta, racionalna dijetetska intervencija
i ciljana farmakoterapija. Kod izražene centralne senzibilizacije i
psiholoških komorbiditeta, kombinacija neuromodulatora i psiholoških
intervencija često daje najbolje rezultate. Individualizovan i
kombinovani pristup odražava savremeno razumevanje IBS-a kao
heterogenog poremećaja regulacije osovine crevo–mozak i omogućava
optimalnu kontrolu simptoma uz minimalno terapijsko opterećenje
pacijenta. [1] Prikaz terapijskog pristupa kod IBS-C i IBS-D je
pokazan na slici 3.

Slika 3. Terapija IBS sa domintntnom konstipacijom
i sa domintnom dijarejom
Zaključak
Sindrom iritabilnog creva predstavlja čest i hroničan
funkcionalni poremećaj koji značajno narušava kvalitet života
pacijenata. Kod bolesnika koji ispunjavaju Roma IV dijagnostičke
kriterijume i nemaju alarmne znake, dijagnoza se može postaviti na
osnovu pažljivo uzete anamneze, analize tipičnih kliničkih simptoma
i fizikalnog pregleda, bez potrebe za opsežnom dijagnostikom.
Nasuprot tome, prisustvo alarmnih simptoma, pojava tegoba nakon
pedesete godine života, pozitivna porodična anamneza na kolorektalni
karcinom, kao i sumnja na celijakiju ili hroničnu inflamatornu
bolest creva, zahtevaju dodatnu laboratorijsku, slikovnu i
endoskopsku obradu.
Lečenje IBS-a započinje detaljnim objašnjenjem prirode poremećaja i
uveravanjem pacijenta da se ne radi o malignoj ili životno
ugrožavajućoj bolesti. Terapija je dugoročna i individualizovana,
usmerena na dominantne simptome i njihov intenzitet. Osnov lečenja
čine edukacija, dijetetske mere i ciljana farmakoterapija, dok kod
pacijenata sa izraženom visceralnom hipersenzitivnošću i psihološkim
komorbiditetima značajnu ulogu imaju neuromodulatori i psihološke
intervencije.
Uspešno lečenje zahteva kontinuiranu i konstruktivnu saradnju između
pacijenta i lekara, uz po potrebi uključivanje drugih specijalista.
Multidisciplinarni i personalizovani pristup odražava savremeno
razumevanje IBS-a kao poremećaja regulacije osovine crevo–mozak i
omogućava optimalnu kontrolu simptoma uz očuvanje kvaliteta života.
Literatura:
1. Huang KY, Wang FY, Lv M, Ma XX, Tang XD, Lv L. Irritable bowel
syndrome: Epidemiology, overlap disorders, pathophysiology and
treatment. World J Gastroenterol. 2023 Jul 14;29(26):4120-4135
2. Videlock EJ, Chang L. Irritable bowel syndrome, In: Wang TC,
Camilleri M, eds. Yamada’s Textbook of Gastroenterology: Seventh
edition. New York: Wiley; 2022. p. 1374–407.)
3. Chey WD, Kurlander J, Eswaran S: Iritable bowel syndrome: a
clinical review. JAMA 2015;313:945–58.
4. Ford AC, et al. Evidence-based clinical practice guidelines for
irritable bowel syndrome. Nat Rev Gastroenterol Hepatol.
2020;17:458–476.
5. Canavan C, West J, Card T. The epidemiology of irritable bowel
syndrome. Clin Epidemiol. 2014. 6:71-80.
6. Husain N, Chaudhry IB, Jafri F, Niaz SK, Tomenson B, Creed F. A
population-based study of irritable bowel syndrome in a non-Western
population. Neurogastroenterol Motil. 2008;20:1022–1029. doi:
10.1111/j.1365-2982.2008.01143.x. ).
7. Thabane M, Marshall JK. Post-infectious irritable bowel syndrome.
World J Gastroenterol. 2009 Aug 7;15(29):3591-6.)
8. Ballou S, Bedell A, Keefer L. Psychosocial impact of irritable
bowel syndrome: A brief review. World J Gastrointest Pathophysiol.
2015 Nov 15;6(4):120-3.
9. Štabuc B. Sindrom razdražljivega črevesa - najpogosteša
funkcionalna črevesna bolezen Slovenian Journal of Gastroenterology
/ Gastroenterolog 2024; 3: 52–6
10. Tang HY, Jiang AJ, Wang XY, et al. Uncovering the
pathophysiology of irritable bowel syndrome by exploring the
gut-brain axis: a narrative review. Ann Transl Med. 2021 Jul.
9(14):1187).
11. Van den Houte K, Bercik P, Simren M, Tack J, Vanner S.
Mechanisms underlying food-triggered symptoms in disorders of
gut-brain interactions. Am J Gastroenterol. 2022 Jun 1.
117(6):937-46.
12. Gao J, Xu K, Liu H, et al. Impact of the gut microbiota on
intestinal immunity mediated by tryptophan metabolism. Front Cell
Infect Microbiol. 2018. 8:13. [
13. Camilleri M. Physiological underpinnings of irritable bowel
syndrome: neurohormonal mechanisms. J Physiol. 2014 Jul 15.
592(14):2967-80
14. Kim GH, Lee K, Shim JO. Gut bacterial dysbiosis in irritable
bowel syndrome: a case-control study and a cross-cohort analysis
using publicly available data sets. Microbiol Spectr. 2023 Feb 14.
11(1):e0212522.
15. Ng QX, Yaow CYL, Moo JR, Koo SWK, Loo EXL, Siah KTH. A
systematic review of the association between environmental risk
factors and the development of irritable bowel syndrome. J
Gastroenterol Hepatol. 2024 May 3.
16. Francis CY, Morris J, Whorwell PJ. The irritable bowel scoring
system: a simple method of monitoring IBS and its progress. Aliment
Pharmacol Therapeut 1997;11:395–402.
17. Palsson OS, Whitehead WE, Miranda AL, Chang L, Chey W, Crowel
MD. Development and validation of the Rome IV diagnostic
questionnaire for adults. Bowel disorders. Gastroenterology
2016;150:1481–91.)
18. Bijkerk CJ, de Wit NJ, Muris JWM, Whorwell PJ, Knottnerus JA,
Hoes AW. Soluble or insoluble fibre in irritable bowel syndrome in
primary care? Randomised placebo controlled trial. BMJ
2009;339:b3154. |
|
|
|



