|
|
|
|
UVOD Hronična srčana slabost je progresivni kompleksni
sindrom koji predstavlja završnu fazu različitih kardiovaskularnih
oboljenja i jedan je od vodećih uzroka morbiditeta i mortaliteta
širom sveta, dok je akutna srčana insuficijencija najteži klinički
oblik sa kardiogenim edemom pluća i kardiogenim šokom, sa najvećom
smrtnošću, zahteva hitno bolničko lečenje, ali je srećom mnogo ređa
od hronične srčane insuficijencije. Prevalencija u opštoj populaciji
procenjuje se na 1–2%, dok kod starijih od 75 godina dostiže i do
10% [1,2]. Globalno, više od 64 miliona ljudi živi sa ovim
oboljenjem, a očekuje se dalji porast usled starenja populacije [3].
Dekompenzovana hronična srčana insuficijencija karakteriše se
zastojem u malom i/ili velikom krvotoku i nakupljanjem tečnosti u
organizmu. Najteži oblik ovog procesa je anasarka, difuzni
generalizovani edem koji može uključivati ascites, pleuralne izlive
i perikardni izliv [4]. Anasarka se, pored srčane insuficijencije,
javlja i u drugim stanjima (nefrotski sindrom, ciroza jetre, teške
hipoalbuminemije), ali u kontekstu srčane slabosti označava
terminalni stadijum, iscrpljenost kompenzatornih mehanizama i lošu
prognozu [5]. Dijagnostika i terapija pacijenata sa anasarkom su
izazovni, jer je često prisutna kombinacija kardijalne, renalne i
hepatičke disfunkcije. Terapija se zasniva na agresivnoj i
individualizovanoj intravesnkoj diuretskoj terapiji, korekciji
elektrolita, optimizaciji hemodinamike i uključivanju konsultanata
[6]. Ovaj prikaz slučaja je jako značajan jer ukazuje da težak oblik
srčane insuficijencije, naizgled refrakternog terminalnog stadijuma
DHSI može da se uspešno leči intenzivnom terapijom sa dominacijom
intravenske diuretske terapije visokim dozama Furosemida uz ostale
stubove lečenja HSI u zbrinjavanju pacijenata sa anasarkom.
Savremeni pristup lečenju HSI zasniva se na tzv. „četiri stuba
terapije“ (ARNI/ACEI, beta-blokatori, MRA i SGLT2 inhibitori), koji
značajno smanjuju mortalitet i hospitalizacije [6,7,8,9] a isto tako
važan i u anasarki presudan je peti stub- diuretska terapija
intravenskim diuretikom henleove petlje.
PRIKAZ SLUČAJA
Osnovni podaci o pacijentu: gospodin K.A., 88 godina,
antropometrijski parametri: telesna masa: 78 kg, telesna visina 167
cm, indeks telesne mase (BMI) 29,4 kg/m2, telesne površine (BSA)
1,9m2, obim struka 92cm i saturacija krvi kiseonikom (SpO2) 96%.
Pacijent je 06.06.2025. godine primljen u stanju teške
dekompenzacije hronične srčane insuficijencije sa izraženom
kongestijom i anasarkom, što predstavlja klinički indikator
uznapredovale bolesti [5].
Anamneza: Pacijent se javio zbog progresivne dispneje, otoka
potkolenica i podlaktica i sa izraženom slabošću, sa zamorom i
gušenjem na najmanji napor i u miru posle napora. Tegobe su prisutne
poslednjih 14 dana, sa brzom progresijom bolesti. Pojačano zamaranje
ima unazad dve nedelje (nije mogao da se popne na prvi sprat),
praćeno ubrzanim i nepravilnim srčanim radom, velikim otokom
potkolenica a zatim i podlaktica. Pregledan od strane interniste u
bolnici pre nedelju dana i tada je uvedena mala doza Furosemid tbl
40 mg 1x1 peroralno, Spironolakton tbl 25mg i Rivaroxaban tbl a 15mg
1x1. Negira bolove u grudima. Krvni pritisak (TA) kod kuće je
uglavnom niži. Pacijent navodi da je lečio hipertenziju unazad 4
godine a da pre toga nije uzimao lekove za srce.
Predhodna terapija koju je pacijent uzimao duže vreme: Bisoprolol 5
mg tableta (tbl) 1+0+1/2, Rivaroxaban 15 mg tbl 1x1, Ramipril +
Hidrohlortiazid 5/25 mg tbl 1x1 ujutru, Ramipril 5 mg tbl 1x1 uveče,
Alopurinol 100 mg tbl 1x1, Furosemid 40 mg tbl 1x1, Spironolacton 25
mg tbl 1x1 i suplementacija gvožđa tbl 30mg 1x1.
Fizikalni status na prijemu:
Opšti status: bled i dispnoičan, acijanotičan, afebrilan.
Vitalni parametri: TA 110/60, frekvenca srca oko 82/min, nepravilan
ritam. Saturacija kiseonikom (SpO₂) je 95%. Koža i sluznice blede.
Pluća auskultatorno: disajni šum oslabljen, obostrano bazalno
nečujno disanje; perkutorni zvuk bazalno tmuo obostrano.
Srce: palpatorno proširen iktus, Frekvenca (Fr) 82/min,
tonovi oslabljeni, ritam nepravilan po tipu atrijalne fibrilacije,
holosistolni regurgitacioni sistolni šum nad iktusom 2-3/6, bez
propagacije.
Abdomen: jetra se palpira 4 cm ispod desnog rebarnog luka
(DRL) na medioklavikularnoj liniji, meke konzistencije; slezina se
ne palpira. Bez znakova za ascit.
Ekstremitetii: Testasti i hladni veliki edemi potkolenica
(desno subpatelarno mensuracija daje obim 41cm, na sredini tibije
36cm, supramaleolarno 25cm; leva strana respektivno 35cm, 34cm,
27cm); blag otok šaka i podlaktica.
Laboratorijske analize:
NT-proBNP: 1314 pg/ml (<526 za dob pacijenta),
D-dimer: 0,46 (<0.4) μg/ml,
Urea: 17 mmol/L,
Kreatinin: 133µmol/L,
GFR 44 ml/min/1,73 m2,
Jetreni enzimi: AST 96 U/L, ALT 165 U/L,
Hemoglobin: 68 g/L, Er 3.65x1012, MCV 67,7 fL
Laboratorijski nalazi su ukazivali na HSI sa kardiorenalnim
sindromom i teškom anemijom, koji su česti komorbiditeti i dodatno
pogoršavaju prognozu [10,11,12].
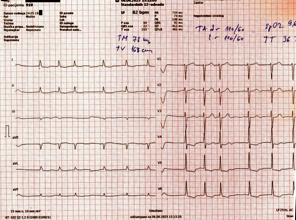
ELEKTROKARDIOGRAM (EKG): Fibrilacija pretkomora sa
apsolutnom aritmijom komora, srčana frekvenca Fr=82/min, zbirni
vektor srčane osovine intermedijaran, normalno trajanje QRS
kompleksa, povremene VES, depresija ST do 2mm i negativan T u V4-V6,
depresija ST do 0.5mm i negativan T u D1, D2, aVL (Slika 1).
Slika 1. -ELEKTROKARDIOGRAM (EKG) na prijemu
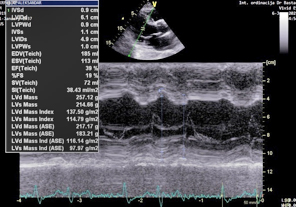
EHOKARDIOGRAFIJA: U nalazu dominira dilatacija leve
komore, normalne debljine zidova leve komore , bez hipertrofije
miokarda i sa sniženom globalnom sistolnom funkcijom: ejekciona
frakcija (EF) leve komore je 39% u M modu (Teicholtz) (Slika 2), a
po Simpsonu 35% i 39%, a biplejn 37% (Slika 3,4).
Slika 2. M MOD EHOKARDIOGRAM ejekciona frakcija
EF=39% po Teicholz-u
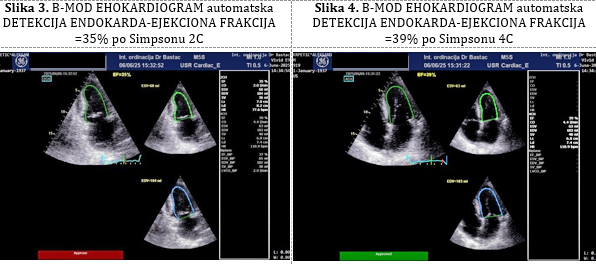
Slika 3. B-MOD EHOKARDIOGRAM automatska DETEKCIJA
ENDOKARDA-EJEKCIONA FRAKCIJA =35% po Simpsonu 2C Slika 4. B-MOD
EHOKARDIOGRAM automatska DETEKCIJA ENDOKARDA-EJEKCIONA FRAKCIJA =39%
po Simpsonu 4C
Na inferiornom zidu manja aneurizma bazalnog segmenta sa
suspektnim organizovanim trombom. Anteroapikalno i
anteroseptoapikalno diskinezija. Najreprezentativniji parametar
dijastolne funkcije E/e' odnos je jako povišen 15,0 (normalno <8,0,
E/e'- odnos transmitralne brzine ranog punjenja leve
komore-E/srednje brizine mitralnog anulusa na tkivnom dopleru-e').
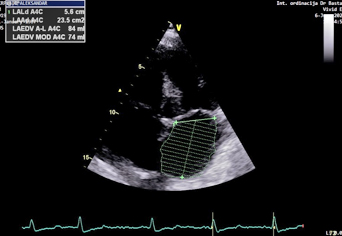
Leva pretkomora je dilatirana, indeks zapremine leve pretkomore
(LAVI) je 45 ml/m2 (normalno<34 ml/m2) (Slika 5). Izmerena je
maksimalna brzina (Vmax) trikuspidne regurgitacije 3,3 m/s
(trikuspidni gradijent je 44mmHg) a sistolni pritisak desne komore
je 64mmHg.
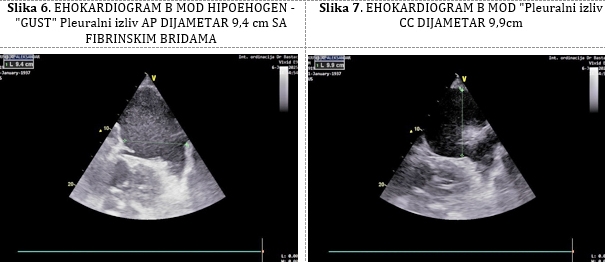
Ultrazvuk pluća: Hidrotoraks, anteroposteriorno (AP) bazalno
pleuralni, hipoehogeni "gust" izliv
levo 9,9 x 9,4cm (Slika 6, 7), APdijametar 6,5x4,6cm na nivou
angulusa skapule,
desno 3cm ispod angulusa skapule AP, 7,0 x 7,0cm, lateralno 7,0 x
10,0cm
Slika 5. indeks zapremine leve pretkomore(LAVi)
Radne dijagnoze: Insuff cordis congestiva I50 (srčana
slabost sa ehokardiografski redukovanom ejekcionom frakcijom leve
komore HFrEF=-35%) sa pratećim kardiološkim dijagnozama: Fibrillatio
atriorum permanens, Cicatrix myocardii post infarctum parietis
inferioris, Aneurysma functionalis ventriculi sinistri cordis
parietis inferioris, Hydrothorax billateralis, Insuff valvulae
mitralis et valvulae semilunaris aortae i Hypertensio arterialis
pulmonalis. Prisutni su komorbiditeti: Morbus renalis gradus 3b;
Anemia microcytica syderopenica chronica gradus gravis.
DALJI TOK BOLESTI DECURSUS MORBI
Pacijent odbija predloženu hospitalizaciju na Internom odeljenju
bolnice ZC Zaječar, upozoren na životno ugrožavajuće stanje koje se
leči u intenzivnoj nezi bolnice. Praćen je u dnevnoj bolnici naše
ordinacije putem EKG monitoringa, merenjem krvnog pritiska i
diureze, saturacije krvi i ostalih vitalnih parametara. Zbog anemije
indikovana transfuzija deplazmatisanih eritrocita (za koju se nije
javljao Službi za transfuziju).
Pacijentu je odmah uvedena intenzivirana parenteralna diuretska
terapija: na dan pregleda Furosemid amp a 20mg No VIII (160mg) u 2
intravenska bolusa, što je u skladu sa preporukama za lečenje akutne
dekompenzacije [6,13,14].
Rana i agresivna diuretska terapija dovela je do značajne redukcije
volumenskog opterećenja, što je ključni terapijski cilj [13,14,15].
Dobija se odlična, promptna diureza. Sutradan dobija Furosemid
intravenski amp a 20mg No IV (80mg). Korigovana je predhodna kućna
terapija: Bisoprolol tbl 5mg 2x1/2; Rivaroxaban 15mg 1x1;
Spironolakton 25mg 1x1 i suplement gvožđa a prekinuta terapija tbl
Ramipril + Hidrohlortiazid 5/25mg 1x1ujutru, tbl Ramipril 5mg
1x1uveče, tbl Alopurinol 100mg 1x1. Uvedeni su ARNI:
Valsartan+Sakubitril 26/24mg 2x1/2; tbl Dapagliflozin 10mg 1 x 1 što
je u skladu sa savremenim preporukama [7,8,16-18]. Zbog bolje
korekcije anemije uvedena je maksimalna doza preparata gvoždja
umesto ranijeg suplementa gvoždja (300mg/dan).
Korekcija anemije sprovedena je zbog njenog negativnog uticaja na
funkcionalni status i ishod bolesti, pojačavajući tkivnu hipoksiju
[12,19]. Pacijentu je od nefarmakoloških mera lečenja savetovana
restrikcija unosa tečnosti i soli i zabrana fizičkih aktivnosti. Uz
ovu terapiju postepeno je došlo do sve veće diureze i značajnog
smanjenja edema.
Na prvoj kontroli već trećeg dana lečenja (07.06.2025.
godine). utvrđuje se odličan uspeh u eliminaciji retencije tečnosti:
pacijent je imao 7 kg manje, uz prestanak dispneje na najmanji napor
i uz značajnu redukciju edema potkolenica (mensuracija: desna 40cm,
35cm, 24cm, leva 36cm, 34cm, 24cm) i porast hemoglobina na Hgb 72
g/L. Tada se od 4-tog dana u peroralnu terapiju uvodi Furosemid
forte 1/2 tbl a 500mg , Digoksin tbl a 0.25mg 1/2 na drugi dan zbog
atrijalne fibrilacije i hipotenzije. Upućen na višeslojnu
kompjuterizovanu tomografiju MDCT skener grudnog koša, koji u daljem
toku nije uradio.
Na drugoj kontroli petog dana lečenja (11.06.2025. godine)
pacijent ima 12kg manje i ima minimalne edeme (mensuracija obima
potkolenica: desna 33 cm, 33cm, 24cm a leva: 34cm, 33cm, 24cm).
Nalaz na plućima: disajni zvuk normalan, bazalno lako oslabljeno
disanje, ekspirijum nije produžen, perkutorni zvuk bazalno tmuo od
10-og rebra. Na ultrazvučnom pregledu srca došlo je do poboljšanja
ejekcione frakcije i poboljšanja dijastolne funkcije odnosno
komplijanse leve komore (odnos E/e' 7,5.). Dobijeni su
laboratorijski rezultati: Serumsko gvožđe <1μmol/l (normalno 11-31),
Feritin 19,2ng/mL (normalno 20-250 ng/mL).
Kontrola nakon dve nedelje (19.06.2025. godina): odlično
poboljšanje kliničkog stusa se održava, sada još 2 kg manje (ukupno
14 kg manje od početka lečenja) što je odličan efekat primenjene
terapije. Žali se na vrtoglavicu i nestabilnost koju povezuje sa
hipotenzijom, TA=90/55 mmHG i 80/50 mmHg, pa se prema tome redukuju
doze lekova koji deluju hipotenzivno: Furosemid tbl a 500mg 1/2 na
drugi dan, i tbl sacubitril-valsartan26/24mg 2 x 1/4. Zbog bolova u
podkolenicama dodaje se lek protiv venskih otoka Diosmin +
Hesperidin tbl a 1000mg 1x1.
Novi relevatni rezultati laboratorijskih analiza: Hgb 88g/l,
sedimentacija (Se) 55mm/h, urea 15,4 mmol/L, kreatinin 131μmol/L,
GFR 44,8mL/min/1,73m², kalijum 4,4mmol/L.
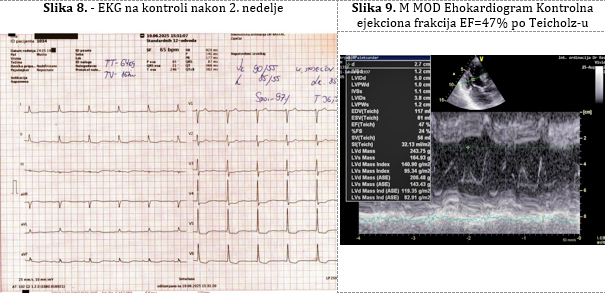
EKG Fibrilacija pretkomora sa apsolutom komora, fr 65/min, depresija
ST do 2mm i negativan T V4-V6, depresija ST do 0,5mm i negativan T u
D1, D2, aVL (Slika 8).
Rutinska kontrola posle 2 meseca 25.08.2025. godine. Pacijent
bez tegoba, ima još 2kg manje, noge ne otiču, nije više
hipotenzivan. Impresivan porast Hemoglobina na 128 g/L zbog terapije
gvožđem ali i zbog korigovanja hemodilucije. Normalizacija bubrežne
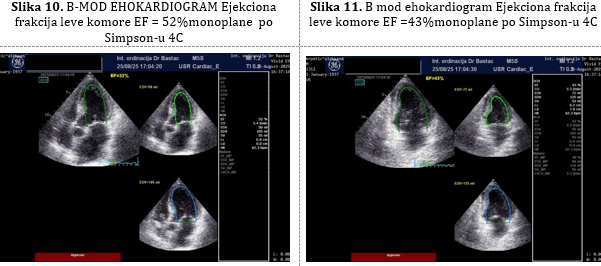
funcije GFR=64mL/min/1,73m². Ultrazvučnim pregledom srca (Slike 9,10
i 11) se registruje odličan porast ejekcione frakcije M mod EF 47%,
a po Simpsonu BIPLEJN EF je 46% uz redukciju dilatacije leve komore
(LK EDD=50mm, a ESD=40mm) i iščezavanje plućne hipertenzije (RVSP
=25 mmHg).
Urađena je dalja korekcija terapije održavanja i redukcija doze
Furosemid tbl a 500 mg 1/4 na drugi-treći dan.
KLINIČKI ISHOD:
Nakon intenzivne intravenske diuretske terapije i posle 3 dana
dnevne bolnice sa EKG monitoringom i praćenjem vitalnih parametara,
došlo je do značajnog kliničkog poboljšanja. Tada se obavlja
prelazak na peroralnu terapiju. Pacijent je izgubio ukupno 14 kg u
periodu od dve nedelje, sa iščezavanjem perifernih edema,
normalizacijom disajnog zvuka na plućima. Nastaje minimalizacija
pleuralnih efuzija, održava se dobra ejekciona frakcija oko 46 do 47
% i poboljšanje dijastolne funkcije na ehokardiografiji.
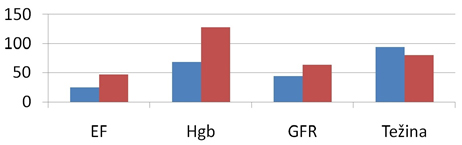
Laboratorijski parametri su pokazali postepeno poboljšanje renalne
funkcije (GFR sa 44 na 64 ml/min/1,73 m²) i značajan porast
hemoglobina nakon primene preparata gvožđa (Grafikon 1 i 2).
Grafikon 1. Trend promena kliničkih parametara
tokom terapije
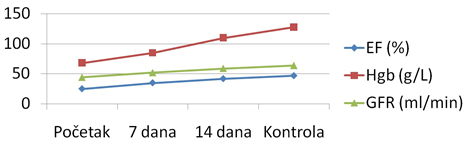
Grafikon 2. Uporedni prikaz pre i posle efekta terapije
DISKUSIJA
Anasarka predstavlja ekstremni oblik retencije tečnosti i marker
uznapredovale srčane insuficijencije sa lošom prognozom [5].
Diuretici ostaju osnov terapije kongestije, pri čemu intravenska
primena omogućava bržu i efikasniju dekongestiju [6,13,14]. Međutim,
njihova primena zahteva pažljivo praćenje zbog mogućeg pogoršanja
bubrežne funkcije [10,20], hipokaliemije i retko hipovolemije i
dehidratacije.
U ovom slučaju, poboljšanje renalne funkcije nakon terapije ukazuje
na reverzibilnost kardiorenalnog sindroma nakon uklanjanja
kongestije, što je već opisano u literaturi [10,11]. Savremene
studije pokazuju da rana primena SGLT2 inhibitora dovodi do brzog
kliničkog benefita i smanjenja hospitalizacija [17,21,22,23]. ARNI
terapija dodatno doprinosi poboljšanju remodelovanja miokarda i
smanjenju mortaliteta [16]. Savremene preporuke naglašavaju
simultanu ili ranu sekvencijalnu primenu pet osnovnih terapijskih
stubova, što je povezano sa najboljim ishodima [7,8,9,24].
Upravljanje kongestijom ostaje ključni terapijski cilj, a
individualizovana intravenska primena diuretika uz praćenje telesne
mase, diureze i renalne funkcije predstavlja osnov uspešnog lečenja
[14,15]. Anemija je čest komorbiditet kod srčane insuficijencije i
njena korekcija, posebno intravenskim preparatima gvožđa, poboljšava
simptome i kvalitet života [12,19]. Ovaj slučaj ukazuje na značaj
pravovremenog uvođenja intenzivne diuretske terapije, stalnog
praćenja diureze i laboratorijskih parametara, kao i
individualizovanog pristupa u zavisnosti od komorbiditeta. Ovaj
prikaz slučaja takođe pokazuje da je i ambulantni pristup, uz
adekvatan nadzor, moguć kod selektovanih bolesnika sa teškom
dekompenzovane hronične srčane insuficijencije, naizgle terminalne i
refrakterne na lečenje ali se ovakvi bolesnici najčešće leče u
hospitalnim uslovima [25].
ZAKLJUČAK
Dekompenzovana srčana slabost sa anasarkom predstavlja ozbiljno i
životno ugrožavajuće stanje koje zahteva agresivan, ali pažljivo
titriran individualni terapijski pristup. Diuretska terapija ostaje
osnovna mera u kontroli volumenskog opterećenja. Ovaj prikaz slučaja
ističe značaj individualizovane diuretske terapije u kombinaciji sa
savremenim farmakološkim strategijama kod pacijenata sa najtežim
oblikom dekompenzovane srčane insuficijencije i anasarkom.
Pravovremeno uvođenje velikih doza parenteralnih diuretika,
optimizacija osnovne terapije i korekcija pridruženih poremećaja
doveli su do značajnog kliničkog i laboratorijskog poboljšanja ovog
bolesnika.
Ovaj prikaz slučaj naglašava važnost davanja intravenske terapije sa
kontinuiranog EKG monitoringa u toku opservacija i praćenjem a i
prilagođavanja terapije prema diurezi, krvnom pritisku i frekvenci
pulsa, nalazu kalijuma i azotnih materija u serumu, krvnog pritiska
i saturacije krvi kiseonikom, radi postizanja optimalnog ishoda.
Posebno se naglašava značaj individualizacije terapije i
pravovremenog prepoznavanja refraktornosti na standardne mere
lečenja u sklopu hronične peroralne terapije. Kombinacija intenzivne
diuretske terapije i savremenih farmakoloških strategija omogućava
značajno kliničko poboljšanje čak i kod bolesnika sa uznapredovalom
bolešću, kao što je naš prikaz slučaja i koji je uspešno kardijalno
komopenzovan u ambulantnim uslovima dnevne bolnice.
LITERATURA
1. Savarese G, Lund LH. Global public health burden of heart
failure. Card Fail Rev. 2017;3(1):7–11.
2. Virani SS, Alonso A, Benjamin EJ, Bittencourt MS, Callaway CW,
Carson AP, et al. Heart disease and stroke statistics—2021 update: a
report from the American Heart Association. Circulation.
2021;143(8):e254–e743.
3. GBD 2022 Heart Failure Collaborators. Global, regional, and
national burden of heart failure, 1990–2022: a systematic analysis
for the Global Burden of Disease Study 2022. Lancet.
2022;400(10363):121–144.
4. Kasper DL, Fauci AS, Hauser SL, Longo DL, Jameson JL, Loscalzo J.
Harrison’s Principles of Internal Medicine. 19th ed. New York:
McGraw-Hill Education; 2015.
5. Eapen ZJ, Tang WHW, Felker GM, Hernandez AF. Defining true
clinical equipoise: cardiac cachexia versus anasarca in advanced
heart failure. Eur J Heart Fail. 2012;14(5):495–500.
6. Ponikowski P, Voors AA, Anker SD, Bueno H, Cleland JGF, Coats
AJS, et al. 2021 ESC Guidelines for the diagnosis and treatment of
acute and chronic heart failure. Eur Heart J. 2021;42(36):3599–3726.
7. Heidenreich PA, Bozkurt B, Aguilar D, Allen LA, Byun JJ, Colvin
MM, et al. 2023 ACC Expert Consensus Decision Pathway on Management
of Heart Failure with Reduced Ejection Fraction. J Am Coll Cardiol.
2023;81(18):1835–1878.
8. McDonagh TA, Metra M, Adamo M, Gardner RS, Baumbach A, Böhm M, et
al. 2023 Focused update of the 2021 ESC Guidelines for the diagnosis
and treatment of acute and chronic heart failure. Eur Heart J.
2023;44(37):3627–3739.
9. Greene SJ, Butler J, Fonarow GC. Simultaneous or rapid sequence
initiation of guideline-directed medical therapy for heart failure.
J Am Coll Cardiol. 2023;81(2):185–197
10. Damman K, Valente MAE, Voors AA, O’Connor CM, van Veldhuisen DJ,
Hillege HL. Renal impairment, worsening renal function, and outcome
in patients with heart failure: an updated meta-analysis. Eur Heart
J. 2014;35(7):455–469.
11. Ronco C, Haapio M, House AA, Anavekar N, Bellomo R. Cardiorenal
syndrome. J Am Coll Cardiol. 2008;52(19):1527–1539.
12. Ponikowski P, van Veldhuisen DJ, Comin-Colet J, Ertl G, Komajda
M, Mareev V, et al. Beneficial effects of long-term intravenous iron
therapy with ferric carboxymaltose in patients with symptomatic
heart failure and iron deficiency. Eur Heart J. 2015;36(11):657–668.
13. Felker GM, Lee KL, Bull DA, Redfield MM, Stevenson LW, Goldsmith
SR, et al. Diuretic strategies in patients with acute decompensated
heart failure. N Engl J Med. 2011;364(9):797–805.
14. Verbrugge FH, Mullens W, Tang WHW. Management of congestion in
heart failure: state-of-the-art review. Eur Heart J.
2023;44(24):2187–2200.
15. Damman K, Beusekamp JC, Boorsma EM, Swart HP, Smilde TDJ, Elvan
A, et al. Randomized, double-blind trial comparing high versus low
dose loop diuretics in acute heart failure. Eur J Heart Fail.
2023;25(3):456–466.
16. McMurray JJV, Packer M, Desai AS, Gong J, Lefkowitz MP, Rizkala
AR, et al. Angiotensin–neprilysin inhibition versus enalapril in
heart failure. N Engl J Med. 2014;371(11):993–1004.
17. McMurray JJV, Solomon SD, Inzucchi SE, Køber L, Kosiborod MN,
Martinez FA, et al. Dapagliflozin in patients with heart failure and
reduced ejection fraction. N Engl J Med. 2019;381(21):1995–2008.
18. Packer M, Anker SD, Butler J, Filippatos G, Pocock SJ, Carson P,
et al. Cardiovascular and renal outcomes with empagliflozin in heart
failure. N Engl J Med. 2020;383(15):1413–1424.
19. Anker SD, Comin Colet J, Filippatos G, Willenheimer R, Dickstein
K, Drexler H, et al. Ferric carboxymaltose in patients with heart
failure and iron deficiency. N Engl J Med. 2009;361(25):2436–2448.
20. Mullens W, Damman K, Harjola VP, Mebazaa A, Brunner-La Rocca HP,
Martens P, et al. The use of diuretics in heart failure with
congestion – a position statement from the Heart Failure Association
of the European Society of Cardiology. Eur J Heart Fail.
2019;21(2):137–155.
21. Butler J, Anker SD, Filippatos G, Khan MS, Ferreira JP, Pocock
SJ, et al. Empagliflozin and outcomes in patients with heart failure
with preserved, mildly reduced, and reduced ejection fraction:
pooled analysis of EMPEROR trials. Eur Heart J. 2023;44(5):449–460.
22. Vaduganathan M, Claggett BL, Jhund PS, Cunningham JW, Ferreira
JP, Zannad F, et al. Time to clinical benefit of dapagliflozin in
patients with heart failure with reduced ejection fraction: insights
from the DAPA-HF trial. Circulation. 2023;147(5):375–385.
23. Docherty KF, Jhund PS, Inzucchi SE, Køber L, Kosiborod MN,
Martinez FA, et al. Effects of dapagliflozin across the spectrum of
ejection fraction in heart failure. Nat Med. 2024;30(1):123–131.
24. Maddox TM, Januzzi JL Jr, Allen LA, Breathett K, Butler J, Davis
LL, et al. 2024 ACC Expert Consensus Decision Pathway for
optimization of heart failure treatment. J Am Coll Cardiol.
2024;83(9):1056–1098.
25. Ambrosy AP, Fonarow GC, Butler J, Chioncel O, Greene SJ,
Vaduganathan M, et al. The global health and economic burden of
hospitalizations for heart failure: lessons learned from
hospitalized heart failure registries. J Am Coll Cardiol.
2014;63(12):1123–1133.
26. Zannad F, Ferreira JP, Pocock SJ, Anker SD, Butler J, Filippatos
G, et al. SGLT2 inhibitors in patients with heart failure with
reduced ejection fraction: a meta-analysis of the EMPEROR-Reduced
and DAPA-HF trials. Lancet. 2020;396(10244):819–829.
27. Anker SD, Butler J, Filippatos G, Ferreira JP, Bocchi E, Böhm M,
et al. Semaglutide in patients with heart failure with preserved
ejection fraction and obesity (STEP-HFpEF trial). N Engl J Med.
2023;389(12):1069–1084.
|
|
|
|









