 |
Glasilo Podružnice Srpskog lekarskog društva Zaječar
Godina 2004 Volumen 29 Broj
3 |
|
|
|
|
[ Home ] [ Gore/Up ][ <<< ] [ >>> ]
|
|
| |
UDK: 615.222.06:616.44-073 |
ISSN 0350-2899,
29(2004) 3 p.157-163 |
|
| |
Originalni radVrednosni in vivo tireoidnih testova - scintigrafije
štitaste žlezde Tehnecijum Pertehnetatom, testa akumulacije Tehnecijum
Pertehnetata (TcU) i testa radiojodne fiksacije (RAIU) kod pacijenata na
terapiji Amiodaronom -
pokušaj vizualizacije štitaste žlezde sa 99mTC-MIBI
Željka Aleksić, Aleksandar Aleksić
Zdravstveni centar Zaječar, Služba za nuklearnu medicinu, Zaječar |
|
| |
|
|
| |
Sažetak:
Amiodaron (AMD) je potentni antiaritmik bogat jodom. Pacijenti na terapiji
ovim lekom unose prekomerne količine joda. Kod 42 pacijenta, 20
eutiroidnih na terapiji sa AMD, i 22 sa supkliničkim ili kliničkim
tireoidnim disfunkcijama (TD) izazvanim amiodaronom, uradili smo jedan ili
više in vivo tireoidnih testova – statičku scintigrafiju štitaste žlezde (ŠŽ)
tehnecijum pertehnetatom, test akumulacije tehnecijum pertehnetata (TcU)
ili test radiojodne fiksacije (RAIU). Kod svih, sem dva eutireodna
pacijenta, štitasta žlezda je bila “blokirana”. Preostala dva pacijenta
imala su funkcionalne noduse u ŠŽ, koji su se dobro prikazali bez obzira
na opterećenje jodom. Amiodaronom indukovane tireotoksikoze (AIT)
pokazivale su ili očuvano ili pojačano vezivanje, AIT tip 1, ili sniženo
vezivanje obeleživača, AIT tip 2. Kod jednog pacijenta sa amiodaronom indukovanim
hipotiroidizmom (AIH) i jednog sa supkliničkim hipotireoidizmom nađena je
normalna vrednost RAIU za 3h. Kod pacijenata sa supkliničkim
hipertiroidizmom bilo je različitih nalaza. Kod 7 pacijenata urađena je i
scintigrafija ŠŽ sa 99mTc-MIBI. Vizualizacije ŠŽ sa 99mTc-MIBI
bila je dobra samo u jednog, supklinički hipotireodnog pacijenta.
Scintigrafija tehnecijum pertehnetatom, TcU i RAIU mogu biti korisni in
vivo testovi za diferencijaciju AIT tip 1 i AIT tip 2.
Ključne reči: amiodaron, scintigrafija štitaste žlezde tehnecijum
pertehnetatom, radiojodna fiksacija, test akumulacije pertehnetata,
scintigrafija štitaste žlezde sa 99mTc-MIBI
Napomena: sažetak na engleskom jeziku
Note: summary in English |
|
| |
|
|
| |
|
|
| |
UVOD
Pacijenti koji se zbog refrakternih aritmija leče amiodaronoma (AMD),
antiaritmikom bogatim jodom, izloženi su hronično povećanom oralnom unosu
joda.
Amiodaron je derivat benzofurana koji sadrži dva atoma joda po molekulu,
odnosno jod čini 37,2% težine molekula. To znači da u svakoj kapsuli od
200 mg amiodarona ima oko 75 mg organskog joda. Nakon oralne primene, on
se nepotpuno i sporo apsorbuje iz GIT-a. Sisitemska biološka raspoloživost
pokazuje velike varijacije i kreće se od 22-80%. Između 8% i 17% joda iz
AMD oslobađa se u cirkulaciji kao neorganski jod, što čini 3 mg
neorganskog joda na 100 mg AMD svakog dana.
Jodid se u tireocite transportuje nasuprot električnog i hemijskog
gradijenta. Sposobnost tireocita da koncentrišu jodid u fiziološkim
uslovima je znatna. Koncentracija jodida u štitastoj žlezdi (ŠŽ) je 20-40
puta veća od koncentracije u plazmi. Jodid koji se dopremi u tireocit,
može biti oksidisan i organifikovan ili slobodno difunduje nazad u
ekstraćelijsku tečnost. 1-4
Tireoidni transport jodida ispunjava sve kriterijume aktivnog transporta.
Aktivni transport jodida u ŠŽ posredovan je Na+-I-
simporterom (NIS), intrinzičnim membranskim proteinom. Monovalentni anjoni
slične veličine, oblika i istog električnog naboja kao jodid takođe se
mogu koncentrisati u ŠŽ. Anjoni ClO3-, TcO4-, SCN-,
SeCN-, NO3-, Br-, BF4-, IO4-,
BrO3- su kompetitivni inhibitori transporta jodida u ŠŽ. 5 |
|
| |
|
|
| |
|
|
| |
CILJ RADA
Cilj nam je bio da u populaciji naših pacijenata na terapiji
amiodaronom, sa ili bez tireoidne disfunkcije(TD) indukovane amiodaronom,
ispitamo vrednosti in vivo testova (scintigrafije ŠŽ, fiksacije radiojoda
– RAIU i akumulacije pertehnetata – TcU). Osim toga, kod jednog broja
pacijenata, pokušali smo vizualizaciju ŠŽ sa 99mTc-MIBI (metoksi-izobutil-izonitril),
čija je akumulacija u ŠŽ nezavisna od TSH I joda. |
|
| |
|
|
| |
|
|
| |
PACIJENTI I METODE
Kod ukupno 42 pacijenta, prosečne starosti 52.95±11.13
godina (29-71) na terapiji AMD-om od 20.44±25.01
meseci, medijana 12 (1-120) urađen je neki od in vivo tiroidnih testova.
Urađeno je 25 statičkih scintigrafija ŠŽ tehnecijum-pertehnetatom, 18
testova akumulacije tehnecijum-pertehnetata, 12 radiojodnih fiksacija i 7
scintigrafija ŠŽ pomoću 99mTc-MIBI. Svim pacijentima urađeni su
i biohemijski testovi tiroidne funkcije, kao i klinička procena tiroidnog
statusa.
Nivo ukupnih tireoidnih hormona, TT4 i TT3 određivan je RIA metodom (RIA
TT4 i RIA TT3 Institut za nuklearne nauke "Vinča"), sa opsegom normalnih
vrednosti 51.5-160 nmol/L za TT4 i 1.33-3.1 nmol/L za TT3. Nivo slobodnih
frakcija tireoidnih hormona određivan je metodom DELFIA (DELFIA FT4 i
DELFIA FT3 Wallac Oy, Turku, Finland). Opseg normalnih vrednosti slobodnih
frakcija tireoidnih hormona su 9.25-25 pmol/L za FT4 i 3.5-9.0 pmol/L za
FT3. TSH je meren ultrasenzitivnom DELFIA metodom (DELFIA hTSH Ultra
Wallac Oy, Turku, Finland) sa referentnim opsegom od 0.1-4 mU/L.
Merenje fiksacije radiojoda (131I) vršeno je nakon 3 i/ili 24
sata od peroralne primene oko 10 μCi (0.37 MBq) Na131I
scintilacionom sondom sa kristalom NaI (Tl), 3x3 inča i divergentnim
kolimatorom pravolinijskog skenera Pho/Dot Scanner, Nuclear Chicago. Opseg
referentnih vrednosti fikasacije radiojoda je 8-20% za 3 sata i 20-45% za
24 sata. Kratki test fiksacije 99mTcO4- (TcU)
izvođen je na gama kameri PHO/GAMMA IV Searle Radiographics sa LPP
kolimatorom, tako što se nakon intravenske primene oko 1.5-2 μCi (50-80
MBq) tehnecijum pertehnetata, kontinuirano merila radioaktivnost nad ŠŽ u
toku 5 minuta. Korišćen je program HISTO i iz regiona od interesa nad ŠŽ
dobija se kriva aktivnost/vreme, a TcU se izračunava iz odnosa priraštaja
(slope) aktivnosti izraženog u impulsima u sekundi i aktivnosti nad
graničnikom A koji deli završetak "vaskularne" faze od početka rane
akumulacije. Priraštaj se meri u linearnom delu krive omeđenom graničnikom
A i graničnikom B, koji se postavlja na kraj linearnog priraštaja
(najčešće oko 3. minuta). Izračunavanje se vrši množenjem proizvoda
priraštaja i aktivnosti nad A sa 1000. Vrednosti iznad 5 su povišene, a
ispod 1 snižene 6. Scintigrafija ŠŽ rađena je nakon 15-20
minuta po intravenskoj primeni oko 1 mCi (37MBq) tehnecijum-pertehnetata (99mTcO4-),
ili 6-8 mCi (222-296 MBq) 99mTc - MIBI (sestamibi) na gama
kameri Simens Diacam. Svi in vivo i in vitro testovi rađeni su u
nuklearnomedicinskoj laboratoriji Zdravstvenog centra u Zaječaru. |
|
| |
|
|
| |
|
|
| |
REZULTATI
Dobijeni rezultati prikazani su u tabeli 1. i na slikama 1, 2 i 3. Statička scintigrafija sa tehnecijum pertehnetatom urađena je kod 12
eutiroidnih (EU) pacijenata na terapiji sa AMD Kod njih 10 bilo je odsutno
vezivanje obeleživača u ŠŽ – »blokirana« ŠŽ. Kod istih pacijenata indeks
TcU bio je nizak, ispod 1. Kod preostala 2 EU pacijenta scintigrafijom su
se prikazali funkcioni nodusi.
Kod jednog pacijenta sa amiodaronom indukovanim hipotireoidizmom (AIH) kod
kog je rađena scintigrafija pertehnetatom dobijen je normalan scintigram
ŠŽ.
Kod 7 pacijenata sa AIT urađena je statička scintigrafija pertehnetatom.
Kod 2 pacijenta otkriveni su toksični adenomi, a kod jednog difuzna
toksična struma, a nalazi su imali dijagnostički značaj u smisli AIT tip
1. Kod preostala 4 pacijenta sa AIT, scintigrafija i TcU pokazivali su
“blokiranu” ŠŽ – AIT tip 2.
Od 5 pacijenata sa supkliničkim hipertiroidizmom, sa suprimiranim uTSH I
normalnim nivoom tireoidnih hormona, kod 3 je nađena »blokirana« ŠŽ, a kod
2 dobijen normalan scintigram ŠŽ.
RAIU je urađen kod 12 pacijenata. Od 5 EU pacijenata, kod svih sem jednog
kod kog je bila normalna, vrednost testa je bila snižena. Kod 5 pacijenata
sa AIT, nivo RAIU je takođe bio snižen, AIT tip 2. Kod jednog pacijenta sa
AIH i jednog sa supkliničkim hipotireoidizmom fiksacija radiojoda za 3
sata bila je normalna (9% i 10% redom).
99mTc-MIBI scan ŠŽ rađen je kod 7 pacijenata. - kod 3 EU
pacijenta, 2 sa AIT, 1 supklinički hipotireoidnog i 1 supklnički
hipertireoidnog.
Dobra vizualizacija i normalne morfološke karatkteristike ŠŽ dobijeni samo
kod 1 pacijenta koji je supklinički hipotireodan.
Starost pacijenata, pol i dužina terapije sa AMD nisu imali značaj za
dobijene rezultate in vivo testova. |
|
| |
|
|
| |
| PACIJENT |
POL |
STAROST |
SCINTIGRAFIJA |
TcU |
RAIU |
VRSTA DISFUNKCIJE |
AMD (m) |
| 290/ 8 |
Z |
68 |
/ |
/ |
9 |
A I H |
48 |
| 444/ 8 |
M |
53 |
NORMALNA ŠŽ |
/ |
/ |
A I H |
3 |
| 259/ 4 |
Z |
37 |
TOKSIČNI ADENOM |
/ |
/ |
A I T 1 |
60 |
| 476/ 4 |
M |
61 |
TOKSIČNI ADENOM |
/ |
/ |
A I T 1 |
12 |
| 168 |
Z |
44 |
DIFFUSA TOXICA |
/ |
/ |
A I T 1 |
48 |
| 1073/ 3 |
M |
48 |
BLOKIRANA ŠŽ |
<1 |
/ |
A I T 2 |
20 |
| 1111/ 3 |
Z |
48 |
/ |
/ |
/<1 |
A I T 2 |
24 |
| 1324/ 3 |
M |
50 |
/ |
/ |
6 |
A I T 2 |
36 |
| 36 |
M |
63 |
/ |
/ |
/2 |
A I T 2 |
28 |
| 444/ 3 |
M |
40 |
BLOKIRANA ŠŽ |
<1/ |
/ |
A I T 2 |
24 |
| 478/ 3 |
Z |
31 |
BLOKIRANA ŠŽ |
<1 |
/ |
A I T 2 |
6 |
| 71 |
M |
56 |
MIBI-NORMALNA ŠŽ |
/ |
10/3.5 |
S K H I P O |
18 |
| 80 |
M |
59 |
MIBI-BLOKIRANA ŠŽ |
<1 |
/1.5 |
A I T 2 |
30 |
| 98 |
M |
51 |
MIBI-NORMALNA ŠŽ |
/ |
/ |
A I T 2 |
12 |
| 205 |
Z |
59 |
BLOKIRANA ŠŽ |
<1 |
/ |
A I T 2 |
24 |
| 142 |
M |
48 |
/ |
/ |
3 |
A I T 2 |
24 |
| 206 |
Z |
65 |
PN-FUNKCIJSKI |
/ |
/ |
E U |
36 |
| 101 |
Z |
66 |
/ |
/ |
7 |
E U |
60 |
| 1138/ 3 |
Z |
71 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
60 |
| 13 |
Z |
39 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
1 |
| 14 |
M |
51 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
4 |
| 16 |
Z |
46 |
BLOKIRANA ŠŽ |
1 |
/ |
E U |
1 |
| 17 |
M |
45 |
/ |
/ |
4/3 |
E U |
36 |
| 21 |
Z |
54 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
3 |
| 23 |
M |
60 |
/ |
/ |
24/34 |
E U |
3 |
| 252/3 |
Z |
45 |
TOPLI MIKRONODUS |
/ |
/ |
E U |
2 |
| 33 |
Z |
29 |
/ |
/ |
3/6 |
E U |
6 |
| 34 |
Z |
63 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
16 |
| 35 |
M |
35 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
3 |
| 40 |
Z |
62 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
36 |
| 42 |
Z |
44 |
/ |
/ |
/2 |
E U |
12 |
| 63 |
M |
63 |
MIBI-BLOKIRANA ŠŽ |
/ |
/ |
E U |
8 |
| 67 |
Z |
66 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
2 |
| 76 |
M |
48 |
BLOKIRANA ŠŽ |
<1 |
/ |
E U |
120 |
| 93 |
M |
64 |
MIBI-BLOKIRANA ŠŽ |
/ |
/ |
E U |
2 |
| 95 |
M |
63 |
MIBI-BLOKIRANA ŠŽ |
/ |
/ |
E U |
6 |
| 194 |
Z |
45 |
NORMALNA ŠŽ |
/ |
/ |
S K H I P E R |
10 |
| 193 |
M |
70 |
BLOKIRANA ŠŽ |
<1 |
/ |
S K H I P E R |
4 |
| 176 |
M |
69 |
BLOKIRANA ŠŽ |
<1 |
/ |
S K H I P E R |
12 |
| 166 |
Z |
56 |
BLOKIRANA ŠŽ |
<1 |
/ |
S K H I P E R |
0.3 |
| 66 |
Z |
48 |
NORMALNA ŠŽ |
/ |
/ |
S K H I P E R |
12 |
| 94 |
Z |
41 |
MIBI-BLOKIRANA ŠŽ |
/ |
/ |
S K H I P E R |
10 |
|
|
| |
|
|
| |
|
|
| |
DISKUSIJA
Akumulaciju jodida u ŠŽ stimuliše TSH, glavni regulator sveukupne
tireoidne funkcije. Drugi glavni faktor regulisanja aktivnosti NIS u ŠŽ je
sam jod. Transport joda je inhibisan viškom joda i povećan i stimulisan
jodnim deficitom nezavisno od TSH 7.
Uticaj joda na sintezu TH zavisi od količine joda i trajanja primene joda.
Kada se primeni akutno u maloj ili umerenoj količini, jod izaziva male
promene u obimu organifikacije i praktično ne utiče na procenat fiksacije
radiojoda.
Veće akutne doze joda izazivaju dvofazni odgovor u veličini organifikacije.
Najpre nastaje porast, a zatim smanjenje organskog vezivanja joda. Wolff i
Chaikoff su 1948. godine objavili da je organsko vezivanje jodida u ŠŽ
pacova bilo blokirano kada je nivo jodida u plazmi dostigao kritično visok
prag. Ovaj fenomen poznat je kao akutni Wolff-Chaikoff-ljev efekat. Oko
dva dana kasnije, u prisustvu neprekidno visokih koncentracija jodida u
plazmi, dolazi do "bega" od, ili adaptacije na akutni efekat koji je
primećen, tako da se ponovno uspostavlja organifikacija i normalna
biosinteza TH. Mehanizam koji je odgovoran za akutni Wolff-Chaikoff-ljev
efekat još nije rasvetljen. Smatra se da je adaptacija na akutni Wolff-Chaikoff-ljev
efekat posledica smanjenja transporta jodida u tireocit, što dovodi do
dovoljno niske intraclularne koncentracije jodida, koja uklanja inhibiciju
organifikacije. Smanjenje transporta jodida koje omogućava adaptaciju,
smanjuje brzinu tireoidnog klirensa jodida i fiksaciju radiojoda. Uprkos
tome, količina joda koja je akumulirana i organifikovana veća je nego
normalno, mada brzina sekrecije T4 nije povećana. Stoga, tokom produžene
primene joda ŠŽ stvara i oslobađa nekalorigene oblike joda. Verovatno je
najveći deo joda koji se gubi iz ŠŽ na ovaj način u obliku jodida - kod
zdravih osoba količina curenja joda je u direktnoj srazmeri sa unosom joda
8.
Nađeno je da pacijenti koji uzimaju 300 mg AMD na dan imaju 40 puta veću
urinarnu ekskreciju neorganskog joda i četrdeset puta veću koncentraciju
neorganskog joda u plazmi, dok je tireoidni uptake smanjen za 75%, a
tireoidni klirens jodida smanjen sa 6 ml/min na 0.5 ml/min 1-4.
Saller i sar. pored visokog povećanja serumske koncentracije neorganskog
joda kod pacijenata na terapiji sa AMD, ne nalaze da su one u korelaciji
sa dnevnom dozom AMD, niti sa serumskom nivoom AMD 9.
Brojni inhibitorni mehanizmi, kao što je već pomenuto, štite organizam od
prekomernog stvaranja tireoidnih hormona usled opterećenja egzogenim
jodom. Jod inhibiše sopstvenu organifikaciju (Wolff-Chaikoff-ljev efekat)
i smanjuje tireoidni klirens joda. Međutim, kada se uzme u obzir apsolutno
preuzimanje joda, uočeno je da nakon šest nedelja lečenja sa AMD dolazi do
trostrukog porasta ove vrednosti, nakon čega dolazi do njegovog
progresivnog pada, ali on i dalje ostaje viši od normalnog 4.
Pretpostavljeni mehanizam nastanka amiodaronom indukovanog hipotiroidizma
(AIH) je perzistentna blokada organifikacije joda izazvana viškom
joda; nakon akutne inhibicije sinteze - akutni Wolff-Chaikoff-ljev efekat,
dolazi do ponovnog uspostavljanja prethodnog nivoa sinteze tiroidnih
hormona (TH) - fenomen bega, što je posledica autoregulatornog mehanizma
smanjenog transporta joda u tireocite. Kod pacijenata koji razvijaju
hipotiroidizam ne dolazi do fenomena bega i sinteza hormona ostaje trajno
inhibisana hroničnim unosom viška joda.
Dokaz za ovakvo događanje kod AIH je:
- očuvana rana fiksacija 131I i 99mTcO4-
u ŠŽ ,
- pozitivan perhloratski test i
- nizak intratireoidni sadržaj joda, što je odlika i klasičnog jodom
indukovanog hipotiroidizma (IIH).
Postoje dva tipa amiodaronom indukovane tirotoksikoze (AIT). AIT tip
l se javlja kod pacijenata sa prethodnom tireoidnom bolešću kao što su
polinodozna, nodozna ili difuzna struma. Supklinički autonomno tkivo ŠŽ
povećava sintezu hormona u odgovoru na hronično opterećenje jodom iz AMD.
Prethodan deficit joda stvara uslove za razvoj autonomnih tireoidnih
nodusa, a sledstvena primena joda vodi ka autonomnom prekomernom stvaranju
TH od strane ovih nodusa - fenomen poznat kao Jod-Basedow (jodom
indukovana tireotoksikoza - IIT). Unger i sar. ovu hipotezu o nastanku AIT
nazivaju metabolička hipoteza
Kod pacijenata sa Graves-ovom bolešću autonomija ŠŽ kao posledica
autoimune stimulacije objašnjava jodom indukovanu tireotoksikozu. Odlike
tipa 1 AIT su:
- normalna ili povišena vrednost fiksacije radiojoda,
- normalna ili lako povišena vrednost serumskog IL-6 i
- karakterističan ultrazvučni nalaz sa nodoznim ili difuzno
hipoehogenim obrascem.
AIT tip 2 se javlja kao posledica direktnog citotoksičnog efekta
amiodarona kod pacijenata sa normalnom ŠŽ. AMD kod ovih pacijenata izaziva
subakutni destruktivni tiroidit sa sledstvenim oslobađanjem već stvorenih
hormona u cirkulaciju. Takođe, iz oštećenih tireoidnih ćelija se verovatno
oslobađa i IL-6:
- fiksacija radiojoda je niska ili odsutna,
- serumski IL-6 je izrazito povišen,
- ultrazvučni nalaz ŠŽ je normalan.
Uprkos velikom unosu joda, fiksacija 131I/99mTcO4-
je detektabilna kod pacijenata sa AIH bez obzira na prisustvo ili odsustvo
prethodne bolesti ŠŽ. Prema istraživanju Ungera i sar., RAIU, kod
pacijenata sa AIH dostiže maksimum nakon 2 sata i ostaje nepromenjen do 24
sata. Rana fiksacija (do 7 sati) je normalna zbog izostanka inhibicije
mehanizma za koncentraciju joda, a niska fiksacija za 24 h se objašnjava
smanjenom organifikacijom joda 10. Nalazi RAIU i scintigrafije
ŠŽ kod naša dva pacijenta sa AIH takođe pokazuju očuvanu ranu akumulaciju
obeleživača, što je slučaj i sa jednim supklinički hipotireoidnim
pacijentom.
Suprotno ovome, kod pacijenata sa AIT, fiksacija 131I je
normalna ili čak povećana kod onih sa prethodnom bolešću ŠŽ, dok je vrlo
niska kod onih sa normalnom ŠŽ 11. Scintigrafija može ukazati
na prisustvo regionalne autonomije. Tri naša pacijenta sa AIT imala su
očuvanu i pojačanu akumulaciju pertehnetata – dva pacijenta sa toksičnim
adenomom i pacijentkinja sa difuznom toksičnom strumom (M.Graves), prema
čemu su svrstani u AIT tip 1, i uspešno lečeni radiojodom, pacijenti sa
toksičnim adenomom, i medikamentnom tireosupresivnom terapijim,
pacijentkinja sa Graves-ovom bolešću.. Preostali pacijenti sa AIT, njih
10, koji su imali “blokiranu” ŠŽ, u skladu sa kliničkim ispoljavanjem,
svrstani su u AIT tip 2, koja se leči glukokortikoidima.
Fiksacija radiojoda je veoma niska kod eutireoidnih pacijenata na terapiji
sa AMD, bez obzira na prisustvo ili odsustvo strume.12-16 Od 17
naših eutireoidnih pacijenata kojima je in vivo testirana ŠŽ , svi sem
troje njih imalo je »blokiranu« ŠŽ. Kod dvoje su prikazani funkcionalni
adenom, a jedan pacijent imao je normalan RAIU. Dužina terapije AMD nije
bila presudna za ovaj nalaz.
Varijacije u nalazima kod supklinički hipertireoidnih i nekih eutireodnih
pacijenata možda bi se mogla objasniti velikim razlikama u biološkoj
raspoloživosti AMD.
Ćelijski uptake 99mTc-MIBI-ja, katjonskog kompleksa, posledica
je kombinacije njegovog naelektrisanja i lipofilnosti sa visokim
negativnim membranskim potencijalom endomitohondrijalno, što uslovljava
njegovu retenciju u mitohondrijama, koja nije organ specifična. Obeleživač
se ne zadržava u ireverzibilno ishemičnim ćelijama, što ga čini osetljivim
markerom ćelijske vijabilnosti. 99mTc-MIBI obezbeđuje
kvalitetne scintigrafije štitaste žlezde (ŠŽ). Za razliku od joda ili
pertehnetata, izgleda da TSH, kao i višak joda, ne utiču na akumulaciju
MIBI-ja u ŠŽ.17
Mogući uzroci slabe vizualizacije ŠŽ sa 99mTc-MIBI kod naših
pacijenata mogli bi biti sledeći:
- Tehnički - radiofarmak, parametri akvizicije (malo verovatno)
- Patološki proces u ŠŽ – difuzna destrukacija tirocita (posledica
citotoksičnosti AMD i/ili samog joda) sa ili bez kliničke i/ili
biohemijske tiroidne disfunkcije
- Opterećenje jodom (ne bi trebalo da utiče na akumulaciju MIBI u ŠŽ)
- Za sada nepoznati razlozi
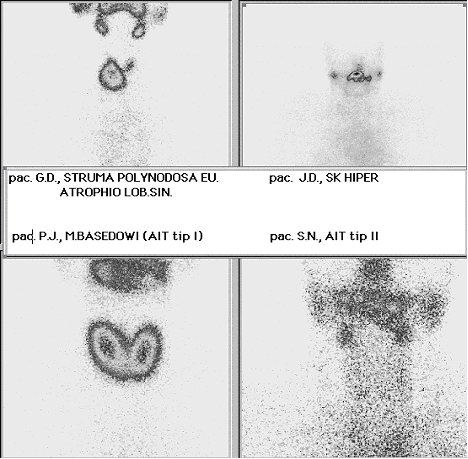
Slika 1. Scintigrafija štitaste žlezde tehnecijum pertehnetatom
kod pacijenata na terapiji sa AMD.
Slika levo gore – funkcionalni adenomi desnog režnja;
slika desno gore i desno dole – “blokirana” ŠŽ;
Levo dole – difuzna toksična struma.
|
|
| |
 |
 |
|
| |
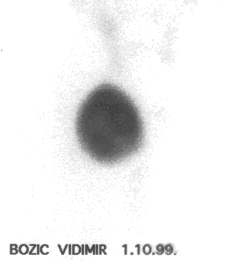
Slika 2.
Scintigrafija štitaste žlezde tehnecijum-pertehnetatom. Dekompenzovani
toksični adenom kod pacijenta (476/4) na hroničnoj terapiji amiodaronom.
Uočljiv očuvan uptake obeleživača uprkos hroničnog opterećenja jodom. |
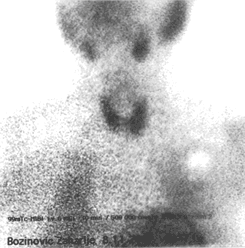
Slika 3.
Scintigrafija ŠŽ sa 99mTc-MIBI kod pacijenta (71) starog 56
godina, na AMD terapiji 22 meseca, SK HIPOtiroidnog. Akvizicija rađena 30
minuta nakon i.v. aplikacije 6 mCi 99mTcMIBI |
|
| |
|
|
| |
|
|
| |
ZAKLJUČAK
In vivo tireoidni testovi, scintigrafija ŠŽ tehnecijum pertehnetatpm,
test akumulacije pertehnetata i test radiojodne fiksacije mogu imati
klinički značaj u kombinaciji sa ostalim in vitro i in vivo testovima u
diferencijalnoj dijagnozi tipova amiodaronom indukovane tireotoksikoze,
čije je razlikovanje bitno za izbor adekvatne terapije. |
|
| |
|
|
| |
|
|
| |
LITERATURA
- Unger J, Lambert M.. Jonckheer M.H, et al. Amiodarone and thyroid:
pharmacological, toxic and therapeutic effects. J Intern Med 1993; 233:
435-443
- Nademanee K, Piwonka R, Singh B, et al. Amiodarone and thyroid. Prog
Cardiovas Disease 1989; 31(6): 427-437
- Davies PH, Franklyn JA. The effects of drugs on tests of thyroid
function. Eur J Clin Pharnacol, 1991; 40: 439-451
- Rao HR, Cready RV, Spathis SG. Iodine kinetic studies during
amiodarone treatment. J Clin Endocrinol Metab. 1986; 62: 563-567
- Dohan O, De la Vieja A, Carrasco N. Molecular study of the sodium-iodide
symporter (NIS): A new field in thyroidology. Trends in Endocrinology
and Metabolisam 2000; 11: 99-105
- Paunković N, Paunković J, Pavlovic O. Procena autoimune stimulacije
štitaste žlezde testom akumulacije 99mTc-pertehnetata. Radiologia
Iugoslavica 1991; 25: 43-46
- Utiger RD and Burrow NG. Thyroid disease. In: Endocrinology and
metabolism. Graw Ed. Hill inc, 1995. 433-553.
- Larsen RP, Sidney IH. The thyroid gland. In: Williams textbook of
endocrinology. Wilson JD Ed. Saunders Co., Philadelphia, 1992. 360-378.
- Saller B, Fink H, Mann K. Kinetics of acute and chronic iodine
excess. Exp Clin Endocrinol Diabetes 1998; 106 suppl 3: 34-38
- Unger J, Surmont DW, Sarot J et al. 24 h-kinetics of iodide uptake
in amiodarone induced hypothyroidism. Thyroidology 1989; 1 (2): 101-2
- Martino E, Aghini-Lombardi F, Lippi F et al. Twenty-four hour
radioactive iodine uptake in 35 patients with amiodarone associated
thyrotoxicosis. J Nucl Med 1985; 26 (12): 1402-7
- Wiersinga W, Touber J, Trip M. et al. Uninhibited thyroidal uptake
of tadioiodine despite iodine excess in amiodarone-induced
hypothyroidism. J Clin Endocrinol Metab 1986; 63: 485-491
- Fragu P, Schlumberger M, Davy JM et al. Effects of amiodarone
therapy on thyroid iodine content as measured by X-ray fluorescence. J
Clin Endocrinol Metab, 1988; 66: 762-769
- Figge H, Figge J. The effects of amiodarone on thyroid hormone
function: a review of the physiology and clinical manifestations. J Clin
Pharmacol 1990; 30: 588-595
- Martino E, Bartalena L, Mariotti S et al. Radioactive iodine thyroid
uptake in patients with amiodarone-iodine-induced thyroid dysfunction.
Acta Endocrinol (Copenh) 1988; 119: 167-173
- Ross DS. Syndromes of thyrotoxicosis with low radioactive iodine
uptake. Endocrinol Metab Clin North Am 1998; 27(1): 169-85
- Helal BO, Delbot T, Rolland C et al. Tc-99m-sestamibi imaging of
suppressed thyroid tissue in hyperthyroid patients. Endocrine Journal
2000; 47 (suppl.): 178
|
|
| |
|
|
| |
Adresa autora:
Željka Aleksić
Zdravstveni centar Zaječar, Služba za nuklearnu medicinu
Rasadnička B.B, 19000 Zaječar,
e-mail: lukaal@ptt.yu
Rad primljen 10. 08. 2004.
Rad prihvaćen 26. 08. 2004.
Elektronska verzija objavljena 18. 09. 2004. |
|
| |
|
|
|
|
|
|
|
|
|
[ Home ] [ Gore/Up ][ <<< ] [ >>> ]
|
|
|
Infotrend
Crea(c)tive Design |
|
|
|
Revised:
20 May 2009
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|



