|
||||||||||||||||||||||||||||||||||||
| [ Sadržaj
] [ Indeks autora ]
|
||||||||||||||||||||||||||||||||||||
| UDK 616.12-008.331.1 616.61-036.1-06 COBISS.SR-ID 78654473 |
strana 84. |
|||||||||||||||||||||||||||||||||||
|
Pregledni članak Novi pristup sagledavanju hipertenzije u hroničnoj bubrežnoj bolesti kroz prizmu poslednjeg KDIGO vodiča 2021
Biserka Tirmenštajn Janković (1), Dušan Bastać (2) |
||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||
| Preuzmite rad u pdf formatu | Sažetak:
Hipertenzija udružena sa hroničnom bubrežnom bolešću (HBB) praćena
je visokim rizikom kardiovaskularnih bolesti (KVB) koje su najčešći
uzrok morbiditeta i mortaliteta kod bolesnika sa HBB. Kontrola
hipertenzije je važna prevashodno zbog smanjenja rizika od KVB i
ukupnog mortaliteta kod bolesnika sa HBB. Nove KDIGO (Kidney
Disease: Improving Global Outcomes) smernice za dijagnostiku i
terapiju krvnog pritiska (KP) u HBB publikovane su 2021. godine i
predstavljaju ažuriranu varijantu originalnih smernica iz 2012.
godine. One obuhvataju sve teme sadržane u originalnom uputstvu, kao
što su optimalni ciljevi krvnog pritiska, intervencije u načinu
života, izbor antihipertenzivnih lekova i specifično lečenje kod
bolesnika sa transplantiranim bubregom i dece. Neki aspekti opšteg i
kardiovaskularnog zdravlja, kao što su kontrola lipida i pušenje su
isključeni. Pored toga, ove smernice uvode poglavlje posvećeno
pravilnom merenju KP, pošto su sva velika randomizovana ispitivanja
na osnovu kojih su izvedeni dokazi i preporuke iz ovog vodiča
koristila standardizovane protokole pripreme i merenja KP kojih su
se pridržavali bolesnici i kliničari. Ključna preporuka KDIGO
smernica odnosi se na ciljni sistolni krvni pritisak niži od 120
mmHg kod većine odraslih osoba sa HBB, pod uslovom da se koristi
metoda standardizovanog merenja KP u ordinaciji. Uprkos datim
preporukama za sniženje ciljnog KP, nedovoljna količina dokaza,
naročito kod bolesnika sa dijabetesom i uznapredovalom HBB, sugeriše
neophodnost induvidualizacije ciljeva u skladu sa karakteristikama,
tolerancijom i preferencijama svakog bolesnika. Potrebne su veće
randomizovane kontrolisane studije koje bi ispitivale efekte ciljnih
vrednosti KP na glavne neželjene događaje i mortalitet kod bolesnika
sa HBB, a posebno u subpopulacijama koje nisu bile adekvatno
zastupljene u prethodnim ispitivanjima. Ključne reči: hronična bubrežna bolest, hipertenzija, KDIGO, merenje krvnog pritiska, ciljni krvni pritisak, način života, fizička aktivnost, antihipertenzivni lekovi. |
|||||||||||||||||||||||||||||||||||
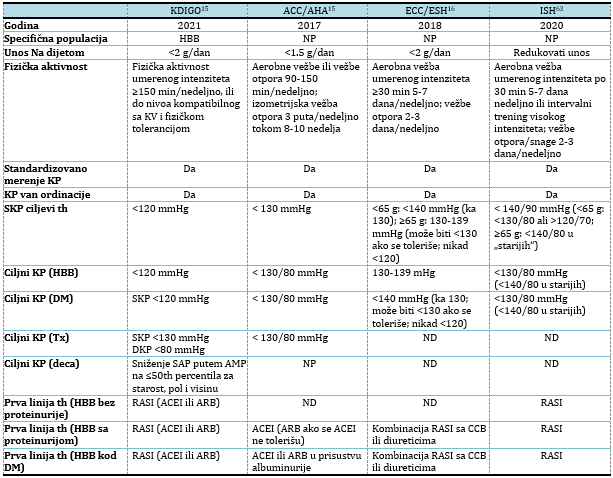
UVODVisok krvni pritisak (KP) je vodeći korektibilni faktor rizika za hronične bolesti u svetu [1]. Visok KP nije samo važan faktor rizika za hroničnu bubrežnu bolest (HBB) [2], već je i važan komorbiditet koji se javlja sa prevalencom od 86% u populaciji bolesnika sa HBB koji se ne leče dijalizom [3]. Kombinacija HBB i hipertenzije (HTA) dovodi do visokog rizika od kardiovaskularnih bolesti (KVB), koje su najčešći uzrok morbiditeta i mortaliteta kod bolesnika sa HBB [4]. Nekoliko kliničkih studija i meta-analiza pokazalo je da agresivan tretman HTA kod bolesnika sa i bez HBB snižava rizik od KVB, kao i svih uzroka mortaliteta, mada protektivni efekti sniženja KP na bubrežnu funkciju ostaju kontraverzni [5,6]. Iz tih razloga do sada je objavljeno više različitih vodiča/smernica za lečenje hipertenzije u HBB, od kojih je nekoliko poslednjih navedeno u tabeli 1. Tabela 1. Komparacija nekoliko najnovijih vodiča za hipertenziju
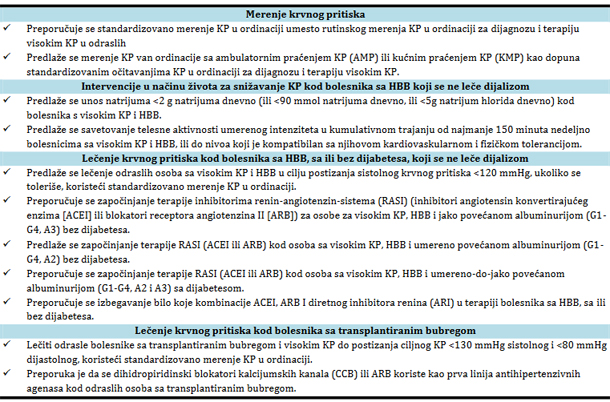
Revidirane smernice KDIGO 2021 takođe se odnose samo na populaciju bolesnika sa HBB koji se ne leče ponavljanim dijalizama i obuhvataju teme sadržane u originalnom vodiču, kao što su optimalni ciljevi krvnog pritiska, intervencije u načinu života, izbor antihipertenzivnih lekova i specifično lečenje kod bolesnika sa transplantiranim bubregom i kod dece (tabela 2). Neki aspekti opšteg i kardiovaskularnog zdravlja, kao što su kontrola displipidemije i pušenja su isključeni. Radna grupa istraživača i kliničara koja je radila na reviziji originalnih smernica identifikovala je dve glavne oblasti koje zaslužuju posebnu pažnju zbog pojave novih dokaza, a to su merenje vrednosti KP i ciljne vrednosti KP kod bolesnika sa HBB. Ova dva problema su usko povezana, jer ciljni SKP <120 mmHg zavisi od pravilnog pridržavanja standardizovanih protokola pripreme i merenja od strane bolesnika i kliničara. Sa druge strane, glavne primedbe su takođe usmerene na ova 2 fokusa: uočenu nepraktičnost standardizovanog merenja KP u kliničkoj praksi i teškoće u postizanju novih ciljnih vrednosti SKP [10]. Tabela 2. Ključne preporuke iz smernica kliničke prakse KDIGO 2021 za dijagnozu i terapiju krvnog pritiska u hroničnoj bubrežnoj bolesti.
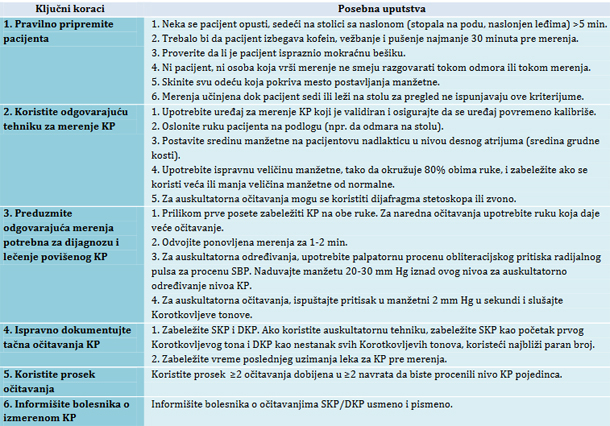
MERENJE KRVNOG PRITISKASfigmomanometrija je prva praktična metoda koju je Riva Rocci uveo u upotrebu 1896. godine za procenu SKP [11]. Očitavanje dijastolnog krvnog pritiska (DKP) postalo je izvodljivo 1905. godine, kada je Korotkov opisao svoju auskultatornu metodu merenja [20]. Ubrzo je zapaženo da KP dramatično varira od jednog očitavanja do drugog, pa je usmerena pažnja na standardizaciju metoda merenja kako bi se izbegle greške u proceni. Međutim, uprkos svim izdatim smernicama, preporukama i specifičnim pristupima za poboljšanje tačnosti merenja, nedavna meta-analiza je dokumentovala da je prosečni SKP u rutinskoj kliničkoj praksi za skoro 15 mmHg viši nego u istraživačkim studijama [13].Poglavlje 1 KDIGO vodiča je novi dodatak originalnim smernicama koji rasvetljava važnost preciznog merenja KP kod odraslih. Standardizovani KP se odnosi na merenja dobijena u skladu sa preporučenim pripremama i mernim tehnikama, bez obzira na vrstu opreme koja se koristi, nasuprot rutinskom merenju KP koje se sprovodi bez ovih priprema. Standardizovano merenje KP je sastavni deo ciljnih vrednosti KP i ciljne vrednosti se ne mogu oslanjati na rutinska merenja, jer su velike randomizovane studije na kojima su zasnovane ciljne vrednosti KP, uključujući SPRINT i ACCORD, dosledno koristile standardizovana merenja [10]. Nadalje, jaki dokazi pokazuju da rutinska i standardizovana merenja KP u ordinaciji ne daju iste vrednosti, a odnosi između ove 2 tehnike su vrlo varijabilni, pa nije moguće koristiti neki faktor korekcije za prevođenje rutinske vrednosti u standardizovanu vrednost KP [14]. KDIGO preporuke za merenje standardizovanog KP su u skladu sa drugim novijim smernicama [15-18], ali ono što čini kritičnu razliku je upravo insistiranje na širokom prihvatanju standardizovanog merenja KP kod bolesnika sa HBB, jer to omogućava primenu nižih ciljnih vrednosti SKP sa dokazanom efikasnošću u kliničkim ispitivanjima. Ključni elementi za uspešno merenje KP u ordinaciji uključuju pravilnu pripremu bolesnika, korišćenje proverenog uređaja za merenje, ispravne tehnike i prosečnih vrednosti KP iz bar 2 merenja (tabela 3). Bolesnike treba uputiti da isprazne mokraćnu bešiku i izbegavaju pušenje, kofein i fizičku aktivnost najmanje 30 minuta pre merenja KP. Trebalo bi da sede na stolici sa naslonom, udobno naslonjeni leđima i sa stopalima na podu >5 minuta pre očitavanja. Bolesnik i osoba koja vrši merenje bi trebalo da se uzdrže od razgovara tokom perioda odmora i tokom merenja KP. Ruka bolesnika mora biti oslonjena na čvrstu podlogu, a odeća uklonjena sa mesta postavljanja manžetne. Veličina manžetne treba da odgovara obimu ruke bolesnika, a manžetna treba biti postavljena u nivou srca (sredina grudnog koša). Smernice preporučuju 2 ili više očitavanja dobijenih u dva ili više navrata kako bi se dobila najbolja procena KP. Bolesnike treba informisati o njihovim vrednostima KP [10,15-18]. Tabela 3. Kontrolna lista za standardizovano merenje krvnog pritiska u ordinaciji
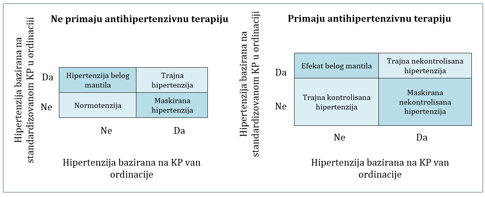
Tehnike za merenje KP van ordinacije uključuju kućni monitoring KP (KMP) i 24-časovni ambulatorni monitoring KP (AMP). Kod bolesnika koji ne uzimaju lekove za snižavanje KP, mogu se kategorisati sledeće 4 grupe na osnovu merenja KP u ordinaciji i van nje (slika 1): normotenzija, hipertenzija belog mantila, trajna hipertenzija i maskirana hipertenzija. Kod onih koji uzimaju lekove sa snižavanje KP, mogu se kategorisati slične 4 grupe: efekat belog mantila, trajna kontrolisana hipertenzija, trajna nekontrolisana hipertenzija i maskirana nekontrolisana hipertenzija [10]. Približno 30% bolesnika ima neusklađene vrednosti KP u ordinaciji i van ordinacije [23]. Maskirana nekontrolisana hipertenzija češća je kod osoba sa HBB u poređenju sa osobama bez HBB [24]. Maskirana hipertenzija povezana je sa povećanim rizikom od KVB i bubrežne insuficijencije. Nasuprot tome, hipertenzija belog mantila je udružena sa nižim rizikom za neželjene događaje od maskirane i trajne hipertenzije, iako bolesnici sa nelečenom hipertenzijom belog mantila imaju veći rizik neželjenih događaja nego bolesnici sa kontrolisanim KP u ordinaciji i van nje [25]. Visoka prevalenca hipertenzije belog mantila i maskirane hipertenzije, kao i povećani rizik od neželjenih ishoda zabeležen u opservacionim studijama, rezultirali su preporukom da se AMP i KMP koriste kao dopuna standardizovanim očitavanjima KP u ordinaciji za dijagnozu i terapiju visokim KP [10,15-17]. Slika 1. Obrasci KP zasnovani na merenjima KP van ordinacije kao dopuna standardizovanom merenju KP u ordinaciji
INTERVENCIJE U NAČINU ŽIVOTAPrema KDIGO smernicama, predloženi unos natrijuma treba biti <2 g dnevno (ili <90 mmol natrijuma dnevno ili <5 g natrijum hlorida dnevno) kod bolesnika sa visokim KP i HBB [10]. Interventne studije u opštoj populaciji pokazuju stepenovanu korist u smanjenju KP i rizika od KVB sa smanjenim unosom natrijuma ishranom [26]. Iako veći deo svetske populacije konzumira više od 2 g natrijuma dnevno, čak i skromno smanjenje unosa natrijuma koje ne dostiže ovaj cilj povezano je sa korisnim efektima na KP i KVB u opštoj populaciji [27]. Međutim, ne postoje velike i dugotrajne randomizovane kontrolisane studije koje procenjuju efekte ograničenja natrijuma u ishrani na kliničke ishode u populaciji bolesnika sa HBB. Nedavna meta-analiza koja je uključila samo studije sa bubrežnim bolesnicima otkrila je da smanjenje soli kod osoba sa HBB značajno smanjuje KP, a ako bi se takav efekat održavao dugoročno rezultirao bi klinički značajnim smanjenjem progresije HBB i KV događaja [28]. Konačno, ACEI i ARB se uobičajeno koriste u populaciji bolesnika sa HBB, a njihova korist za bubrege i KV sistem može se povećati ako ih prati ishrana sa niskim sadržajem natrijuma [29].S obzirom da podaci o specifičnim ciljevima unosa natrijuma u populaciji bolesnika sa HBB i visokim KP nisu čvrsto utemeljeni, radna grupa KDIGO usvojila je preporučeni cilj Svetske zdravstvene organizacije za unos natrijuma ishranom u opštoj populaciji [30], koji je u skladu sa preporukama nekoliko nedavno objavljenih vodiča za hipertenziju [16,17], ali i sa smernicama za upravljanje dijabetesom KDIGO 2020 [31]. Radna grupa je, takođe, zabeležila da postoje okolnosti u kojima se preporuke iz opšte populacije ne mogu primeniti na populaciju bubrežnih bolesnika. Upozorenje se odnosi na bolesnike sa HBB i nefropatijom sa gubitkom soli kod kojih smanjenje unosa natrijuma može biti neprikladno. Drugo važno upozorenje se odnosi na dijetetski pristup tretmanu hipertenzije, s obzirom da su dijete koje se koriste za snižavanje KP obično bogate kalijumom, a zamene za so takođe sadrže kalijum kao primarni katjon. Ovakav pristup bi mogao povećati rizik od hiperkalemije, naročito u odmaklom stadijumu HBB [10]. U sklopu promene životnog stila, bolesnicima sa visokim KP i HBB savetuje se fizička aktivnost umerenog intenziteta u kumulativnom trajanju od najmanje 150 minuta nedeljno, ili do nivoa kompatibilnog sa njihovom kardiovaskularnom i fizičkom tolerancijom. Studije u opštoj populaciji su jasno dokazale korisne efekte fizičke aktivnosti na snižavanje KP, fizičku kondiciju i snagu, gubitak telesne težine i smanjenje rizika od disglikemije i dijabetesa [10]. U populaciji bolesnika sa HBB dokazi su mnogo ograničeniji, ali takođe sugerišu da fizička aktivnost smanjuje KP i telesnu težinu i poboljšava kvalitet života [32,33]. Opservacioni podaci pokazali su dozno-zavisnu povezanost između većeg nivoa fizičke aktivnosti i nižeg rizika mortaliteta kod bolesnika sa HBB [34]. Sa druge strane, radna grupa KDIGO prepoznala je veću prevalencu komorbiditeta i slabosti u populaciji bolesnika sa HBB koji mogu ograničiti nivo fizičke aktivnosti i povećati rizik neželjenih događaja. Stoga stepen fizičke aktivnosti treba individualizirati u skladu sa kognitivnim i fizičkim stanjem bolesnika, koje se može menjati tokom vremena. Značajna zdravstvena korist se može ostvariti čak i ako nivo fizičke aktivnosti padne ispod predloženih ciljeva [10]. CILJNI KRVNI PRITISAKKod odraslih osoba sa visokim KP i HBB, KDIGO smernice predlažu ciljni SKP niži od 120 mmHg kada se toleriše, pod uslovom da se koristi metoda standardizovanog merenja KP u ordinaciji. Ova preporuka se odnosi na bolesnike sa dijabetesom i bez dijabetesa, a ne odnosi se na osobe sa transplantiranim bubregom ili na one koji se leče dijalizom [10].Za većinu bolesnika sa HBB, posebno za one starije, sa niskim nivom albuminurije ili u početnim stadijumima HBB, rizik od KVB i KV mortaliteta je mnogo veći od rizika progresije ka terminalnom stadijumu HBB [35]. Zato se ova KDIGO preporuka oslanja pretežno na rezultate visokokvalitetne i randomizovane SPRINT studije koja je pokazala korisne efekte na KV ishode i mortalitet u studijskoj kohorti hipertenzivnih osoba randomizovanoj na ciljni SKP <120 mmHg u odnosu na 140 mmHg [5]. U ovoj studiji 90% učesnika na početku je primalo antihipertenzivnu terapiju, a korisni efekti su dokazani i u grupi bolesnika sa HBB [36], kod starijih osoba [37] i kod onih sa predijabetesom [38]. Dve meta-analize takođe su saopšile smanjenje rizika za KV događaje sa intenzivnim sniženjem KP u populaciji osoba sa HBB, bez obzira da li je to smanjenje bilo jednako [39] ili niže od onog u opštoj populaciji [40]. Efekti intenzivnog snižavanja KP na progresiju HBB ka terminalnom stadijumu su manje sigurni. Postoji uobičajena percepcija da je snižavanje KP renoprotektivno, ali tek sekundarne analize nekih ranijih randomizovanih studija pokazale su da intenzivnije snižavanje KP smanjuje stopu progresije HBB kod bolesnika sa većom proteinurijom [41,42]. Međutim, rezultati dve najčešće citirane novije randomizovane studije SPRINT i ACCORD ukazuju da intenzivno sniženje SKP dovodi do malog, ali doslednog sniženja jačine glomerularne filtracije (eGFR, estimated glomerular filatration rate) ubrzo nakon početka u poređenju sa manje intenzivnom kontrolom (što se potencijalno može objasniti hemodinamskim efektima), dok efekti intenzivnog snižavanja SKP na eGFR tokom dužeg vremenskog perioda ostaju neizvesni [36,43]. Originalne KDIGO smernice iz 2012. godine preporučile su intenzivnije snižavanje KP za bolesnike sa albuminurijom od onih bez albuminurije [7]. Sa usvajanjem ciljnog SKP <120 mmHg za sve bolesnike sa HBB u revidiranim smernicama, odvojeni ciljevi za bolesnike sa i bez albuminurije više se nisu smatrali neophodnim. Radna grupa je smatrala da su koristi intenzivne kontrole SKP za KV ishode i preživljavanje nadmašile uočeno povećanje rizika od hiperkalemije, hipokalemije i akutnog oštećenja bubrega [36]. Međutim, dokazi koji podržavaju ciljni SKP <120 mmHg manje su sigurni u nekim subpopulacijama, uključujući bolesnike sa dijabetesom, uznapredovalom HBB (G4 i G5), značajnom proteinurijom (>1 g/dan), početnim SKP od 120-129 mmHg, kod mlađih od 50 godina ili veoma starih (starost > 90 godina), kao i kod onih sa hipertenzijom „belog mantila“ ili teškom hipertenzijom [10], (tabela 4). Na primer, ACCORD studija je proučavala isključivo osobe sa dijabetesom i randomizovala ih na iste ciljne vrednosti SKP kao i SPRINT studija (< 120mmHg, naspram <140 mmHg), ali je isključila one sa nivoom s-kreatinina >132,6 umol/L i one sa proteinurijom >1g/dan. Intenzivna kontrola KP je rezultirala manjim rizikom od moždanog udara, ali bez statistički značajnog smanjenja ukupnih KV događaja. Analize ACCORD studije sugerišu KV korist od ciljnog nižeg SKP u grupi sa standardnom kontrolom glikemije, ali ne i u grupi sa intenzivnom glikemijskom kontrolom [8,43,44]. Međutim, za slično smanjenje SKP postojao je veći rizik od opadanja eGFR kod osoba sa dijabetesom u ACCORD-BP studiji nego kod osoba bez dijabetesa u SPRINT studiji [45]. Stoga, radna grupa KDOQI (Kidney Disease Outcomes Quality Initiative) komentariše da odnos rizika i koristi od nižeg ciljnog SKP kod bolesnika sa HBB i dijabetesom zahteva dalje proučavanje u randomizovanim kontrolisanim studijama, a za sada u ovoj subpopulaciji smatra razumnijim ciljni SKP <130 mmmHg [46]. Tabela 4. Sigurnost dokaza koji podržavaju ciljni SKP <120 mmHg za bolesnike sa HBB
Skraćenice: HBB, hronična bubrežna bolest; DKP, dijastolni krvni pritisak; SKP, sistolni krvni pritisak; *HBB G4-G5 ukazuje na procenjenu GFR <30 ml/min/1.73m2. Neizvesnost u vezi sa koristima i rizicima intenzivnog snižavanja SKP u različitim subpopulacijama ne znači da intenzivno snižavanje KP nije opravdano, ali sugeriše da bi trebalo uzeti u obzir i potencijalne štetne efekte kada se odlučuje o ciljnom KP svakog pojedinačnog bolesnika. Nedoslednost u preporukama za ciljne vrednosti SKP može doprineti konfuziji lekara: ACC/AHA (American College of Cardiology/American Heart Association) smernice predlažu ciljni KP <130/80mmHg za bolesnike sa HBB, što je agresivnije u odnosu na preporuke ESC/ESH (European Society of Cardiology/European Society of Hypertension; SKP 130-139 mmHg) iz 2018. godine i drugačije od NICE preporuka (National Institute of Health and Care Excellence; SKP 120-129 mmHg) [15,16,47]. Ažurirani ESC klinički vodič o prevenciji KVB u kliničkoj praksi iz 2021. preporučuje ciljni SKP za osobe sa HBB <140-130 mmHg (niži SKP je prihvatljiv ako se toleriše) i DKP <80mmHg [48]. U praktičnom radu treba imati u vidu upozorenje da bi preporučeni niži SKP prema KDIGO smernicama bilo potencijalno opasno primeniti na merenja KP dobijena na nestandardizovani način. Takođe je razumno primeniti manje intenzivnu terapiju za snižavanje KP kod osoba sa vrlo ograničenim životnim vekom ili simptomatskom ortostatskom hipotenzijom [10].IZBOR ANTIHIPERTENZIVNIH LEKOVAPreporuke za izbor antihipertenzivne terapije u HBB zasnivaju se na dokazima da inhibitori renin-angiotenzin sistema (RASI), ACEI i ARB, smanjuju stopu KV događaja i krajnjih bubrežnih ishoda kod bolesnika sa HBB. Jačina dokaza varira od jakih u subpopulaciji bolesnika sa niskom eGFR i jako povećanom albuminurijom do slabih ili odsutnih u subpopulaciji sa normalnom eGFR i bez albuminurije. Mnogim bolesnicima sa HBB će biti potrebna kombinacija 2 ili više antihipertenzivnih lekova, ali ne postoje randomizovana ispitivanja koja upoređuju različite kombinacije lekova u HBB. Stoga se svaki algoritam za antihipertenzivnu terapiju u HBB zasniva na mišljenju stručnjaka, patofiziološkim ili farmakodinamskim razmatranjima, ili ekstrapolaciji nalaza iz opšte populacije [10].Kod bolesnika sa visokim KP, HBB (G1-G4) i jako povećanom albuminurijom (A3) bez dijabetesa, preporučuje se započinjanje terapije inhibitori renin-angiotenzin sistema (RASI) ACEI ili ARB [10]. Dokazi koji podržavaju ovaj stav zasnivaju se na rezultatima nekoliko placebo kontrolisanih randomizovanih studija koje su potvrdile efekat ove terapije na smanjenje rizika za neželjene bubrežne ishode i KV događaje [49-51]. Kod bolesnika sa visokim KP, HBB (G1-G4) i umereno povećanom albuminurijom (A2) bez dijabetesa, preporučuje se započinjanje terapije RASI (ACEI ili ARB) [10]. Ovo je slaba preporuka, jer ne postoje visokokvalitetni dokazi iz randomizovanih kontrolisanih studija koji procenjuju bubrežne ishode u ovoj subpopulaciji. Preporuka se uglavnom oslanja na rezultate HOPE (Heart Outcomes and Prevention Evaluation) studije koja je pokazala KV korist od ramiprila u odnosu na placebo, nezavisno od KP, kod bolesnika sa umereno povećanom albuminurijom [52]. Kod bolesnika sa visokim KP, HBB (G1-G4) i umereno do jako povećanom albuminurijom (A2 i A3) sa dijabetesom, preporučuje se započinjanje terapije RASI (ACEI ili ARB) [10]. Jaki dokazi iz IDNT (Irbesartan Diabetic Nephropathy Trial) i RENAAL studije (Reduction of Endpoints in NIDDM With the Angiotensin II Antagonist Losartan) ukazuju da RASI u poređenju sa placebom ili blokatorima kalcijumskih kanala (CCB), redukuju rizik od renalnih događaja kod bolesnika sa dijabetesom i ozbiljno povećanom albuminurijom [53,54]. MICRO-HOPE podstudija (Microalbuminuria, Cardiovascular, and Renal Outcomes substudy of Heart Outcomes Prevention Evaluation) je otkrila smanjenje KV rizika kod bolesnika sa dijabetesom i umerenom albuminurijom koji su bila randomizovani na primenu ramiprila [55,56]. U sprovedenoj meta-analizi, KDIGO ERT (Evidence Review Team) je pokazao da ACEI u poređenju sa placebom nisu imali efekta na ukupni mortalitet, ali su značajno redukovali rizik od dupliranja serumskog kreatinina i progresije albuminurije od kategorije A2 ka A3 [10]. U KDIGO smernicama izdvojeno je nekoliko praktičnih tačaka na koje treba obratiti pažnju. Prva sugeriše da bi RASI (ACEI ili ARB) bili razuman izbor terapije za osobe sa visokim KP, HBB i bez albuminurije, sa ili bez dijabetesa. Na osnovu nekih istraživanja [57], radna grupa KDOQI smatra da bi diuretik ili CCB bili podjednako razumni izbor kao lekovi prve linije za lečenje visokog KP kod bolesnika sa HBB bez dijabetesa i bez albuminurije [46], što je takođe u skladu sa ACC/AHA preporukama [15]. Dalje se naglašava potreba za primenom RASI (ACEI ili ARB) u najvećoj odobrenoj dozi koja se toleriše, jer su opisane koristi u ispitivanjima postignute korišćenjem baš ovih doza. Promene KP, nivoa serumskog kreatinina i kalijuma treba proveriti u roku od 2-4 nedelje nakon uvođenja ili povećanja doze RASI, a u zavisnosti od trenutne eGFR i nivoa kalijuma u serumu. Hiperkalemija povezana sa upotrebom RASI često se može lečiti merama za smanjenje nivoa kalijuma u serumu, umesto smanjenjem doze ili ukidanjem RASI. Terapiju sa ACEI ili ARB treba nastaviti, osim ako kreatinin u serumu ne poraste za više od 30% u roku od 4 nedelje nakon početka lečenja ili povećanja doze. O smanjenju doze ili ukidanju ACEI ili ARB treba razmisliti u uslovima simptomatske hipotenzije ili nekontrolisane hiperkalemije uprkos medicinskom lečenju, ili radi ublažavanja uremičnih simptoma tokom lečenja bubrežne slabosti (eGFR <15 ml/min/ 1.73m2). Antagonisti mineralokortikoidnih receptora (MRA) su efikasni u lečenju refraktarne hipertenzije, ali mogu izazvati hiperkalemiju ili reverzibilni pad bubrežne funkcije, posebno kod bolesnika sa niskom eGFR [10]. Posebna preporuka se odnosi na izbegavanje bilo kakve kombinacije ACEI, ARB ili direktnog inhibitora renina (DRI) kod bolesnika sa HBB, sa ili bez dijabetesa. Ovo je snažna preporuka zasnovana na dokazima iz randomizovanih kontrolisanih studija dovoljnog trajanja za procenu bubrežne i KV protekcije. Sve je više dokaza da dvojna RAS blokada ne vodi dugoročno korisnim KV ili bubrežnim efektima uprkos kratkotrajnom sniženju proteinurije, a sa druge strane povećava rizik od hiperkalemije i AOB. Velika meta-analiza koja je upoređivala efekte monoterapije i dvojne blokade RAS kod bolesnika sa HBB, sa i bez dijabetesa, nije pronašla značajne razlike u ukupnom mortalitetu, progresiji ka terminalnom stadijumu HBB i KV događajima između 2 grupe [58]. Nasuprot tome, postoje dokazi da dvojna blokada RAS kod bolesnika sa HBB, sa i bez dijabetesa, povećava incidencu AOB za 40% u odnosu na monoterapiju [9,59]. Stoga se može smatrati opravdanim što ova preporuka pridaje veću važnost prevenciji hiperkalemije i AOB u odnosu na potencijalnu korist od redukcije albuminurije [46]. Većini bolesnika sa HBB će biti potrebna višestruka antihipertenzivna terapija sa ACEI ili ARB kao dodatak CCB i diureticima radi postizanja ciljnih vrednosti KP. Instrumentalna analiza varijabli koju su uradili Markovitz i saradnici demonstrirala je postepeno snižavanje SKP i kardiovaskularnog rizika sa uvođenjem svakog dodatnog antihipertenzivnog agensa u SPRINT studiji [60]. Diuretici se često koriste kod bolesnika sa HBB i visokim KP zbog postojeće hipervolemije, ali je literatura o efektima diuretika na glavne kliničke ishode u ovoj populaciji ograničena. Ograničeni podaci pokazuju da dodavanje MRA, kao što su spironolakton, eplerenon ili finerenon, osnovnom ACEI ili ARB za renoprotekciju kod bolesnika sa HBB smanjuje KP i proteinuriju/albuminuriju, ali sa merljvim rizikom od hiperkalemije [61]. Nedavno objavljeno istraživanje FIDELIO-DKD (The Finerenone in Reducing Kidney Failure and Disease Progression in Diabetic Kidney Disease) u populaciji bolesnika sa HBB i dijabetesom pokazalo je protektivni efekat finerenona na bubrege i KV sistem, uprkos njegovom skromnom efektu na SKP i većoj incidenci događaja povezanih sa hiperkalemijom [62]. ZAKLJUČAKAžurirani KDIGO vodič kliničke prakse iz 2021. godine insistira na standardizovanom merenju KP u ordinaciji i preporučuje ciljni SKP <120 mm Hg u većini subpopulacija bolesnika s HBB, pod uslovom da se koristi ova tehnika. Implementacija standardizovanog merenja KP u užurbanoj kliničkoj praksi je prepoznata kao izazov, ali je fundamentalna za praksu medicine zasnovane na dokazima, jer su dostupni dokazi za preporuke o lečenju izvedeni iz studija u kojima je KP meren na ovaj način. To znači da je usvajanje ciljnog SKP <120 mmHg neraskidivo povezano sa tehnikom standardizovanog merenja KP, a od toga zavise korisni efekti na KV sistem i bubrege koji bi dugoročno proistekli iz intenzivnijeg snižavanja KP kod bolesnika sa HBB. S obzirom na važnost ovih ciljeva i postojeći otpor standardizaciji metode, moguće je da će nove mere zahtevati regulatornu primenu standardizovanih protokola za merenje KP u rutinskoj kliničkoj praksi.Bez obzira na preporučeni ciljni SKP, radna grupa KDIGO upozorava na oprez u pojedinim subpopulacijama bubrežnih bolesnika ukazujući da je razumno primeniti manje intenzivne ciljeve KP kod osoba sa vrlo ograničenim životnim vekom ili simptomatskom ortostatskom hipotenzijom. Ova sugestija podržava autonomiju lekara i zajedničko donošenje odluka, u zavisnosti od karakteristika bolesnika, podnošljivosti i preferencija, a u cilju selekcije onih bolesnika koji će najverovatnije imati koristi od intenzivnijeg snižavanja KP. Potrebne su velike randomizovane kontrolisane studije o efektima intenzivnog snižavanja KP na kardiovaskularne, bubrežne i kognitivne ishode i/ili preživljavanje kod bolesnika sa HBB, a posebno u subpopulacijama koje nisu bile adekvatno zastupljene u prethodnim ispitivanjima. Takođe su neodložno potrebna randomizovana ispitivanja koja bi upoređivala efekte različitih kombinacija antihipertenzivnih lekova na ishode, a što bi doprinelo razvoju algoritama zasnovanih na dokazima za lečenje hipertenzije u HBB. LITERATURA:
|
||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||
| Adresa autora: Biserka Tirmenstajn
Janković, Odeljenje nefrologije i hemodijalize, Zdravstveni centar
“Zaječar” E-mail: biserkatirmenstajn@gmail.com |
Rad primljen: 21.7.2022. Elektronska verzija objavljena: 4.11.2022. |
|||||||||||||||||||||||||||||||||||
| [ Sadržaj
] [ Indeks autora ]
|
||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||