| |
|
|
UVOD
Klinička slika miokarditisa je raznovrsna [1]. Miokarditis (MY)
može biti uzrok iznenadne srčane smrti kod mladih odraslih osoba bez
poznatih srčanih oboljenja u 20%, idiopatske ventrikularne
tahikardije (VT) u 30%, akutne srčane insuficijencije u 10% [2,3].
MY je jedan od vodećih uzroka iznenadne srčane smrti i dilatacione
kardiomiopatije (DCM) u mladih osoba [4,5]. U kliničkoj seriji
iznenadne srčane smrti, MY je treći vodeći uzrok posle hipertrofične
kardiomiopatije i kong enitalnih i aterosklerotskih bolesti
koronarnih arterija [6]. Autopsijske studije pokazuju da je MY je
čest uzrok DCM kod biopsijom dokazanog miokardita ali sa velikom
varijacijom od serije do serije: od 0,5% do 67% , medijana je 10,3%.
Zbog mogućnosti klinički tihog toka bolesti i retke biopsije
miokarda, tačna učestalost: incidenca i prevalenca MY i inflamatorne
kardiomiopatije(ICM) nije poznata [7,8].
Miokarditis (MY) ili inflamacija miokarda može biti rezultat
multiplih uzroka, ali je uobičajano vezana za infektivne agense i
više od 20 virusa koji oštećuju miokard direktnom invazijom,
produkcijom kardiotoksičnih supstanci i inflamacijom, sa ili bez
perzistentne infekcije kao i autoimune rekacije na srčane epitope
[7,9,10,11]. AVMY je jedan od najvećih izazova u pogledu kako
dijagnoze, tako i terapije [7,12]. Klinička klasifikacija AVMY
[7,13]:
- Moguć subklinički akutni miokardititis (tipični virusni
sindrom bez srčanih simptoma a sa EKG promenama, pozitivnim
biomarkerima CKMB i troponin, uz ehokardiografski nalaz: pad EF
i regionalne anomalije pokretljivoisti zidova leve komore i
promene u teksturi miokarda)
- Verovatan klinički akutni miokarditis (sve predhodno+
simptomi: bol, kratkoća daha, palpitacije etc.)
- Definitivni miokarditis (potvrdjen patohistološki,
imunohistohemijski i PCR virusni genom putem EMB)
Ova klasifikacija još uvek nije revidirana putem kardiomagnetne
rezonance (CMR), što bi bilo neophodno.
Termin ICM uveden 1995 od strane Svetske zdravstvene organizacije
[14] i podrazumeva miokarditis sa sistolnom disfuncijom i/ili
dilatacijom leve komore, ali on ne opisuje fenotip i ne definiše
uročnika [15]. Po toku se virusni miokarditisi dele na subakutni i
hronični, često se govori o njima ali retko se dokazuju [15].
Postoji promena najčešće vrste uzročnika virusnih miokardita, ranije
su to bili Koksaki B virusi i adenovirusi a poslednje dve decenije
Parvo B19, herpes virus tip 6, hepatitis C virus, a sada ređe
koksaki B virusi, adenovirusi, Epštajn-Bar-ov virus i
Citomegalovirus. [7,11,12]. Miokarditis takođe može da se razvije u
bolesniika sa HIV infekcijom, hepatitisom C ili Lajmskom bolešću
[7,11,12]. Najskorije od 2019 u toku COVID 19 epidemije javljaju se
dokazani slučajevi miokarditisa izazvanog virusom SARS CoV-2, ali se
o tome još nedovoljno zna [16-20].
Najveći broj bolesnika sa akutnim virusnim miokarditisom se oporavi
bez sekvela, ali jedan deo bolesnika progredira u hroničnu
inflamatornu i dilatacionu kardiomiopatiju, srčanu insuficijenciju i
bude kandidat za transplantaciju srca [1,5,12, 13,15].
Do danas ne postoji takozvani neinvazivni zlatni standard za
dijagnozu AVMY zbog niske specifičnosti i senzitivnosti
tradicionalnih dijagnostičkih testova, ali razvoj kardiomagnetne
rezonance je obećavajući [12,21,22]. Endomikardna biopsija sa
patohistološkim pregledom i prisustvom virusnog genoma jesu
najpouzdanije metode, ako se dobiju reprezentativni uzorci miokarda
[7,9] i ona omogućavaju primenu terapijskog algoritma, ali je ova
invazivna dijagnostika uglavnom rezervisana za teže i nejasne
slučajeve inflamatornih kardiomiopatija. Zato klinička slika, EKG,
biomarkeri i imaging metode, prvenstveno u praksi najlakše
izvodljiva ehokardiografija i sve više magnetna rezonanca, mogu u
vidu mozaika da komplementarno slože dijagnozu miokardita na osnovu
kliničke slike i različitih dijagnoističkih kategorija sa ESC skorom
od 2 i više bodova [11,12].
Glavne tegobe AVMY su uobičajeno: umor, palpitacije, bol u grudima,
nedostatak vazduha pri naporu a fizikalnim pregledom se otkriva
tahikardija, oslabljen prvi ton S1 i često ritam S3 galopa i de novo
mezosistolni šum [13,15,21]. Uobičajeni EKG nespecifični nalaz kod
klinički suspektnog AVMY je najčešće sinusna tahikardija i razne
disritmije: ventrikularne i supraventrikularne ekstrasistole, retko
ventrikularna tahikardija i atrijalna fibrilacija i ređe
bradikardija i srčani blokovi; EKG promene u ST segmentu i T talasu
su dosta specifične za leziju miokarda: tranzitorne promene u ST
segmentu i T talasu, depresija ili elevacija ST segmenta, duboki
negativni T talasi, blok leve grane Hissovog snopa i nekad slika
infarkta miokarda [13,15, 21].
Laboratorijski se otkrivaju povišeni srčani troponini a postoje i
noviji markeri. Kod dece sa fulminantnim miokarditisom, viši nivo
kreatinina, laktata i aspartat-transaminaze (AST) u serumu povezan
je sa povećanim mortalitetom u bolnici [23]. Natriuretički peptid
(NT-pro-BNP) je povišen kod dece sa akutnom ICM-om i generalno brzo
opada pri oporavku funkciju leve komore [24]. Kod odraslih su veće
koncentracije interleukina-10 povezane sa povećanim rizikom od
smrti. Zabeleženo je da antitela na miokard (AHA) predviđaju
povećan rizik od smrti ili potrebu za transplantacijom. [25].
Titrovi cirkulišućih virusnih antitela nisu u dobroj korelaciji sa
tkivnim virusnim genomima i zbog niske senzitivnosti retko su za
korisni za dijagnostičku upotrebu u praksi [11,12, 26].
NEINVAZIVNE SLIKOVNE TEHNIKE SNIMANJA (imaging). Koncept
imidžinga je evoluirao od monomodaliteta u multimodalitet imidžing
strategiju gde svaki test dodaje informacije koje povećavaju
specifičnost dijagnostičkog markera za dijagnozu miokarditisa.
Transtoraksna Ehokardiografija (TTE) je najdostupnija metoda uz
bolesničku postelju a kojom može da se posumnja na miokarditis.
Ehokardiografski znaci klinički suspektnog AVMY su variabilni i
heterogeni: najčešće disfunkcija leve komore uz poremećaje
regionalne segmentne kinetike, dilatacija leve komore ili perikardni
izliv, retko intrakardijalni tromb ali nalaz može da bude i normalan
[11,12,27]. Kada je ehokardiografski prozor neadekvatan, važan korak
u dijagnostici je transezofagusna ehokardiografija [28]. Imidžing
deformacije putem spekl treking strejn ehokardiografije (speckle
tracking strain) obično pokazuje snižen longitudinalni patern
deformacije miokarda ali to je takođe nespecifičan znak bolesti
miokarda. Prednost metode je što može da prepozna rane promene
funkcije miokarda pre nego što ih vidimo uz pomoć „običnih“ ili
konvencionalnih metoda koje se zasnivaju na merenju ejekcione
frakcije leve komore(EF). [29,30,31,32,33]. Sniženje globalne
longitudinalne deformacije (GLS) ima diagnostičku vrednost i utiče
na prognozu bolesti kod inflamatorne kardiomiopatije i srčane
insuficijencije. Srčana magnetna rezonanca (CMR) je korisna u
postavljanju dijagnoze AVMY i za praćenje napredovanja bolesti, a
prisustvo kasnog nakupljanja gadolinijuma (LGE) je najbolji
nezavisni prediktor za srčani mortalitet [21,34,35]. CMR pokazuje a
vezivanje gadolinijuma u medijalnom delu miokarda leve komore i
subepikardno, što se potpuno razlikuje od nalaza kod ishemijske
kardiomiopatije [9,11,12,35].
Endomiokardna biopsija (EMB) sa patohistološkim pregledom i
prisustvom virusnog genoma putem PCR i imunohistohemijskih dokaza
inflamacije jesu najpouzdanije metode i omogućavaju primenu
terapijskog algoritma, ali je ova invazivna dijagnostika uglavnom
rezervisna za teške slučajeve i kardiomiopatije. [7,9]. Ako uzorci
miokarda nisu reprezentativni mogući su lažno negativni nalazi EMB.
Ipak većina autoriteta podržava koncept da EMB treba da bude zlatni
standard za dijagnozu definitivnog miokarditisa. [7,9,11,12].
U osnovi lečenja AVMY je lečenje srčane insuficijencije i aritmija.
Specifično lečenje za fulminantni i akutni AVMY je antivursna
terapija a za posvirusni hronični autoreaktivni miokarditis je
imunosupresivna terapija kortikosteroidima i ciklosporinom [36] te u
najnovije vreme CD3 muromonab-om [22].
CILJEVI ISTRAŽIVANJA: Analizirati vrstu i značaj
ehokardiografskih parametara i karakteristika u dijagnozi klinički
suspektnih akutnih virusnih miokarditisa u svakodnevnoj praksi.
Utvrditi kakvu ulogu ima dinamika titra antivirusnih antitela za
dijagnozu klinički suspektnog akutnog virusnog miokarditisa i
izvršiti komparaciju virusne serologije u odnosu na ehokardiografske
parametre dijastolne i sistolne funkcije leve komore.
MATERIJAL I METODE
Urađena je retrogradna transverzalna studija u desetogodišnjem
periodu od 2006. do 2015. godine gde je izdvojeno iz baze podataka
Internističke ordinacije "Dr Bastać", 126 konsekutivnih pacijenata
klinički suspektnih na akutni virusni miokardit (grupa A) koji su
klinički, ehokardiografski i serološki praćeni zbog dinamike titra
antitela na kardiotropne viruse. Ispitivana grupa (A) je bila
prosečne starosti 43,3± 8,9 godina, indeksa telesne mase BMI 27,8 ±
5,9 , dominira ženski pol-78 (62%). Srednje vrednosti sistolnog i
dijastolnog pritiska na dolasku su bile -127 ± 14 /78 ± 11 mmHg.
Kontrolna grupa (B) je bila komparabilnih karakteristika: 103 osobe
prosečne starosti 46±12 godina, indeksa telesne mase BMI 29,3±6,4,
53 osobe (52%) ženskog pola. Srednje vrednosti sistolnog i
dijastolnog pritiska na dolasku su bile 136 ± 14 / 71 ± 11 mmHg.
Kriterijumi isključivanja Odsustvo hipertenzije, poznate
koronarne bolesti, valvularnih mana drugih relevantnih bolesti i sa
niskom pre-test verovatnoćom (PTP) <15% na ishemijsku bolest srca.
Kriterijumi uključivanja: korišćeni su najpre kriterijumi
Dennerta i saradnika iz 2007 [7] a kasnije su re-evualirani putem
kriterijuma Radne grupe za bolesti miokarda i perikarda Evropskog
udruženja kardiologa iz 2013 godine za klinički suspektan
miokarditis [11]. Bilo je potrebno da imaju najmanje 2 kriterijuma:
najmanje jedan iz grupe kliničkih prezentacija i najmanje jedan iz
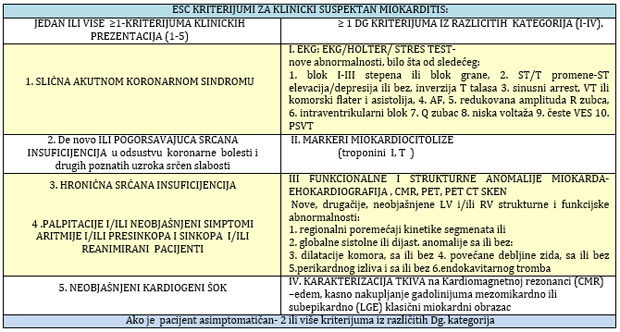
grupe dijagnostičkih kategorija što je prikazano na TABELI 1 [11]:
TABELA 1. Kriterijumi Radne grupe za bolesti
miokarda i perikarda Evropskog udruženja kardiologa iz 2013. godine
za klinički suspektan miokarditis [11]
METODOLOGIJA. Uz rutinske kliničke metode: anamneza i fizikalni
pregled, EKG, antropometrija, osnovna biohemija krvi, svima je
rađena ehokardiografija i serologija IgM i IgG antivirusnih
antitela. U pojedinačnim slučajevima je rađena radiografija toraksa
, te troponin T, pro BNP i D dimer. Vrlo retko je finalizovan
predloženi pregled na kardio-magnetnoj rezonanci , dok je
endomiokardna biopsija urađena samo kod 2 pacijenta
EHOKARDIOGRAFIJA. Ehokardiografski pregledi su obavljani pomoću
aparata marke „Toshiba Power Vision 6000", Toshiba Xario CV i GE
Vivid 7 multifrekventnim sektorskim sondama od 2,0 do 4,5 MHz sa
harmonskom slikom (harmonic imaging). Svi ispitanici su podvrgnuti
pregledu standardnim protokolom prema tada važećim preporukama
[37,38] a interpretirani su u svetlu najnovijih preporuka za
standarde u izvođenu ehokardiografije [39,40]. Ehokardiografski
pregledi su vršeni metodama konvencionalne M-mode i dvodimenzionalne
(B-mod) ehokardiografije, a takođe je izvršena i Doppler analiza
transmitralnog protoka tokom dijastole, kao i pregled metodom
pulsnog tkivnog (Tissue) Doppler-a. Od strukturnih parametara,
izmereni su između ostalih: dijametar leve pretkomore (LA),
teledijastolni dijametar leve komore (LVEDD), telesistolni dijametar
leve komore (LVESD), debljina zadnjeg zida leve komore (PWTd) i
interventrikularnog septuma u dijastoli (IVSTd). Kriterijum za
dilatacija leve komore bio je teledijastolna dimenzija leve komore
≥54mm za žene i ≥59mm za muškarce) [37]. Volumeni leve komore i
ejekcione frakcije leve komore (EF) su automtski izračunavani putem
Teicholtz metode i biplejn Simpsonovog pravila [37] a zatim su
izračunati masa leve komore (LVM) formulom po Devereux-u i indeks
mase leve komore (LVMI).
( LVMI (g/m²) = [(TDD + ZZd + IVSd)3 –TDD3] x 1.05-13.4 / BSA (m²)
[37]
Normalna masa miokarda je za muški pol do 224 g a za ženski do 162g.
Indeks mase miokarda je za ženski pol manje od 95 g/m², za muški
manje od 115 g/m². Dijastolna funkcija je procenjena merenjem
maksimalne brzine rane (E) i kasne (A) faze komorskog punjenja,
vreme decelacije E brzine(DTE, normalno 160-200 ms), kao i
izračunavanjem odnosa E/A (normalno E/A ≥0.8). Tehnikom tkivnog
Doppler-a, izvršena su merenja tkivnih dijastolnih (e') i sistolnih
brzina (S´) miokarda na septalnoj i lateralnoj strani mitralnog
anulusa i uzimana je srednja vrednost (e'), a potom je izračunat
odnos E/e' [38], kao surogat pritiska punjenja leve komore
Dijastolna funkcija je kategorizovana kao:
(a) normalna ( E/A ≥0.8 - <1.5, vreme decelacije E brzine-DTE >160
ms, srednji E/e’≤8);
(b) Stepen 1, oštećena relaksacija (E/A <0.8, DTE >200 ms, srednji
E/e’≤8);
(c) Stepen 2, Pseudonormalizacija (E/A ≥0.8 and <1.5, DTE 160–200
ms, srednja E/e’ = 9–12);
(d) Stepen 3, Retstiktivni obrazac (E/A ≥1.5, DTE <160 ms, srednja
E/e’ ≥13).
Regionalni poremećaji u kontraktilnosi leve komore jesu segmentne
hipokinezije, akinezije, diskinezije. Promene u teksturi miokarda;
hiperehogene ektenzivne subendokardne ili transmuralne zone su jasan
nalaz dok ovalne hiperehogene zone miokarda- najčešće u
intraventrikularnom septumu su kontraverzan parametar. Značajne su
samo ekstenzivne zone ili 3 manje zone prečnika ≥3mm ili pak
transmuralno zahvatanje (znaci fibroze i cicatrixa) uz hipokineziju.
Na osnovu gore navedenih kriterijuma se postavljao klinički
suspektan miokarditis–tim pacijentima se (do 2015) rutinski
određivao serumski nivo antitela IgM I IgG na Parvo B19, Koksaki i
Adenovrus, a izuzetno i na ređe potencijalne izazivače (Ebštajn Bar
virus, citomegalovirus, virus influence, hepatitis C) određivan iz 2
uzorka uparenih seruma na 2 do 8 nedelja. Antivirusna antitela i
antisrčana antitela su određivana enzimo-imunološkom metodom
(ELISA). Na osnovu pozitivnosti IgM antivirusnih antitela ispitivana
grupa (A) je podeljena na podgrupe: A1 sa povišenim titrom antitela
klase IgM kod 43 (32%) ispitanika (PODGRUPA A1) i A2 bez povišenog
titra IgM antitela (Grupa A2)- 83(68%) pacijenata. (PODGRUPA A2).
Statsitička obrada je rađena u bazi EXCEL putem metoda deskriptivne
statistike, Studentovog-T testa i Hi2 testa.
REZULTATI
Klinički suspektan miokarditis (grupa A) sa ≥2 ESC kriterijuma)
imalo je 126 pacijenata (GRUPA A). Najčešći simptomi su bile
palpitacije 107/126 (85%), bol u grudima 83/126 (66%) i zamaranje,
osećaj umora, nedostatak vazduha i dispneja na napor 62/126 (49%) u
raznim kombinacijama (TABELA 2)
TABELA 2 Simptomi, fizikalni znaci i EKG promene kod pacijenata
grupe A sa suspektnim miokarditisom i/ili inflamatornom
kardiomiopatijom
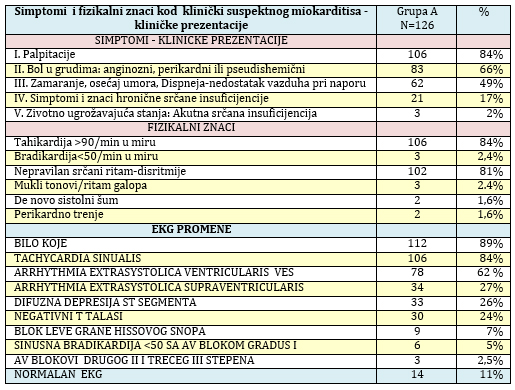
U fizikalnom nalazu kod suspektnog miokardita (TABELA 2) dominirala
je tahikardija 106/126 (84%), nepravilan srčani ritam 102/126 (81%)
a dosta ređe su bile teže kliničke forme: znaci srčane
dekompenzacije 21/126 (17%), (kasnoinspiratorni pukoti na plućima,
tahipneja, dispneje u miru. nabrekle vene na vratu,
kasnoinspiratorni pukoti na plućima, hepatomegalija, periferni
edemi). Objektivni, fizikalni nalaz je bio normalan u 14 /126 (11%)
ispitanika
Od 126 slučajeva grupe A većina je imala neke EKG promene-112/126
(89%), a sa normalnim EKG je bilo samo 14/126 (11%) ali kod njih su
nađene ehokardiografske promene. Analizom EKG-a (TABELA 2)
registruje se visoka učestalost nespecifičnih poremećaja-disritmija:
sinusna tahikardija u 112/126 (89%), ventrikularne ekstrasistole
78/126 (62%), supraventrikularne ekstrasistole 24/126 (19%) i
elektropatoloških promena za klinički suspektan miokarditis: difuzna
depresija ST segmenta 33/126 (26%), difuzno negativni T talasi
30/126 (24%) i blok leve grane Hisovog snopa u 9(7%) bolesnika.
Analizom parametara merenih transtorakalnom ehokardiografijom (TTE),
u zastupljenosti ehokardiografskih kriterijumima za klinički
suspektan miokardit grupe A (TABELA 3) dominirala je dijastolna
disfunkcija leve komore u 39/126 (31%), od toga je 17 (14%) imalo
težu dijastolnu disfunkciju gradus III.
Globalna sistolna disfunkcija leve komore kvantifikovana putem
ejekcione frakcije leve komore (EF) manje od 50% (EF<50%) nađena je
kod 19/126 (15%) i kod svih je bila prisutna blaga do umerena
dilatacija leve komore i kriterijumi za inflamatornu kardiomiopatiju
(ICM). Povećana masa miokarda leve komore i indeks mase miokarda
leve komore (LVMI) usled mogućeg edema miokarda registrovan je u 16
pts (13%) od ovih 19 pacijenata. Regionalna sistolna disfunkcija
(hipokinezija 2 ili više miokardnih segmenata leve komore) koji
najčešće nisu po distribuciji perfuzije koronaranih arterija,
utvrđena je u 21/126 (17%), uz prisutan cicatrix u 11 pacijenata.
najčešće infero-postero-lateralno. Akinezije miokarda nije bilo u
ispitivanoj grupi a diskinezija septuma je bila prisutna u bloku
leve grane (nije uzimana u obzir) kod 9 bolesnika (7%). Promene u
teksturi miokarda- ekstenzivne hiperehogene zone miokarda i
fibroza-cicatrix nadjene su u 17 (13%) ispitanika. Ipak 24/126 (19%)
pacijenata je imalo potpuno normalan ehokardiografski nalaz ali uz
kliničke i EKG kriterijume za miokarditis.
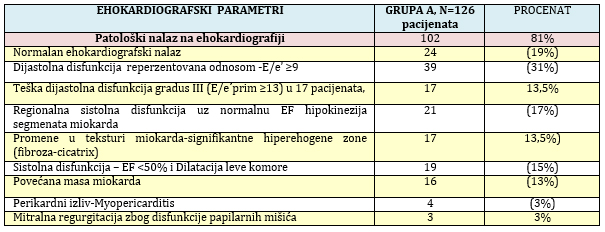
TABELA 3. EHOKARDIOGRAFSKI PARAMETRI U INDIVIDUALNOJ DISTRIBUCIJI
kod klinički suspektnog mioakrdita (grupa A)
Kod pacijenata sa klinički suspektnim miokarditisom je klinička
verovatnoća virusne etiologije je dijagnostički potkrepljena
povišenim titrom antitela klase IgM kod 43 (32%)
ispitanika-(podgrupa A1) (GRAFIKON 1) dok je većina je bila bez
povišenog titra IgM antitela (Grupa A2)- 83 (68%) pacijenata.
GRAFIKON 1. Distribucija IgM serološke pozitivnosti kod 43 (34%) od
126 ispitivanih pacijenata na suspektnu skorašnju infekciju virusom
i dokaz autoimunog odgovora putem povišenog serumskog titra AHA
antitela
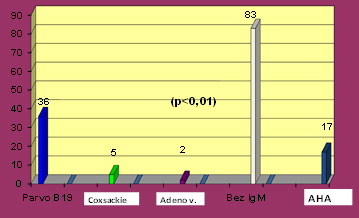
Postoji dominacija IgM antitela na virus Parvo B 19 u 36/43 (84%)
pacijenata(p<0,01) a samo u 5/43 (12%) slučajeva na Coxsackie B i u
2/43 (5%) pacijenta na Adenovirus. Većina pacijenata je bila bez
povišenog titra IgM antitela-(podgrupa A2) od 83 (68%) pacijenata a
oko polovine njih -41/126 (32%) ima samo povišen serumski titar IgG
antitela na kardiotropne koji nema dijagnostički značaj sam za sebe,
bez dinamike titra IgM antitela.
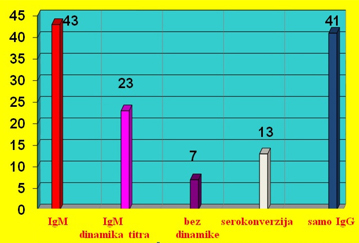
Jasna dinamika titra IgM je zabeležena kod 23/126 (18%) ispitivane
osobe a pad titra uz rast IgG titra (serokonverzija) u 13/126 (10%)
bolesnika, dok je bez uhvaćene dinamike titra bilo 7 bolesnika
(GRAFIKON 2).
GRAFIKON 2. Dinamika titra IgM antitela na kardiotropne viruse i
serokonverzija Igm u IgG kod 43 pacijenata podgrupe A1
Povišen titar IgG antitela nema dijagnostički značaj sam za sebe,
bez dinamike titra IgM antitela. U grupi A2 bez IgaM povišen
serumski titar IgG antitela na kardiotropne viruse imalo je 41/126
(32%) (grafikon 2), najčešće na parvo B19, adenovirus i koksaki B.
Čak 42/126 bolesnika (33%) nije imala povišen titar ni IgM ni IgG
antivirusnih antitela, ali su imali jasne kriterijume (2 i više) za
klinički miokardtitis a od njih je 8 imalo povišena antisrčana
antitela i znake inflamatorne CMP. Određivanje antisrčanih
autoantitela (AHA) koje je novijeg datuma urađeno kod težih
slučajeva 17 inflamatorne kardiomiopatije (GRAFIKON 1) i od toga su
8 njih imali antimiokardna autoantitela, ali njihova uloga nije još
definisana.
Kvantitativni ehokardiografski parametri kod pacijenata sa klinički
suspektnim miokarditisom su prikazani na TABELI 4 i GRAFIKONIMA 3 i
4
TABELA 4. Kvantitativni ehokardiografski parametri u odnosu na
virusnu serologija kod klinički suspektnog miokardita
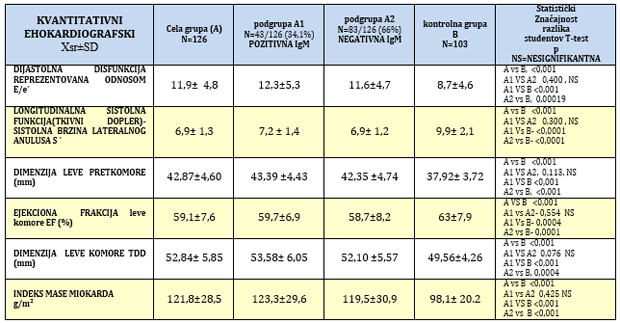
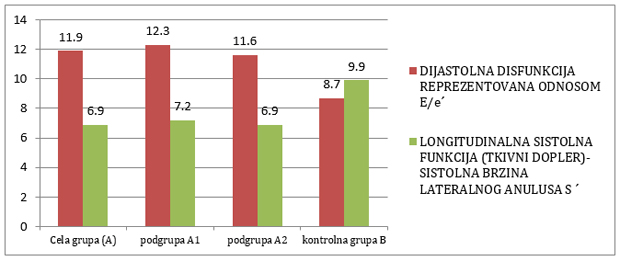
GRAFIKON 3. kvantitativni ehokardiografski parametri tkivnog
Dopplera: dijastolna funkcije i longitudinalna sistolna funkcija u
odnosu na virusnu serologija kod klinički suspektnog miokardita
GRAFIKON 4. Ehokardiografski parametri sistolne funkcije i dimenzija
leve komore i pretkomore u odnosu na virusnu serologija kod klinički
suspektnog miokardita
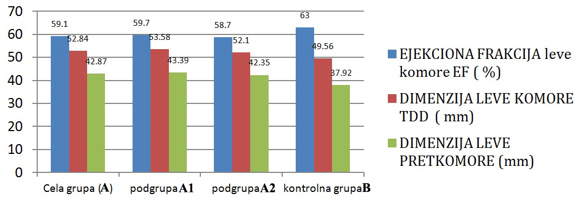
Cela grupa G klinički suspektnog miokardita u odnosu na kontrolnu
grupu C ima statistički visoko značajno snižene parametre sistolne
funkcije (EF=59,1±7,6% vs. 63±7,9%; p<0,001) (tabela 4 i grafikon 3)
uključujući i longitudinalnu sistolnu funkciju S´ putem tkivnog
doplera 6,9±1,3 cm/s vs. 9,9±2,1; p<0,001 (tabela 4 i grafikon 4).
Dijastolna disfunkcija (E/e´11,9±4,8 vs. 8,7±4,6; p<0,001) prikazana
na tabela 4 i grafikonu 3, je visoko značajno izražena u ispitivanoj
grupi vs kontrolna grupa. Povećanje teledijastolne dimenzije leve
komore (TDD, EDD), indeksa mase miokarda (LVMI) i dimenzije leve
pretkomore (TABELA 4 i GRAFIKON 4) je statistički visoko značajno
povećana u grupi klinički suspektnog miokarditisa. Cela grupa g
klinički suspektnog miokardita ima indeks mase miokarda statistički
značajno veći, što se objašnjava edemom miokrda a ne hipertrofijom
kao u hipertenziji.
Komparacijom podgrupa A i B nije nađena statistički značajna
razlika, izmedju IgM pozitivnih i IgM negativnih pacijenata u odnosu
na na kvantitativne ehokardiografske promene (TABELA 4 i GRAFIKONI 3
i 4) što znači da povišen titar IgM antitela i serokonverzija ne
ukazuju na stepen oštećenja miokarda i samim tim na težu formu
miokarditisa.
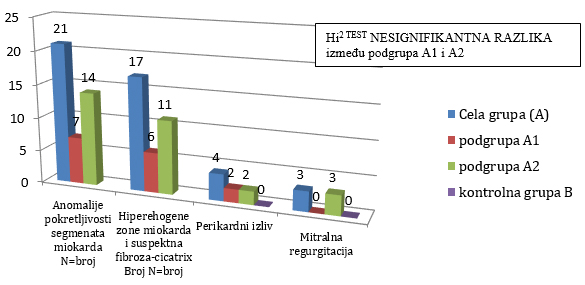
Kvalitativne ehokardiografske promene su prikazane na GRAFIKONU 5.
Ove promene se ne javljaju u kontrolnoj grupi, što ukazuje na
njihovu dobru specifičnost. Kao iza kvantitativne ehokardiografske
parametre nema statistički značajne razlike između podgrupa A i B
(Xi2 test nesignifikantne razlike).
GRAFIKON 5. Kvalitativne ehokardiografske promene kod klinički
suspektnog miokarditisa
DISKUSIJA
Do danas ne postoji takozvani zlatni standard za dijagnozu akutnog
miokarditisa zbog niske specifičnosti i senzitivnosti tradicionalnih
dijagnostičkih testova. Endomikardna biopsija sa patohistološkim
pregledom, imunohistohemijom i prisustvom virusnog genoma jesu
najpouzdanije metode i omogućavaju primenu terapijskog algoritma,
ali je ova invazivna dijagnostika uglavnom rezervisana za teže i
nejasne slučajeve dilatacionih i/ili inflamatornih kardiomiopatija.
Akutni virusni miokarditis je generalno blaga i samoograničavajuća
posledica sistemske infekcije kardiotropnim virusima [41]. Međutim,
pacijenti mogu razviti privremeno ili trajno oštećenje srčane
funkcije, uključujući akutnu kardiomiopatiju sa hemodinamskom
kompromItacijom ili teške aritmije. Akutni fulminatni miokardit je
redak, javlja se prvenstveno u dece kao kardiogeni šok ili edem
pluća a prepoznavanje na vreme spašava život. EF se najčešće se
vraća skoro u normalu ali rezidualna dijastolna disfuncija može da
limitira veće napore kod nekih koji su preležali fulminantni
miokardit [13]. Proporcija dilatacionih kardiomiopatija (DCM) zbog
virusne infekcije ostaje kontraverzna [42]. U najvećoj seriji od
1426 osoba dečijeg uzrasta miokarditis je uzrok DCM u 34% [43].
Precizno predviđanje KV rizika u ranijim fazama miokardita posebno
je važno zbog pravovremene identifikacije visokorizičnih bolesnika
[15].
Najveći broj objavljenih studija retko ima uključene i inicijalne i
follow-up biopsije [44,45,46] i ima samo iznesene inicijalne nalaz
EMB na početku simptoma. Serije bez EMB imaju postavljenu dijagnozu
hroničnog miokardita na osnovu kliničke prezentacije, povišene
inflamatorne markere i imidžing karakterizaciju kod pacijenata sa
normalnom koronarografijom [47]. Predhodne studije procenjuju da se
30% DCM razvija iz miokardita [45,46,48,49].
Pacijenti sa akutnim miokarditisom uobičajeno se prezentuju sa bolom
u grudima, dispenjom ili sa oba simptoma uz tahikardije i disritmije
[1,13,50,51,52]. U nedavnoj seriji od 245 pacijenata sa klinički
sumnjivim miokarditisom, najčešći simptomi su bili umor (82%),
dispneja pri naporu (81%), aritmije (55%, supraventrikularna i
ventrikularna), palpitacije (49%) i bol u grudima u mirovanju (26%)
[53]. Ovo je saglasno sa našim rezultatima, gde su aritmije i
palitacije dominirale u 84%, dok je bol u grudima bio duplo češći
(66%). Virusni prodrom groznice, mijalgije i respiratornih simptoma
javlja se u između 20% i 80% slučajeva, pacijent može lako
propustiti da prijavi prodrome, pa se na to ne može osloniti u
dijagnozi.
Od naših 126 slučajeva klinički suspektnog miokardita većina je
imala neke elektropatološke EKG promene-112/126 (89%), a sa
normalnim EKG je bilo 14/126 (11%) te on ne može da posluži za
isključenje miokardita. Ipak kod ovih 14 pacijenata su postojale
ehokardiografske promene I kriterijumi kliničke prezentacije.
Disritmije nemaju specifičnost za miokardit, dok EKG znaci oštećenja
miokarda depresija ili elevacija ST, blok leve grane Hisovog snopa
govore u prilog lezije miokarda ali ne ukazuju na uzrok. Procena
senzitivnosti EKG za miokarditis na oko 47%, dok je specifičnost
vrlo niska [52]. Troponin na primer ima još nižu senzitivnost za
miokarditis 34% ali dobru specifičnost preko 89% [52].
Analizom parametara merenih transtorakalnom ehokardiografijom u
kriterijumima za klinički suspektan miokarditis dominirala je
dijastolna disfunkcija leve komore, koju reprezentuje odnos
E/e´prim≥9 u 39/126 (31%), od toga je 17 (14%) pacijenata, oko
polovine imalo težu dijastolnu disfunkciju gradus III (E/e´prim ≥14
). U jednoj seriji od 147 patienta sa jako redukovanom EF (23 ± 8%),
dijastolnu disfunkciju je imalo 42%, ali su to bili teži bolesnici
sa inflamatornom kardiomiopatijom. Poboljšanje dijastolne funkcije u
58% tih pacijenata posle lečenja i praćenja oko 6 meseci je
prognostički važno, isto kao i poboljšanje EF i nosi rastuću
prognostičku vrednost za stratifikaciju rizika [54]. Globalna
sistolna disfunkcija leve komore (EF<50%) nađena je kod samo
19/126(15%) naših pacijenata i kod svih je bila prisutna blaga
dilatacija leve komore i kriterijumi za inflamatornu
kardiomiopatiju. Značajno je veći broj bolesnika sa sistolnom
disfunkcijom u italijanskoj studiji kod biopsijom dokazanom
miokarditu u seriji od 41 pts [55], gde je sistolna difunkcija leve
komore bila prisutna u 69% a regionalni poremećaji u kontraktilnostu
u 64%, hipertrofija leve komore zbog edema miokarda u 20%, promene u
teksturi miokarda 23% , ventrikularnu tromb u 15% i restriktivni
patern punjenja leve komore u 7%. Većina naših pacijenata je imala
normalnu ejekcionu frakciju njih 107 pts ili 85%, što je važan
prognostički faktor u većini relevantnih studija [56,57,58]. U
registru jednog nemačkog centra na 210 EMB-dokazanih miokardita 50%
ili tri puta više nego u našim rezulattima je imalo sniženu
ejekcionu frakciju, zbog kliničkog spektra teških bolesnika sa
miokarditom koji se šalju na EMB. Posle dvogodišneg praćenja i
lečenja standardnom terapijom za srčanu insuficijenciju, 26% je
normalizovalo EF a 27% je ostalo sa sniženom EF [59]. Studija Grun
S. i saradnika [56] sa serijom od 222 konsekutivna pts sa EMB
dokazanim virusnim miokarditom, iznosi mortalitet od 19% sa
medijanom 4,7 godina. Generalno oko 1/4 bolesnika sa EMB dokazanim
virusnim miokarditom razvija se u pravcu pogoršanja srčane funkcije
i budu podvrgnuti transplantaciji srca ili egzitiraju. [15].
Prediktori ishoda variraju u raznim studijama sa EMB: Perzistencija
NYHA klase III do IV, dilatacija leve pretkomore i poboljšanje EF
unutar 6 meseci jesu nezavisni prediktori dugoročnog ishoda [42].
Kinderman I i saradnici iznose da visoka NYHA klasa, imunološki
znaci inflamacije i nedostatak betablokatora u terapiji jesu
prediktori lošeg ishoda a ne histološke karakateristike Dallas
kriterijuma ili prisustvo virusnog genoma [10]Regionalna sistolna disfunkcija po našim istraživanima bila je
utvrđena u 21/126 (17%) i u ovim slučajevima mora se isključiti
cicatrix posle asimptomatskog infarkta stres ehokardiografskim
testom farmakološkim ili fizičkim opterećenjem a u inkonkluzivnim
slučajevima MSCT ili invazivnom koronarografijom [60].
Ehokardiografija je odličan alat za dijagnozu i praćenje pacijenata
sa miokarditom i DCM. Speckle tracking echokardiografija (slika
deformacije miokarda) ima sve veči značaj u ranim stadijumima
miokardita i detekciji progresije u kardiomiopatiju [50].
Promena vrste virusa izazivača miokardita je u skladu sa drugim
studijama [7,8,11,12], dok jedna od ređih novijih studija iz
Bugarske nalazi na serološku dominaciju Koksaki virusa kao mogućeg
izazivača miokardita [61]. Jasna dinamika titra IgM je zabeležena
kod malog broja pacijenata u 23/126 (18%) osoba sa dominacijom Parvo
B19 antitela a pad titra uz rast IgG titra (serokonverzija) u 13/126
(10%) bolesnika. Povećanje dinamika titra cirkulišućih antivirusnih
antitela od akutne ka subakutnoj i hroničnoj fazi može da potpomogne
Dg virusnog miokardita sa mogućim spontanim oporavkom [13].
Senzitivnost antivirusnih antitela je niska i procenjena na osnovu
više studija na 25-32% a specifičnost na 40% [52]. To govori za
aktivni proces infekcije bilo gde u organizmu i ima doprinos mogućoj
kauzalnoj dijagnozi samo uz jake dokaze zahvaćenosti miokarda putem
važećih ESC kriterijuma za klinički suspektan miokarditis. U
najznačajnijoj studiji na ovu temu, Mahfoud F. i saradnici [26] su
ispitivali serologija virusa i upoređivali je sa nalazom PCR putem
endomikardne biopsije sa histološkim i imunohistohemijskim nalazom
kod 124 pacijenta starosti 40 ± 15 godina sa sumnjom na miokarditis.
Virusni genom je detektovan u miokardu lančanom reakcijom
polimeraze. Akutnu virusnu infekciju kardiotropnim virusima
dijagnostikovali su putem IgM u početnom uzorku ili serokonverzija
IgG u narednom uzorku. Imunohistohemijski znaci upale bili su
prisutni kod 54 pacijenta. Virusni genom je otkriven u miokardu 58
pacijenata (47%). Kod 20 pacijenata (16%), akutna virusna infekcija
dijagnostikovana je serologijom, što je u skladu sa našim rezultatom
od 18%. Ali samo kod 5 od 124 pacijenta (4%) postojali su serološki
dokazi o infekciji istim virusom koju je otkrila EMB. Senzitivnost
serologije virusa bila je samo 9% a specifičnost 77%. Nedostatak
korelacije između serologije i EMB je dokaz protiv rutinske upotrebe
virusne serologije kod svih pacijenata sa klinički suspektnim
miokarditom. Senzitivnost virusne serologije je jako niska u odnosu
na EKG i ehokardiografiju, a specifičnost umerena, te istu ne treba
koristiti rutinski u evaluaciji miokardita, već u selekcionisanim
slučajevima uz ESC kriterijume gde se ne radi CMR i EMB. Iz
kliničkog iskustva se zna da je teško neke pacijente razuveriti da
nemaju "Koksaki virus u srcu". Psihičko opterećenje pacijenata i
vezivanja za "Koksaki bolest " za koji su ubeđeni da ga nose više
godina samo na osnovu povećanih serumskih IgG antivirusnih antitela
je kontraproduktivno sa socijalnomedicinskog stanovišta. Antisrčana
antitela (AHA) nemaju ustanovljenu ulogu, jer se javljaju i u drugim
bolestima (CAD, genetske CMP) a senzitivnost je slična kao i kod
virusne serologije 25-30% i specifičnost oko 40% [52]. Međutim i
sami patohistološki Dallas krititerijumi [52] bez imunohistologije i
PCR imaju slabu senzitivnost 35 do 50% i dobru specifičnost 78 do
89%. Dopunjeni imunohistohemijom i PCR identifikacijom genoma virusa
senzitivnost je zadovoljavajuća 65% do 70% a specifičnost 80 -100%.
Nažalost čak i EMB ima lažno negativne nalaze, zavisno odakle su
uzimani uzorci i da li je tehnički uzeto dovoljno tkiva.
Komparacijom grupe A i grupe B nije nađena statistički značajna
razlika u ehokardiografskim parametrima, što znači da IgM antitela i
serokonverzija ne ukazuju na teže forme miokardita. Nema do sada
studija o ovom aspektu.
Cela grupa G klinički suspektnog miokardita u odnosu na kontrolnu
grupu C ima stistički visoko značajno redukovane parametre globalne
sistolne (EF=59,1±7,6 vs. 63±7,9; p<0,001) i longitudinalne sistolne
funkcije (S´=6,9±1,3 vs 9,9± 2,1) što upućuje da ove suptilne
promene mogu u svakodnevnoj kliničkoj praksi da nas navedu da
mislimo na miokarditis. U individulanoj distrubuciji sistolna
disfuncija je upola manje zastupljena od dijastolne (15% Vs 31%).
Dijastolna disfunkcija, uprkos kompleksnosti procene je još
izraženije snižena u odnosu na kontrolnu grupu C, kada posmatramo
najreprezentativniji parametar E/e´ (E/e´11,9±4,8 vs. 8,7±4,6;
p<0,001). Dilatacija leve pretkomore i leve komore su visoko
značajno povećanih srednjih vrednosti u odnosu na kontrolnu grupu.
Masa miokarda i indeks mase miokarda su moguće merilo edema miokarda
kod miokardita i značano su većih srednjih vrednosti u ispitivanoj
grupi vs. kontrolna grupa (121,8±28,5 g/m² vs. 98,1±20.2, p<0,001)
što je važno za postavljanje radne dijagnoze klinički suspektnog
miokardita, praćenje toka bolesti i efekta lečenja. Sve
ehokardiografske promene su, bez patognomoničnosti i specifičnosti
za miokardit, ali imaju dobru dijagnostičku senzitivnost. Sposobnost
ehokardiografskih parametara za predviđanje razvoja manifestne
srčane insuficijencije mortaliteta i neželjenih KV događaja u
populaciji inflamatorne kardiomiopatije je dokazana je u malom broju
studija. Kod bolesnika sa klinički suspektnim miokarditom koji još
nisu započeli lečenje srčane insuficijecije i/ili aritmija,
potvrđena je povezanost i ejekcione frakcije i dijastolne
disfunkcije sa KV mortalitetom [62,63,64]. Paradoksalno u skorašnjoj
meta-analizi Chen-a WH. i sradnika prisustvo virusnog genoma ne
pogoršava dugotrajnu prognozu pacijenata sa miokarditsom ili
inflamatornom kardiomiopatijom. Ipak virus-pozitivni pacijenti koji
nisu bili pod specifičnim antivirusnim tretmanom imaju lošiju
prognozu od virus negativnih. Znači da rana dijagnoza prisustva
virusne infekcije miokarda poboljšava prognozu pacijenata [64].
U ovom našem ispitivanju nismo imali konzistentne podatke o vrednost
parametara kardijalnih biomarkera Troponina I i T kao i NT-pro BNP,
što je objektivni nedostatak ove studije. Takodje tada nismo
rutinski radili volumen indeks leve pretkomore (LAVI) koji je bolji
pokazatelj dijatolne funkcije od dimenzije leve pretkomore.
Ehokardiografija putem deformacije miokarda spekl-treking
tehnologijom (myocardial strain) će dati jači eho alat u evaluaciji
klinički suspektnog miokarditisa.
ZAKLJUČAK
Dijagnoza akutnih virusnih miokardita nije laka i postavlja se na
osnovu kriterijuma za klinički suspektan miokarditis Evropskog
udruženja kardiologa (ESC) koji uključuju kliničke prezentacije i 4
različite dijagnostičke kategorije, sa dominantnom ulogom EKG i
ehokardiografije u svakodnevnoj kliničkoj praksi uz obavezno
isključenje drugih kardiovaskularnih bolesti. Cela grupa klinički
suspektnog miokarditisa G imala je visoko stistički značajno niže
parametre sistolne i dijastolne funkcije u odnosu na kontrolnu grupu
C. Dominirala je dijastolna disfunkcija leve komore u 31% gde je 17
pacijenata imalo težu dijastolnu disfunkciju gradus III i klinički
srčanu insuficijenciju sa očuvanom ejekcionom frakcijom. Regionalna
sistolna disfunkcija utvrđena je u 17% a globalna sistolna
disfunkcija leve komore (EF<50%) kod 15% sa dilatacijom leve komore
i kriterijumima za inflamatornu kardiomiopatiju. Promene u teksturi
miokarda- hiperehogene zone miokarda i znaci fibroze-cicatrixu bili
su prisutni u 13% ispitanika. te visoko značajno povećanje
teledijastolne dimenzije leve komore, indeksa mase miokarda i
dimenzije leve pretkomore Normalan ehokardiografski nalaz je imalo
24 (19%) pacijenta ali uz kliničke i EKG kriterijume za miokarditis.
Ipak 81% pacijenata imalo je neku od ehokardiografskih patoloških
promena, koje su specifičnije za dijagnozu od EKG promena. Normalan
EKG i ehokardiografski nalaz ne mogu da služe za isključenje
dijagnoze miokardita. Komparacijom podgrupa sa prisustvom dinamike
titra antivirusnih IgM antitela (A) i bez iste (B) nije nađena
statistički značajna razlika u ehokardiografskim parametrima.
Senzitivnost IgM titra na kardiotropne viruse je jako niska i ne
treba je koristiti u rutinskoj dijagnozi miokardita.
LITERATURA:
- Ammirati E, Cipriani M, Moro C, Raineri C, Pini D, Sormani P, et
al. Registro Lombardo delle Miocarditi. Clinical presentation and
outcome in a contemporary cohort of patients with acute myocarditis:
multicenter lombardy registry.Circulation. 2018; 138(11):1088–1099.
doi:10.1161/CIRCULATIONAHA.118.035319
- Hosenpud JD, McAnulty JH, Niles NR. Unexpected myocardial disease
in patients with life threatening ar-rhythmias. Br Heat J
1986;56(1):55-61. doi: 10.1136/hrt.56.1.55.
- Felker GM, Thompson RE, Hare JM, Hruban RH, Clemetson DE, Howard
DL, et al. Underlying causes and long-term survival in patients with
initially unexplained cardiomiopathy. N Engl J Med
2000;342(15):1077-84. doi: 10.1056/NEJM200004133421502.
- Maron BJ, Udelson JE, Bonow RO et al : Eligibility and
Disqualification Recommendations for Competitive Athletes With
Cardiovascular Abnormalities: Task Force 3: Hypertrophic
Cardiomyopathy, Arrhythmogenic Right Ventricular Cardiomyopathy and
Other Cardiomyopathies, and Myocarditis. Circulation
2015;132(22):e273-80. doi: 10.1161/CIR.0000000000000239.
- Harmon KG, Asif IM, Meleshewski JJ et al. Incidence and etiology
of sudden cardiac arrest and death in High school Athletes in the
United States. Mayo Clin Proc. 2016;91(11):1493-1502. doi:
10.1016/j.mayocp.2016.07.021. Epub 2016 Sep 28.
- Chandra N, Bastiaenen R, Papadakis M, Sharma S: Sudden cardiac
death in young athletes: Practical challenges and diagnostic
dilemmas. J Am Coll Cardiol. 2013;61(10):1027 2013. doi:
10.1016/j.jacc.2012.08.1032.
- Dennert R, Crijns HJ, Heymans S. Acute viral myocarditis Eur
Heart J. 2008;29(17):2073-20 82. doi: 10.1093/eurheartj/ehn296. Epub
2008 Jul 9
- Global Burden of Disease Study C. Global, regional, and national
incidence, prevalence, and years lived with disability for 301 acute
and chronic diseases and injuries in 188 countries, 1990-2013: a
systematic analysis for the global burden of disease study
2013.Lancet. 2015; 386(9995):743–800. doi:
10.1016/S0140-6736(15)60692-4
- Leone O, Veinot JP, Angelini A, Baandrup UT, Basso C, Berry G. at
al. 2011 Consensus statement on endomyocardial biopsy from the
Association for European Cardiovascular Pathology and the Society
for Cardiovascular Pathology. Cardiovasc Pathol 2012;21(4):245–74.
doi:10.1016/j.carpath.2011.10.001. Epub 2011 Dec 3.
- Kindermann I, Barth C, Mahfoud F, Ukena C, Lenski M, Yilmaz A.
at al. Update on myocarditis. J Am Coll Cardiol 2012;59(9):779–92.
doi: 10.1016/j.jacc.2011.09.074.
- Caforio ALP, Pankuweit S, Arbustini E, Basso C, Gimeno-Blanes J,
et al. Current state of knowledge on aetiology, diagnosis,
management, and therapy of myocarditis: a position statement of the
European Society of Cardiology Working Group on Myocardial and
Pericardial Diseases. Eur Heart J 2013;34(33):2636–48. 2648a-2648d.
doi: 10.1093/eurheartj/eht210. Epub 2013 Jul 3.
- Ammirati E, Frigerio M, Adler ED, Basso C, Birnie DH, Brambatti
M, at al. Management of Acute Myocarditis and Chronic Inflammatory
Cardiomyopathy: An Expert Consensus Document. Circ Heart Fail.
2020;13(11):e007405. doi:10.1161/CIRCHEARTFAILURE.120.007405. Epub
2020 Nov 12.
- Lakdawala NK, Stevenson LW and Loscalozo J. cardiomyopathy and
myocarditis. IN: Jameson JL, Kasper DL, Lomgo DL, Fauci AS, Hauser
SL, Loscalozo J, editors. Harrisson´s Principles of Internal
Medicine 20.th ed. New York: McGraw Hill; 2018.p. 1779-1797.
- Richardson P, Mc Kenna W, Bristow M, et al. Report of the 1995
World Health Ogranization/International Society and Federation of
Cardiology Task Force on the Definition and Classification of
cardiomyopathies. Circulation. 1996;93(5):841-2. doi:
10.1161/01.cir.93.5.841.
- Arbustini E, Agozzino M, Favalli V and Narula J. Myocarditis.
IN: Valentin Fuster, Robert A. Harrington, Jagat narula, Zubin J.
Eapen, editors. HURST´S The HEART14th ed. New York: McGraw Hill;
2017.p. 1528-1560.
- Raukar NP,Cooper LT. Implications of SARS-CoV-2-Associated
Myocarditis in the Medical Evaluation of Athletes.Sports Health.
2021;13(2):145-148. doi: 10.1177/1941738120974747. Epub 2020 Nov 17.
- Bhatia HS, Bui QM, King K, DeMaria A, Daniels LB. Subclinical
left ventricular dysfunction in COVID-19. Int J Cardiol Heart Vasc,
2021;34:100770. doi: 10.1016/j.ijcha.2021.100770. Epub 2021 Mar 24.
- Rathore SS, Rojas GA, Sondhi M, Pothuru S, Pydi R, Kancherla N.
et al. Myocarditis associated with Covid-19 disease: A systematic
review of published case reports and case series. Int J Clin Pract.
2021;e14470. doi: 10.1111/ijcp.14470.
- Ozieranski K, Tyminska A, Jonik S, Marcolongo R, Baritussio A,
Grabowski M.et al . Clinically Suspected Myocarditis in the Course
of Severe Acute Respiratory Syndrome Novel Coronavirus-2 Infection:
Fact or Fiction? J Card Fail . 2021;27(1):92-96. doi:
10.1016/j.cardfail.2020.11.002. Epub 2020 Nov 6.
- Sala S, Peretto G, Gramegna M, Palmisano A, Villatore A, Vignale
D. ET AL. Acute myocarditis presenting as a reverse Tako-Tsubo
syndrome in a patient with SARS-CoV-2 respiratory infection. Eur
Heart J. 2020;41(19):1861-1862. doi: 10.1093/eurheartj/ehaa286.
- Leslie T Cooper and Kirk U. Knowlton, MYOCARDITIS IN: IN:Zipes
DP, Libby P, Bonow RO, Mann DL, Tomaselli GF, Braunwald E.
BRAUNWALD’S HEART DISEASE: A TEXTBOOK OF CARDIOVASCULAR MEDICINE
11th ed. Philadelphia: Elsevier; 2019 p 1617-1630.
- Sanguineti F, Garot P, Mana M, et al. Cardiovascular magnetic
resonance predictors of clinical outcome in patients with suspected
acute myocarditis. J Cardiovasc Magn Reson. 2015;17(1):78. doi:
10.1186/s12968-015-0185-2.
- Teele SA, Allan CK, Laussen PC, et al.: Management and outcomes
in pediatric patients presenting with acute fulminant myocarditis. J
Pediatr. 2011;158(4):638-643.e1. doi: 10.1016/j.jpeds.2010.10.015.
- Mlczoch E, Darbandi-Mesri F, Luckner D, Salzer-Muhar U: NT-pro
BNP in acute childhood myocarditis. J Pediatr. 2012; 160(1):178-9.
doi: 10.1016/j.jpeds.2011.08.065.
- Caforio AL, Tona F, Bottaro S, et al.: Clinical implications of
anti-heart autoantibodies in myocarditis and dilated cardiomyopathy.
Autoimmunity. 2008;41(1):35-45. doi: 10.1080/08916930701619235.
- Mahfoud F, Gartner B, Kindermann M, et al.: Virus serology in
patients with suspected myocarditis: Utility or futility?. Eur Heart
J. 2011;32(7):897-903. doi: 10.1093/eurheartj/ehq493.
- Marwick TH, De Maria AN, Blanchard DG and Zoghbi WA.
Echocardiography, Dilated cardiomyopathy. IN: Fuster V, Harrington
RA, Narula J, Eapen ZJ, editors. HURST´S The HEART14th ed. New York:
McGraw Hill; 2017.p. 353-432.
- Vojkan Čvorović i Ivan Stanković. Transezofagijalna
ehokardiografija IN: Ivan Stanković, Aleksandar N. Nešković, Zorica
Mladenović editors. Klinička ehokardiografija 1th ed. Beograd:
ECHOS; 2021. p.477-490.
- Escher F, Kasner M, Kühl U, Heymer J, Wilkenshoff U, Tschöpe C,
Schultheiss HP. New echocardiographic findings correlate with
intramyocardial inflammation in endomyocardial biopsies of patients
with acute myocarditis and inflammatory cardiomyopathy. Mediators
Inflamm. 2013;2013:875420. doi: 10.1155/2013/875420. Epub 2013 Mar
20.
- Kasner M, Aleksandrov A, Escher F, Al-Saadi N, Makowski M,
Spillmann F, at al. Multimodality imaging approach in the diagnosis
of chronic myocarditis with preserved left ventricular ejection
fraction (MCpEF): The role of 2D speckle-tracking echocardiography.
Int J Cardiol. 2017;243:374-378. doi: 10.1016/j.ijcard.2017.05.038.
- Caspar T, Fichot M, Ohana M, El Ghannudi S, Morel O, Ohlmann P.
Late Detection of Left Ventricular Dysfunction Using Two-Dimensional
and Three-Dimensional Speckle-Tracking Echocardiography in Patients
with History of Nonsevere Acute Myocarditis. J Am Soc Echocardiogr.
2017;30(8):756-762. doi: 10.1016/j.echo.2017.04.002. Epub 2017 Jun
7.
- Uziębło-Życzkowska B, Mielniczuk M, Ryczek R, Krzesiński P.
Myocarditis successfully diagnosed and controlled with speckle
tracking echocardiography. Cardiovasc Ultrasound. 2020;18(1):19.
doi: 10.1186/s12947-020-00203-4.
- Trifunović-Zamaklar D, Gordana Krljanac. Analiza deformacije
miokarda. IN: Ivan Stanković, Aleksandar N. Nešković, Zorica
Mladenović editors. Klinička ehokardiografija 1th ed. Beograd:
ECHOS; 2021. p.421-436.
- Aquaro GD, Perfetti M, Camastra G, Monti L, Dellegrottaglie S,
Moro C, at al. Cardiac MR with late gadolinium enhancement in acute
myocarditis with preserved systolic function: ITAMY study. J Am Coll
Cardiol. 2017; 70(16):1977–1987. doi: 10.1016/j.jacc.2017.08.
- Gräni C, Eichhorn C, Bière L, Murthy VL, Agarwal V, Kaneko K, at
al. Prognostic value of cardiac magnetic resonance tissue
characterization in risk stratifying patients with suspected
myocarditis. J Am Coll Cardiol. 2017;70(16):1964–1976. doi:
10.1016/j.jacc.2017.08.050.
- Frustaci A, Russo MA, chimenti C. Randomized study on the
efficacy of immunosupressive therapy in patients with virus-negative
inflammatory cardiomyopathy: the TIMIC study. Eur Heart J.
2009;30(16):1995-2002. doi: 10.1093/eurheartj/ehp249.
- Lang RM, Badano LP, Mor-Avi V, Afilalo J, Armstrong A, Ernande L
et al. Recommendations for cardiac chamber quantification by
echocardiography in adults: an update from the American Society of
Echocardiography and the European Association of Cardiovascular
Imaging. Eur Heart J Cardiovasc Imaging 2015;16(3):233–70. doi:
10.1093/ehjci/jev014.
- Nagueh SF, Smiseth OA, Appleton CP, Byrd BF 3rd, Dokainish H,
Edvardsen T et al. Recommendations for the evaluation of left
ventricular diastolic function by echocardiography: an update from
the American Society of Echocardiography and the European
Association of Cardiovascular Imaging. Eur Heart J Cardiovasc
Imaging 2016;17(12):1321–60. oi: 10.1093/ehjci/jew082.
- Mitchell C, Rahko PS, Blauwet LA et al. Guidelines for
Performing a Comprehensive Transthoracic Echocardiographic
Examination in Adults: Recommendations from the American Society of
Echocardiography . 2019;32(1):1-64. doi: 10.1016/j.echo.2018.06.004.
Epub 2018 Oct 1.
- Dušan Bastać, Radosava Cvjetan i Angelina Stevanović. Izvođenje
ehokardiografskog pregleda. IN: Ivan Stanković, Aleksandar N.
Nešković, Zorica Mladenović editors. Klinička ehokardiografija 1th
ed. Beograd: ECHOS; 2021. p.23-40.
- Tschöpe C, Cooper LT, Torre-Amione G, Linthout S. Management of
Myocarditis-Related Cardiomyopathy in Adults. Circulation Research.
2019;124(11):1568–1583. doi: 10.1161/CIRCRESAHA.118.313578.
- Kindermann I, Kindermann M, Kandolf R, et al.:Predictors of
outcome in patients with suspected myocarditis. Circulation
2008:118(6):639-48.. doi: 10.1161/CIRCULATIONAHA.108.769489.
- Towbin JLA, Colan S. et al. Incidence, causes and outcome of
dilated cardiomyopathy in children. JAMA. 2006;296(15):1867-1876.
doi: 10.1001/jama.296.15.1867.
- Schultheiss HP, Piper C, Sowade O, et al. Betaferon in chronic
viral cardiomyopathy (BICC) trial: Effects of interferon-β treatment
in patients with chronic viral cardiomyopthy. Clin Res Cardiol.2016;105(9):763-73. doi: 10.1007/s00392-016-0986-9.
- Kuhl U, Paushchinger M, Seeberg B, et al. Viral persistence in
the myocardium is associated with progressive cardiac dysfunction.
Circulation. 2005;112(13):1965-1970. doi:
10.1161/CIRCULATIONAHA.105.548156.
- Kuhl U, Lassner D, von Schlippenback J, et al. Interferon-Beta
improves survival in enterovirus-associated cardiomyopathy. J Am
Coll Cardiol. 2012;60(14):1295-1296. doi:
10.1016/j.jacc.2012.06.026.
- Cihakova D, Rose NR. Pathogenesis of myocarditis and dilated
cardiomyopathy. Adv Immunol. 2008;99:95-114. doi:
10.1016/S0065-2776(08)00604-4.
- Anzini M, Merlo M, Sabbadini G, et al. Long-term evolution and
prognostic stratification of biopsy-proven active
myocarditis.Circulation. 2013;128(22):2384-94. doi:
10.1161/CIRCULATIONAHA.113.003092.
- Caforio A, Calabrese F, Angelini A, et al. A prospective study
of biopsy-proven myocarditis:prognostic relevance of clinical and
aetipathogenetic features at diagnosis. Eur Heart J.
2007;28(11):1326-33. doi: 10.1093/eurheartj/ehm076.
- Thor Edvardsen : Cardiomyopathies, myocarditis and the
transplanted heart IN John Camm et al. editors. ESC Textbook of
Cardiovascular Medicine, 3rd ed. 2019. p.457-460.
- Lancellotti P, Price S, Edvardsen T, Cosyns B, Neskovic AN,
Dulgheru R, at al. The use of echocardiography in acute
cardiovascular care: recommendations of the European Association of
Cardiovascular Imaging and the Acute Cardiovascular Care
Association. Eur Heart J Cardiovasc Imaging 2015;16(2):119–46. doi:
10.1093/ehjci/jeu210.
- Peter Liu and Kenneth L. Baughman. Myocarditis IN Robert O.
Bonow, Douglas L. Mann Douglas P. Zipes, Peter Libby editors.
BRAUNWALD’S HEART DISEASE: A TEXTBOOK OF CARDIOVASCULAR MEDICINE.
Philadelphia 9.th ed. 2012 p.1595-1610.
- Kuhl U, Pauschinger M, Noutsias M, et al.: High prevalence of
viral genomes and multiple viral infections in the myocardium of
adults with “idiopathic” left ventricular dysfunction. Circulation.
2005;111(7):887-93. doi: 10.1161/01.CIR.0000155616.07901.35.
- Cavalcante JL, Marek J, Sheppard R, Starling RC, Mather PJ,.
Alexis JD at al. Diastolic function improvement is associated with
favourable outcomes in patients with acute non-ischaemic
cardiomyopathy: insights from the multicentre IMAC-2 trial Eur Heart
J Cardiovasc Imaging. 2016;17(9):1027–35. doi: 10.1093/ehjci/jev311.
/
- Pinamonti B, Alberti E, Cigalotto A, Dreas L, Salvi A, Silvestri
F, at al. Echocardiographic findings in myocarditis. Am J Cardiol.
1988;62(4):285-91. doi: 10.1016/0002-9149(88)90226-3.
- Grun S, Schumm J, Greulich s, et al. Long-term follow-up of
biopsy-proven viral myocarditis: predictors of mortality and
incomplete recovery. J am Coll cardiol. 2012;59(18):1604-15. doi:
10.1016/j.jacc.2012.01.007.
- Abbate A, Sinagra G, Bussani R, et al. Apoptosis in patients
with acute myocarditis. Am J Cardiol. 2009;104(7):995-1000. doi:
10.1016/j.amjcard.2009.05.041.
- Kim G, Ban GH, Lee HD, Sung SC, Kim H, Choi KH. Left ventricular
end-diastolic dimension as a predictive factor of outcomes in
children with acute myocarditis. Cardiol Young 2017;27(3):443-451.
doi: 10.1017/S1047951116000706. Epub 2016 May 26.
- McCarthy 3rd RE, Boehmer JP, Hruban RH, Hutchins GM, Kasper EK
at al. Long-term outcome of fulminant myocarditis as compared with
acute (nonfulminant) myocarditis. N Engl J Med 2000;342(10):690-5.
DOI: 10.1056/NEJM200003093421003.
- Pasupathy S, Air T, Dreyer RP, Tavella R, Beltrame JF.
Systematic review of patients presenting with suspected myocardial
infarction and nonobstructive coronary arteries. Circulation. 2015;
131(10):861–70. doi: 10.1161/CIRCULATIONAHA.114.011201.
- Ivanova SK, Angelova SG, Stoyanova AS, Georgieva IL,
Nikolaeva-Glomb LK et al. Serological and Molecular Biological
Studies of Parvovirus B19, Coxsackie B Viruses, and Adenoviruses as
Potential Cardiotropic Viruses in Bulgaria. Folia Med (Plovdiv)
20161;58(4):250-256. doi: 10.1515/folmed-2016-0036
- Younis A, Matetzky S, Mulla W, Masalha E, Afel Y, Chernomordik
F, Fardman A, Goitein O, Ben-Zekry S, Peled Y, et al.. Epidemiology
characteristics and outcome of patients with clinically diagnosed
acute myocarditis.Am J Med. 2020;133(4):492–499. doi:
10.1016/j.amjmed.2019.10.015
- White JA, Hansen R, Abdelhaleem A, Mikami Y, Peng M, Rivest S,
Satriano A, et al.. Natural history of myocardial injury and chamber
remodeling in acute myocarditis.Circ Cardiovasc Imaging.
2019;12(7):e008614. doi: 10.1161/CIRCIMAGING.118.008614.
- Chen WH, Guo YS, Zhang DH and Zhang HJ. Long-Term Prognosis of
Suspected Myocarditis and Cardiomyopathy Associated with Viral
Infection of the Myocardial Tissue: A Meta-Analysis of Cohort
Studies. Cardiovasc Ther. 2019;2019:9342792. doi:
10.1155/2019/9342792.
|
|
|
|









