| |
|
|
UVOD I PREGLED LITERATURE
Sinkopa je prolazni gubitak svesti nastao zbog tranzitorne
globalne hipoperfuzije mozga, koji se karakteriše naglim nastankom,
kratkim trajanjem i spontanim potpunim oporavkom.
Termin sinkopa je ponekad korišćen kao sinonim za prolazni gubitak
svesti, bez uzimanja u obzir uzroka gubitka svesti, što predstavlja
tako široku definiciju koja obuhvata i epileptične napade. Ovakve
nejasnoće se još uvek mogu naći u literaturi [1].
Praveći razliku između prolaznog gubitka svesti i sinkope, izbegava
se moguća konceptualna i dijagnostička zabuna.
Iako se sinkopa definiše kao naglo nastao gubitak svesti, u nekim
oblicima sinkopa može postojati prodromalni period sa različitim
simptomima (preznojavanje, mučnina, poremećaji vida ).
Tipična sinkopa je kratkog trajanja. Ipak, sinkope mogu nekada biti
i dužeg trajanja, čak i do nekoliko minuta, kada je diferencijalna
dijagnoza između sinkope i drugih uzroka gubitka svesti otežana [2].
Za sinkopu je uobičajen spontani potpuni oporavak. Ponekad je period
oporavka posle sinkope praćen iscrpljenošću i retrogradnom
amnezijom, posebno kod starijih osoba [3].
Stanja koja se pogrešno dijagnostikuju kao sinkopa najčešće su
poremećaji sa parcijalnim ili kompletnim gubitkom svesti, ali bez
globalne cerebralne hipoperfuzije: epilepsija, metabolički
poremećaji (hipoglikemija, hipoksija, hiperventilacija sa
hipokapnijom), intoksikacije i tranzitorni vertebrobazilarni
ishemijski atak.
Sinkope se klasifikuju na:
- Refleksne sinkope (neuronalnog porekla),
- Sinkope uzrokovane ortostatskom hipotenzijom,
- Kardijalne (kardiovaskularne) sinkope.
Refleksne sinkope mogu biti vazovagalne, situacione, sinkope
karotidnog sinusa i atipične forme bez vidljivih trigera i/ili sa
atipičnim prezentacijama.
Sinkope uzrokovane ortostatskom hipotenzijom obuhvataju primarni
autonomni poremećaj, sekundarni autonomni poremećaj, lekovima
uzrokovanu ortostatsku hipotenziju i gubitak volumena.
Kardijalne sinkope kao primarni uzrok mogu imati aritmiju
(bradikardiju, tahikardiju), strukurnu bolest srca i druge uzroke
(plućna embolija, disekcija aorte, plućna hipertenzija) [4, 5].
Različiti su patofiziološki mehanizmi koji dovode do pada krvnog
pritiska sa posledičnom cerebralnom hipoperfuzijom kao osnovom
sinkope.
Iznenadni prekid cerebralnog protoka u trajanju od 6-8 sekundi
dovoljan je da izazove potpuni gubitak svesti.
Sistemski krvni pritisak je determinisan srčanim outputom i
perifernom vaskularnom rezistencijom, a pad jednog ili drugog može
izazvati sinkopu. Često je prisutna kombinacija oba mehanizma [6].
Poremećaji srčanog ritma su najčešći kardijalni uzroci sinkope. Oni
uzrokuju hemodinamsku nestabilnost koja može dovesti do kritičnog
smanjenja u srčanom outputu i cerebralnoj perfuziji [7].
Kod intrizične bolesti sinusnog čvora, poremećeno je sino-atrijalno
sprovođenje. U ovom slučaju sinkope se javljaju zbog dugačkih pauza
u srčanom radu, zbog sinusnog aresta ili sino-atrijalnog bloka.
Kao po pravilu, teže stečene forme atrio-ventrikularnog bloka
(Mobitz II, viši stepen, kompletan AV blok) dovode se u blisku vezu
sa sinkopom koja nastaje zbog odloženog uključivanja pomoćnih
pejsmejkera [5, 7].
Sinkopa ili presinkopa se javlja na početku paroksizmalne
tahikardije, pre razvoja vaskularnih kompenzatornih mehanizama.
Svest se obično oporavlja pre terminacije tahikardije. Ukoliko
hemodinamska nestabilnost i dalje traje, kao posledica tahikardije,
gubitak svesti se održava, oporavak svesti tada nije spontan i više
nije u pitanju sinkopa, već srčani zastoj [8].
Neke vrste lekova mogu izazvati bradi i tahiaritmiju i posledično
sinkope. Mnogi antiaritmici indukuju bradikardiju delujući na
sinusni čvor ili AV sprovođenje, a lekovi koji produžavaju QT
interval ne pripadaju samo grupi antiaritmika već su to i
vazodilatatori, psihotropni lekovi i nesedativni antihistaminici.
Strukturne bolesti srca mogu biti u osnovi sinkope kada oštećena
sposobnost srca da poveća output nije u stanju da nadomesti potrebe
cirkulacije [9].
Sinkopa je česta u opštoj populaciji i javlja se u karakterističnom
uzrastu [10]. Postoji visoka prevalenca pojave prve sinkope u
uzrastu od 10-30 godine starosti, sa pikom oko 15. godine života.
Refleksna sinkopa je daleko najčešći uzrok [11]. Incidenca sinkope
ponovo raste posle 70. godine života (Framinghajmska studija) [12].
Sinkopa kao posledica kardiovaskularnih oboljenja je drugi najčešći
uzrok [3]. Ortostatska hipotenzija je česta kod starijih pacijenata
[13].
Prognoza sinkope (odnosno stratifikacija rizika) se razmatra kao
rizik od smrti i po život opasnih događaja, kao i rizik od
ponavljnja sinkope i fizičkih povreda [14]. Strukturna bolest srca i
poremećaj srčanog ritma su glavni faktori za naprasnu srčanu smrt i
ukupni mortalitet kod bolesnika sa sinkopom [15].
Ortostatska hipotenzija, kao uzrok sinkope, povezana je sa dvostruko
većim rizikom od smrti zbog ozbiljnosti komorbiditeta u poređenju sa
opštom populacijom. Nasuprot tome, mlađi pacijenti bez strukturne
bolesti srca i poremećaja srčanog ritma, kod kojih je u pitanju
refleksna sinkopa, imaju dobru prognozu [15, 16].
Inicijalna evaluacija bolesnika sa tranzitornim gubitkom svesti
sastoji se od pažljivo uzete anamneze i heteroanamneze, tj. istorije
bolesti, zatim fizikalnog pregleda i EKG-a.
Na osnovu ovih nalaza može se doneti odluka da se izvrše dopunska
ispitivanja: masaža karotidnog sinusa kod bolesnika starijih od 40
godina, ehokardiografija, EKG monitoring, test ortostaze i/ili
head-up tilt test, neurološko ispitivanje, laboratorijske analize
[17].
Posle inicijalne evaluacije treba odgovoriti na tri ključna pitanja:
da li je u pitanju sinkopa ili ne, da li je poznata etiološka
dijagnoza i postoje li podaci koji ukazuju na visok rizik za neki
kardiovaskularni događaj ili smrtni ishod?
Važna anamnestička pitanja u inicijalnoj evaluaciji sinkope se
odnose na okolnosti koje su prethodile gubitku svesti, u smislu
položaja tela, aktivnosti, predisponirajućih i precipitirajućih
događaja. Takođe su važna pitanja o početku i kraju napada, kao i
heteropodaci o samom napadu. Obavezno pitati o porodičnoj istoriji
iznenadne smrti i učestalosti napada [8].
Inicijalna evaluacija omogućava definisanje uzroka sinkope kod
23-50% slučajeva [4]. Kada uzrok sinkope ostane nepoznat posle
inicijalne evaluacije, potrebno je najpre uraditi procenu rizika za
ozbiljan kardiovaskularni događaj ili iznenadnu smrt na osnovu
kratkoročnih visokorizičnih kriterijuma koji zahtevaju hitnu
hospitalizaciju ili intenzivnu evaluaciju [14].
Kod sumnje na kardijalnu sinkopu, sprovodi se elektrokardiografski
monitoring (neinvazivni i invazivni): holter monitoring,
intrahospitalni telemetrijski monitoring, spoljni i implantabilni
loop recorder (ILR) [9, 19, 20, 21].
Implantabilni loop recorder je mali uređaj, težine 17 grama, koji se
implantira u prednji zid grudnog koša pacijenta. Njegova baterija
ima životni vek do 3 godine. Ovi uređaji imaju loop memoriju koja
omogućava čuvanje retrospektivnih EKG zapisa, u slučaju aktiviranja
od strane samog pacijenta ili posmatrača, obično posle sinkope, ili
automatski, u slučaju predefinisanih aritmija. Automatsko
aktiviranje je obično programirano za pauze u ventrikularnom ritmu
duže od 3 sekunde i ventrikularni ritam niži od 40/min ili viši od
165/min za više od 16 otkucaja. EKG snimci su sačuvani za kasniju
procenu i traženje korelacije između sinkopalnih događaja i aritmije
[20, 21].
Zlatni standard za dijagnostikovanje sinkope izazvane aritmijom je
registrovanje povezanosti između simptoma i dokumentovane aritmije.
Prema vodiču za dijagnostiku i lečenje sinkope Evropskog udruženja
kardiologa ( ESC ) iz 2009. godine, preporučene su indikacije za
upotrebu ILR-a u proceni sinkope (klasa 1, nivo dokaza B):
- u ranoj fazi evaluacije pacijenata sa ponavljanim sinkopama
nepoznatog porekla, koji nemaju procenjen visok rizik za ozbiljan
kardiovaskularni događaj ili iznenadnu smrt, ali imaju visoku
verovatnoću od ponavljanja epizode sinkope tokom trajanja rada
baterije ILR-a (do 3 godine);
- kod pacijenata sa procenjenim visokim rizikom od iznenadne smrti i
po život opasnih događaja, čija početna procena, uključujući
elektrofiziološku evaluaciju, nije identifikovala uzrok sinkope
[22].
Indikacije za ugradnju ILR-a u proceni sinkope (klasa 2A, nivo
dokaza B) su :
- u proceni uloge bradikardije u pacijenata sa poznatom ili
suspektnom refleksnom sinkopom pre razmatranja ugradnje pejsmejkera
[22].
Pored neobjašnjenih sinkopa ispitivana je uloga ILR-a i kod
bolesnika kod kojih postoji sumnja na epilepsiju, ali je terapija
ostala bez efekta kao i kod starijih pacijenata sa neobjašnjenim
padovima [22]. Diferencijalna dijagnoza sinkope u odnosu na
epilepsiju u nekim slučajevima može biti teška. U toku najvećeg
broja epileptičnih napada dolazi do tranzitornog gubitka svesti.
Sinkope su obično provocirane, dok epileptični napadi najčešće nisu.
Izuzetak su refleksne epilepsije. Pažljivim uzimanjem anamneze
obično je moguće razlikovati auru epileptičnog napada od
presinkopalnih senzacija [23, 24].
Tokom samog gubitka svesti potpuna relaksacija muskulature obično ne
govori u prilog epilepsiji. Jedini izuzetak su atonični napadi, koji
se javljaju retko i obično bez provokacije kod dece sa već
postojećim neurološkim smetnjama.
Pokreti tela mogu biti prisutni i kod epilepsije i kod sinkope. Kod
epilepsije su prisutni tonično-klonični pokreti, klonizmi ili
automatizmi, koji traju do nekoliko minuta, dok su kod sinkope
tonično-klonični pokreti prisutni retko i traju nekoliko sekundi
(manje od 15 sekundi). Trzaji tela kod epilepsije su grubi, ritmični
i obično sinhronizovani, dok su oni kod sinkope manjeg obima,
aritmični i asinhroni. Ugriz jezika i cijanoza tokom gubitka svesti
pre upućuju na epilepsiju, ali nisu isključeni ni kod sinkope.
Urinarna inkontinencija se javlja u oba slučaja.
Pacijenti mogu biti zbunjeni i dezorjentisani duže vremena posle
epileptičnog napada, dok je kod sinkope osvešćivanje trenutno.
Glavobolja, bol u mišićima, visok nivo kreatin kinaze i prolaktina
su češći posle epileptičnog napada [4].
Radi razlikovanja epileptičnog napada od sinkope, pored detaljne
anamneze i heteroanamneze, potrebno je uraditi neurološki pregled i
elektroencefalografiju (EEG). EEG nalaz je normalan između dva
napada sinkope. Normalan interiktalni EEG ne može isključiti
epilepsiju, mora uvek biti interpretiran u kliničkom kontekstu [25].
EEG nije neophodan ako je sinkopa najverovatniji uzrok tranzitornog
gubitka svesti, ali jeste kada je epilepsija verovatni uzrok ili
kada klinički nije jasno kom se entitetu radi. EEG se takođe koristi
u dijagnostici psihogene pseudosinkope, ukoliko se snima tokom
provociranog napada [26].
CT, MR i dopler ultrazvučni pregled krvnih sudova vrata i mozga mogu
biti od značaja za neurološku evaluaciju nejasnih slučajeva.
Osnovni cilj lečenja bolesnika sa sinkopom je produženje životnog
veka, smanjivanje mogućnosti povređivanja i prevencija ponavljanja
sinkopa. Značaj i prioritet ovih različitih ciljeva zavise od uzroka
sinkope.
Terapijske mere su u direktnoj vezi sa uzrokom sinkope i
stratifikacijom rizika. Sinkope uzrokovane srčanim aritmijama se
moraju lečiti kauzalnom terapijom: pejsmejker terapijom, kateterskom
ablacijom, antiaritmicima i implantabilnim kardioverter
defibrilatorom (ICD) [27]. Postoje bolesnici kod kojih je tačan
mehanizam sinkope nepoznat ili nesiguran i na kraju kompletne
evaluacije. Kod ovih bolesnika primarni cilj lečenja je redukcija
rizika za smrtni ishod [28].
PRIKAZ SLUČAJA
Mi predstavljamo slučaj bolesnice stare 22 godine, koja je treće
dete zdravih roditelja, trudnoća majke uredna, porođaj u terminu,
prirodnim putem bez komplikacija, telesna težina na rođenju 3150 gr.
Rani psihomotorni razvoj protekao uredno. Nije značajnije bolovala.
U porodici nema bolesti od značaja za neurološki i kardiološki
hereditet.
Prve tegobe su se javile 2006. godine, u 14. godini života. Osetila
je „lupanje srca”, vrtoglavicu, „tačkice pred očima”, izgubila
svest, nema heteropodataka, nije se javljala lekaru.
Posle oko godinu dana, 2007. godine, posle časova u školi osetila da
joj nije dobro, imala je zamagljen vid, sela, kada se osvestila
ležala je na podu, nije bilo očevidaca. Sutradan, posle buđenja
predosetila da će se onesvestiti, vrisnula je i više se ne seća
ničeg. Majka ju je u sledećem trenutku zatekla kako sedi u krvetu.
Neposredno potom, tokom pregleda u Domu zdravlja, imala je dve
epizode tokom kojih je prevrnula očima, ukočila se i imala trzaje
ekstremiteta. Dobila je diazepam i.v. i transportovana je na dečije
odeljenje bolnice u Valjevu. Urađen joj je CTC koji je opisan kao
uredan. Tokom boravka na odeljenju iznenada je kriknula, izgubila
svest, imala klonizme, bila je ekstremno bleda. Registrovana je
tahikardija od 300/min (bila je na monitoru), potom je nastupio
srčani zastoj, reanimirana je, posle oko 90 sec. uspostavljen je
sinusni ritam od 70/min.
Transportovana je u Institut za majku i dete u Beogradu. Po prijemu
u jedinicu intenzivne nege, započeto je kontinuirano praćenje
vitalnih funkcija. Istog dana po prijemu registrovan je iregularni
srčani ritam, polimorfne ventrikularne ekstrasistole na monitoru,
potom klinički prestanak srčane radnje, reanimirana je, odmah je
započeta intravenska terapija amiodaronom, koji se tokom boravka
postepeno prevodi na peroralnu primenu uz uvođenje malih doza
propranolola.Od momenta uvođenja u terapiju amiodarona napadi se
više nisu javljali.
Tokom boravka u Institutu urađeno je sledeće: laboratorijske
analize, FOU, u više navrata EKG, 24-satni holter EKG monitoring,
radiografija srca i pluća, ehokardiografija, EEG u dva navrata (oba
puta iznad centralnih regiona leve hemisfere registrovani su retki
solitarni šiljci i oštri talasi).
U zaključku na otpustu sa Instituta je konstatovano da su na osnovu
anamnestičkih podataka, opisa napada, uzrasta deteta i registrovanog
srčanog zastoja sa ozbiljnom aritmijom diferencijalno dijagnostički
dolazile u obzir epilepsija, Long QT sindrom, tumor u pretkomorama,
akutni miokarditis ili aritmogena displazija desne komore (ADDK).
Sprovedenim programom ispitivanja isključene su sve prethodno
pomenute dijagnoze, osim aritmogene displazije desne komore.
Ultrazvučnim pregledom je registrovana hipertrabekularna desna
komora apikalno 3cm pregrađena dubokim recesusima i postavljena je
radna dijagnoza ADDK. Preporučena je terapija amiodaron tabletama od
200mg, 1 dnevno i inderal tabletama od 40mg, polovina ujutru, cela
uveče. Data je preporuka za MR srca, kontrolni EKG holter monitoring
i eventualnu biopsiju srca. Zabranjena joj je fizička aktivnost.
Naredne godine uz amiodaron je u terapiju umesto inderala uveden
sotalol u dozi od 3x40mg. Na navedenoj terapiji je bila od 2007. do
2012. godine, bez kriza svesti, osim jedne u 2008. godini, koja se
javila kada je samoinicijativno kratkotrajno prekinula uzimanje
lekova. Tokom ovog perioda, u više navrata je hospitalizovana na
Institutu za majku i dete, gde su joj rađeni EKG holter monitorinzi
i nalazi su bili uvek uredni. U dva navrata je radila MR srca i nisu
registrovani znaci za ADDK. U više navrata rađen je EEG u budnom
stanju i u spavanju, nalazi su bili uredni. U aprilu 2012. godine
primljena je u Institut za kardiovaskularne bolesti „Dedinje” radi
elektrofiziološkog ispitivanja srca. Isključena joj je sva terapija.
U jednom aktu je urađen supraventrikularni i ventrikularni program.
Prilikom intervencije bolesnica je osetila malaksalost, vrtoglavicu,
jako „lupanje srca”, imala je osećaj da joj se predmeti približavaju
i udaljavaju, imala je trzaje rukama i nogama, osećala je strah,
svest nije gubila. Ovaj napad nije bio praćen patološkim promenama
na EKG-u. Konsultovan je neurolog koji je iskazao sumnju da se radi
o konverzivnom napadu. Posle 7 dana urađen je kontrolni
ventrikularni program i sve je proteklo bez komplikacija, nalaz je
bio uredan. Otpuštena je sa Dedinja bez antiaritmijske terapije, sa
preporukom za head-up tilt test, pregled neurologa i EEG.
Dva meseca posle ukidanja terapije, imala je krizu svesti istih
osobina kao i ranije. Tada se javila neurologu, koji je uradio
neurološku evaluaciju. Neurološki nalaz je bio uredan. Standardni
EEG i EEG posle deprivacije spavanja nisu beležili patološke
promene. MR endokranijuma je registrovao fokus postishemijske glioze
levo periventrikularno. Uradila je head-up tilt test u KBC
„Bežanijska kosa”. Rađen je test pod uglom od 70 stepeni, po
konzervativnom protokolu. U samom početku testa javila se izražena
tahikardija sa presinkopalnim tegobama, zbog čega je test prekinut.
Hemodinamski odgovor je ukazivao na posturalni tahikardični sindrom
(POTS) i iskazana je sumnja na vazovagalnu sinkopu.
Tokom 2012. godine u tri navrata je imala krize svesti sledećih
osobina: oseti lupanje srca i nedostatak vazduha, izgubi svest,
pomodri, nekada ima grčeve ekstremiteta, umokri se, posle napada
oseća umor.
Posle svake od ovih kriza rađeno je kardiološko ispitivanje, nalazi
uredni, kardiolozi isključuju kardiološki uzrok gubitaka svesti.
Krajem juna 2012. godine u terapiju je uveden valproat (Eftil R
tbl.) u dozi od 500mg uveče. Naredna dva meseca je bila bez napada.
Zbog procene neurologa da nije definitivno utvrđen mehanizam
nastanka gubitaka svesti i da samim tim postoji značajan rizik od
značajnih kardiovaskularnih događaja i iznenadne srčane smrti,
konsultovan je tim kardiologa i neurologa, dogovoreno je dalje
kardiološko praćenje i ukidanje antiepileptika, što je i učinjeno u
avgustu 2012. godine.
Tokom oktobra 2012. godine javila se serija gubitaka svesti istih
osobina, te je hospitalizovana na neurološkom odeljenju bolnice u
Valjevu. Posle više konsultacija kardiologa, upućena je na
kardiologiju KC Srbije, gde joj je urađena implantacija ILR
Medtronic Raveal prepektoralno potkožno (aparat koji samo registruje
EKG aktivnost bez mogućnosti defibrilacije), uz amiodaron, jednu
tabletu dnevno, 5 dana, vikendom pauza. Otpusna dijagnoza je bila:
Sincopa recidivans. Tachycardia paroxismalis non specificata.
Od oktobra 2012. do aprila 2013. godine nije imala krize svesti.
Početkom aprila 2013. godine izgubila je svest, imala grčeve,
umokrila se. Primljena je na kardiologiju bolnice u Valjevu, gde je
elektronska kontrola ILR-a pokazala kratkotrajnu epizodu polimorfne
ventrikularne tahikardije, maksimalne frekvence 330/min.
Slika 1 – Epizoda polimorfne ventrikularne
tahikardije sa ILR naše bolesnice.
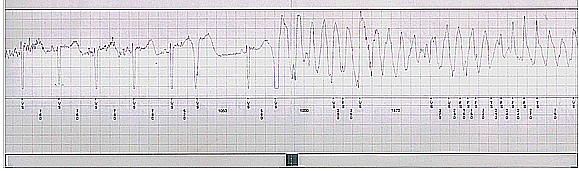
Slika 2 – Epizoda polimorfne ventrikularne
tahikardije sa ILR naše bolesnice.

Prevedena je u Pejsmejker centar KC Srbije gde je 3. 04. 2013.
godine operisana, urađena je ekstrakcija ILR-a i implantiran je
ICD-VR (Implantabile Cardioverter Defibrilator). Preporučena je i
terapija propranolol 2x20mg.
Od tada je bez kriza svesti i bez aktivacije defibrilatora.
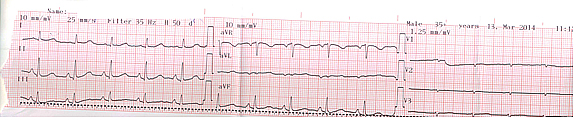
Poslednje kontrole neurologa i kardiologa su obavljene u martu 2014.
godine. Bolesnica je bez neurološke terapije.
Slika 3 – Normalan EKG zapis sa poslednje kontrole
naše bolesnice.
Za sada smatramo da se radi o konvulzivnim kardiološkim sinkopama
izazvanim ventrikularnom tahikardijom nepoznate etiologije. Za
prikaz ovog slučaja autori su imali pisanu saglasnost bolesnice.
DISKUSIJA
Tokom hospitalizacije u Instututu za majku i dete 2007. godine
iskazana je sumnja, tj. postavljena je radna dijagnoza aritmogene
displazije desne komore (ADDK), a paroksizam vetrikularne
tahikardije tokom boravka u bolnici je tretiran ampuliranim
amiodaronom, koji je uz inderal preporučen i za ambulantni tretman.
Kasnije je inderal zamenjen sotalolom.
Najveća studija sprovedena na 81 bolesniku ukazuje da je sotalol
najefikasniji lek u lečenju ADDK sa uspešnošću od 68%, za razliku od
amiodarona, gde je uspešnost bila 26% [29]. Zaključeno je da je,
ukoliko je terapija sotalolom neuspešna, neophodno razmišljati o
invazivnijem načinu lečenja.
Radiofrekventna kateter ablacija efikasna je za neke pacijente sa
ventrikularnom tahikardijom [30]. Iako takav način lečenja može biti
efektivan u kratkom periodu, sama procedura je povezana sa visokom
stopom ponovnog javljanja (kod 40% slučajeva se ponovi za 3 godine),
što govori da je ovaj način zbrinjavanja ADDK palijativne prirode
[31].
Implantabilni kardioverter defibrilator (ICD) konvertuje
ventrikularni flater/fibrilaciju u sinusni ritam i ugrađuje se kod
selektovanih bolesnika koji su u povišenom riziku od iznenadne
srčane smrti. MR srca se smatra zlatnim standardom za neinvazivno
postavljanje dijagnoze ADDK i kod naše bolesnice je rađen dva puta;
oba puta nalaz je opisan kao uredan. Najverovatnije se smatralo da
je tim nalazima isključeno strukturno oboljenje srca, te se odustalo
od nagoveštene biopsije srca.
Biopsija miokarda, tj. endomiokardna biopsija se po pravilu uzima iz
interventrikularnog septuma desne komore. Biopsija slobodnog zida
desne komore se smatra rizičnom jer može prouzrokovati potencijalnu
perforaciju i tamponadu, naročito kada je u pitanju istanjeno,
fibrozno tkivo [32].
Optimalan način lečenja ADDK je kontroverzan. Postoji više opcija
koje obuhvataju antiaritmike, radiofrekventnu ablaciju,
implantabilni kardioverter defibrilator, hirurške metode i
transplantaciju srca. Naša bolesnica je najpre lečena
antiaritmicima, potom kardioverter defibrilatorom.
ZAKLJUČAK
Predstavljen je slučaj 22-godišnje bolesnice sa ponavljanim
kardijalnim konvulzivnim sinkopama, kod koje, uprkos ekstenzivnom
ispitivanju uzrok konvulzivnih epizoda, nije razjašnjen do ugradnje
implantabilnog loop recorder-a (ILR), koji je pokazao da su gubici
svesti izazvani izraženom vetrikularnom tahikardijom (preko
300/min). Lečenje je sprovedeno ugradnjom kardiodefibrilatora.
Prikaz slučaja naše bolesnice ukazuje na teškoće koje se ponekad
javljaju u diferencijalnoj dijagnozi između sinkope i epilepsije. U
slučaju naše bolesnice, ključna dijagnostička metoda koja je
definitivno razjasnila slučaj je bio ILR. Dijagnozom polimorfne
ventrikularne tahikardije sa frekvencom 330/min, rešen je
dijagnostički problem posle oko 7 godina, a bolesnica je uspešno
lečena kardioverter defibrilatorom.
Ovaj slučaj ukazuje na značaj korišćenja ILR-a kod pacijenata sa
refrakternim konvulzivnim epizodama nedovoljno jasne etiologije, gde
je poremećaj srčanog ritma mogući uzrok. Blagovremena dijagnoza
nejasnih sinkopalnih stanja je od izuzetne važnosti zbog velikog
rizika od naprasne smrti ove grupe bolesnika.
Naglašavamo veliki značaj timskog rada u obradi i lečenju ove grupe
bolesnika, imajući u vidu kompleksnost i multidisciplinarnost ove
problematike.
LITERATURA
- Thijs RD, Beneditt DG, Mathias CJ, Schondorf R, Sutton R,
Wieling W, van Dijk JG. Definitions of syncope and related
disorders. Clin Auton Res 2005; 15: 35-39.
- Hoefnagels WA, Padberg GW, Overweg J, van der Velde EA, Roos
RA. Transient loss of consciousness: the value of the history
for distinguishing seizure from syncope. J Neurol 1991; 238:
39-43.
- Kenny RA. Syncope in the elderly: diagnosis, evaluation, and
treatment. J Cardiovasc Electrophysiol 2003; 14: S74-S77.
- Brignole M, Alboni P, Benditt DG, Bergfeldt L, Blanc JJ,
Bloch Thomsen PE, van Dijk JG, Fitzpatrick A, Hohnloser S,
Janovsek J, Kappor W, Kenny RA, Kulakowski P, Masotti G, Moya A,
Raviele A, Sutton R, Theodorakis G, Ungar A, Wieling W; Task
Force on Syncope, Europiean Society of Cardiology. Guidelines on
menagement (diagnosis and treatment) of syncope – update 2004.
Europace 2004; 6: 467-537.
- Hilz MJ, Marthol H, Neundorfer B. Syncope – a sistematic
overview of classification, pathogenesis, diagnosis and
management. Fortschr Neurol Psychiatr 2002; 70: 95-107.
- Grubb BP. Pathophysiology and differential diagnosis of
neurocardiogenic syncope. Am J Cardiol 1999; 84: 3Q-9Q.
- Koller ML, Meesmann M. Neurocardiogenic convulsive syncope –
differential diagnosis, pathophysiology and therapy based on a
case report. Z Kardiol 2000; 89: 1032-1038.
- van Dijk JG, Thijs RD, Benditt DG, Wieling W. A guide to
disorders causing transient loss of consciousness: focus on
syncope. Nat Rev Neurol 2009; 5: 438-448.
- Pezawas T, Stix G, Kastner J, Woltz M, Mayer C, Moertl D,
Schmidinger H. Unexplained syncope in patients with structural
heart disease and of electrophysiologically guided implantable
cardioverter defibrilator therapy. Europace 2003; 5: 305-312.
- Del Rosso A, Alboni P, Brignole M, Menozz C, Raviole A.
Relation of clinical presentation of syncope to the age of
patients. Am J Cardiol 2005; 96: 1431-1435.
- Soteriades ES, Evans JC, Larson MG, Chen MH, Chen L,
Benjamin EJ, Levy D. Incidence and prognosis of syncope. N Engl
J Med 2002; 347: 878-885.
- Savage DD, Corwin L, Mc Gree DL, Kannel WB, Wolf PA.
Epidemiologic features of isolated syncope: the Framingham
study. Stroke 1985; 16: 626-629.
- Ganzeboom KS, Mairuhu G, Reitsma J, Linzer M, Wieling W, van
Dijk N. Lifetime cumulative incidence of syncope in the general
population: a study of 549 Dutch subjects aged 35-60 years. J
Cardiovasc Electrophysiol 2006; 17: 1172-1176.
- Martin TP, Hanusa BH, Kapoor WN. Risk stratification of
patients with syncope. Ann Emerg Med 1997; 29: 459-466.
- Crane SD. Risk stratification of patients with syncope in an
accident and emergency department. Emerg Med J 2002; 19: 23-27.
- Sarasin FP, Louis-Simonet M, Carballo D, Slama S, Rajeswaran
A, Metzger JT, Louis C, Unger PF, Junod AF. Prospective
evaluation of patients with syncope: a population-based study.
Am J Med 2001; 111: 177-184.
- Jhanjee R, van Dijk JG, Sakaguchi S, Benditt DG. Syncope in
adults: terminology, classification, and diagnostic strategy.
Pacing Clin Electrophysiol 2006; 29: 1160-1190.
- Wieling W, Ganzeboom KS, Krediet CT, Grundmeijer HG, Wilde
AA, van Dijk JG. Initial diagnostic strategy in the case of
transient losses of consciousness: the importance of the medical
history. Ned Tijdschr Geneeskd 2003; 147: 849-854.
- Kranh AD, Klein GL, Tee R, Skanes AC. Detection of
asymptomatic arrhythmias in unexplained syncope. Am Heart J
2004; 148: 326-332.
- Boersma L, Mont L, Sionis A, Garcia E, Brugada J. Value of
implantable loop recorder for the menagement of patients with
unexplained syncope. Europace 2004; 6: 70-76.
- Lombardi F, Calosso E, Mascioli G, Marangoni E, Donato A,
Rossi S, Pala M, Foti F, Lunati M. Utility of implantable4 loop
recorder ( Raveal Plus ) in the diagnosis of unexpained syncope.
Europace 2005; 7: 19-24.
- Nesan Shanmugam, Reginald Liew. The Implantable Loop
Recorder- An Important Additional to the Armentarium in the
Menagement of Unexplained Syncope. Ann Acad Med Singapore 2012;
41: 115-124.
- Sheldon R, Rose S, Ritchie D, Connolly SJ, Koshman ML, Lee
MA, Frenneaux M, Fisher M, Murphy W. Historical criteria that
distinguish syncope from seizures. J Am Coll Cardiol 2002; 40:
142-148.
- Alboni P, Brignole M, Menozzi C, Raviele A, Del Rosso A,
Dinelli M, Solano A, Bottoni N. Diagnostic value of history in
patients with syncope with or without heart disease. J Am Coll
Cardiol 2001; 37: 1921-1928.
- Abubakr A, Wambacq I. The diagnostic value of EEGs in
patients with syncope. Epilepsy Behav 2005; 6: 433-434.
- Benbadis SR, Chichkova R. Psychogenic pseudosyncope: an
underestimated and provable diagnosis. Epilepsy Behav 2006; 9:
106-110.
- Steinberg JS, Beckman K, Greene HL, Marinchak R, Klin RC,
Greer SG, Ehlert F, Foster P, Menchavez E, Raitt M, Wathsen MS,
Morris M, Hallstrom A. Follow-up of patients with unexplained
syncope and inducible ventricular tachyarrhythmias: analysis of
the AVID registry and AVID substudy. Antiarrhythmics versus
Implantable Defibrillators . J Cardiovasc Electrophysiol 2001;
12: 996-1001.
- Petkar S, Cooper P, Fitzpatrick AP. How to avoid a
misdiagnosis in patients presenting with transient loss of
conciousness. Postgrad Med J 2006; 82: 630-641.
- Bomma C, Dalal D, Tandri H, et al. Evolving role of
multidetector computed tomography in evaluation of
arrhythmogenic right ventricular dysplasia/cardiomyopathy. Am J
Cardiol. 2007; 100: 99-105.
- Wichter T, Borggrefe M, Haverkamp W, Chen X, Breithardt G.
Efficacy of antiarrhytmic drugs in patients with inducible and
noninducible ventricular tachycardia. Circulation. 1992; 86:
29-37.
- Polin GM, Haqqani H, Tzou W, Hutchinson MD, Garcia FC,
Callans Đ, et al. Endocardial unipolar voltage mapping to
identify epicardial substrate in arrhythmogenic right
ventricular cardiomyopathy/dysplasia. Heart Rhythm. 2011; 8(1):
76-83.
- Paul M, Stypmann J, Gerss J, Wirdeier S, Zumhagen S,
Breithardt G, et al. Safety of endomyocardial biopsy in patients
with arrhythmogenic right ventrucular cardiomyopathy: a study
analyzing 161 diagnostic procedures. JACC Cardiovasc Interv.
2011; 4(10): 1142-1148.
|
|
|
|



