| |
|
|
UVOD
Grejvs-Bazedovljeva bolest (GB) definiše se kao hipertireoidizam
sa difuznom strumom nastalom zbog imunskih poremećaja. Incidenca ove
bolesti u opštoj populaciji može biti i do 1%, a četiri do pet puta
je češća u žena, što važi i za većinu autoimunih bolesti [1, 2].
Napori da se identifikuju činioci koji bi mogli da ukažu na
verovatnoću postizanja remisije, odnosno pojave recidiva po prekidu
medikamentne tirosupresivne terapije (MTT) neprekidno traju.
Izveštaji o postignutoj dugotrajnoj remisiji kreću se od 14 do 80%
lečenih, a ukupna stopa recidiva po prekidu lečenja je 30-50% [1,
3-13].
Utvrđivanje ranih prognostičkih faktora za ishod medikamentne
tirosupresivne terapije moglo bi da omogući razlikovanje pacijenata
koji reaguju i koji ne reaguju na terapiju, i pravovremeni izbor
ablativne terapije. Ultrazvuk omogućava objektivnu procenu dimenzija
tireoidne žlezde i može se ponavljati bez štetnih efekata po
pacijenta.
U brojnim istraživanjima prethodnih decenija, primećeno je da
prisustvo velike strume, na početku MTT može predstavljati loš
prognostički znak za ishod terapije. S druge strane, smanjenje
strume tokom lečenja predstavlja povoljan prognostički znak za ishod
MTT [4, 14].
Cilj ovog rada je bio da utvrdi uticaj veličine strume na
predviđanje nastanka remisije tokom medikamentne tirosupresivne
terapije.
MATERIJAL I METODE
Istraživanje je sprovedeno u vidu prospektivne studije uključivši
106 uzastopnih pacijenata sa novootkrivenom GB, kojima je započeta
medikamentna tirosupresivna terapija u ambulanti za bolesti štitaste
žlezde Službe za nuklearnu medicinu Zdravstvenog centra Zaječar.
Nakon postavljanja dijagnoze hipertireoidizma pacijentima upućenim
ambulanti za bolesti štitaste žlezde, a na osnovu anamnestičnih
podataka, kliničkog pregleda, utvrđivanja znakova hipermetabolizma,
te utvrđivanjem suprimiranog nivoa TSH i povišenih nivoa slobodnih
frakcija tireoidnih hormona u serumu, svim pacijentima urađena je
ehosonografska volumetrija i, u nejasnim slučajevima, rađena je
scintigrafija štitne žlezde tehnecijum pertehnetatom u cilju potvrde
autoimunog hipertireoidizma.
Postavljanje dijagnoze i sprovođenje terapije oslanjalo se na važeći
Vodič o dijagnozi i lečenju bolesti štitaste žlezde [15].
Svim ispitanicima uzeta je detaljna lična i porodična anamneza i
započeto je lečenje medikamentnom tirosupresivnom terapijom.
Klinički pregled je obuhvatao inspekciju i palpaciju tireoidne
žlezde, merenje pulsa, utvrđivanje prisustva ili odsustva tremora,
procenu kvaliteta kože, merenje telesne mase, kao i inspekciju očnih
jabučica i očnih kapaka u cilju utvrđivanja prisustva tireoidne
oftalmopatije.
Palpatorni nalaz na tireoidei gradiran je sa: 0 – bez strume; 0A –
palpabilna tireoidea; 0B – palpabilna i vidljiva pri ekstenziji
vrata; I – lako difuzno uvećana i vidljiva pri normalnom položaju
vrata; II – umereno difuzno uvećana; III – izrazito difuzno uvećana.
Nivo slobodnih frakcija tireoidnih hormona određivao se metodom LIA
(LIA FT4 Brahms Diagnostica GMBH), DELFIA (DELFIA FT3 Wallac Oy,
Turku, Finland) i ACCESS imunoesej sistemom. Opseg normalnih
vrednosti slobodnih frakcija tireoidnih hormona su 9,25-22 pmol/L za
FT4, i 3,8-6,0 pmol/L za FT3. TSH meren ultrasenzitivnom ILMA
metodom (ILMA ultrasensitive TSH Brahms Diagnostica GMBH), sa
referentnim opsegom 0,3-4 mU/L i ACCESS imunoesej sistemom, sa
referentnim opsegom 0,3-4,0 mIU/L.
Ehosonografija štitaste žlezde rađena je na Toshiba Justvision 200
ultrazvučnom aparatu sa linearnom sondom 8 MHz. Volumen se
izračunavao metodom Brunn i saradnika, kao zbir volumena
pojedinačnih režnjeva, a volumen pojedinačnog režnja izračunavao se
po formuli: širina režnja (cm) x debljina režnja (cm) x visina
režnja (cm) x 0,479 [16].
Scintigrafija štitaste žlezde rađena je nakon 15-20 minuta po
intravenskoj primeni oko 2 mCi (74 MBq) tehnecijum-pertehnetata
(99mTcO4), na gama kameri Simens Diacam. Svi in vivo i in vitro
testovi rađeni se u Službi za nuklearnu medicinu Zdravstvenog centra
Zaječar.
Kontrolni pregledi, koji su obuhvatali klinički pregled i
određivanje nivoa TSH, FT4 i FT3, vršeni su u periodu jednog do tri
meseca tokom medikamentne tirosupresivne terapije, pri čemu je
titrirana doza leka. Ehosonografska volumetrija rađena je na početku
tirosupresivne terapije i nakon 12 meseci terapije.
Nakon perioda praćenja od 12 meseci, pacijenti su podeljeni u dve
grupe, prema odgovoru na medikamentnu tirosupresivnu terapiju: grupa
A – pacijenti koji su postigli remisiju i grupa B – pacijenti koji
nisu postigli remisiju. Remisijom se smatralo odsustvo simptoma i
znakova bolesti, klinički i biohemijski eutireoidno stanje, sa
normalnim, ili povišenim nivoom TSH i normalnim, ili sniženim nivoom
tireoidnih hormona na terapiji dozom održavanja (za metimazol 5mg
dnevno, za propiltiouracil 50mg dnevno), 12 meseci po započinjanju
medikamentne tirosupresivne terapije, i odsustvo recidiva tokom
narednih 12 meseci praćenja.
Podaci su uneti u bazu podataka formiranu u Micrisoft Excel 2010.
Starost pacijenata, veličina strume, dužina medikamentnog
tirosupresivnog lečenja i volumen tireoidee izraženi su kao srednja
vrednost, SD, medijana, te minimalna i maksimalna vrednost. Za
testiranje razlika korišćeni su parametarski (Studentov t-test,
ANOVA) i neparametarski testovi (χ2 test, Friedmanov test, Mann –
Whitney U test, Cochrane,s Q test). Podaci su prikazani tabelarno i
grafički.
REZULTATI
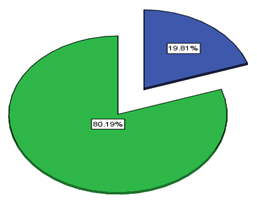
Od ukupno 106 ispitanika, 21 je bilo muškog pola (19,81%) i 85
ženskog pola (80,19%).
Prosečna starost svih ispitanika bila je 44,27±15,35 godina (opseg
14-74). Ukupno praćenje pacijenata bilo je 45 meseci. Prosečno
trajanje MTT iznosilo je 21,20±14,01 (medijana 17 meseci), a
prosečno praćenje nakon ukidanja terapije bilo je 28,38±27,21
(medijana 24 meseca), što je prikazano u tabeli 1, dijagramu 1.
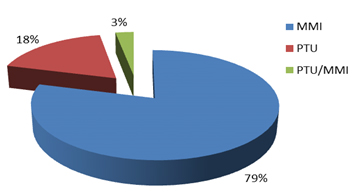
Kod svih naših ispitanika je po postavljanju dijagnoze započeta MTT
titracijskim režimom. Većina pacijenata lečena je metimazolom (79%),
dok je propiltiouracilom lečeno (18%). Kod preostalih, oko (3%)
ispitanika, terapija je započeta metimazolom, a potom nastavljena
propil-tiouracilom, uglavnom zbog alergijskih manifestacija na
metiamozol (dijagram 2).
Tabela 1. Struktura ispitanika.
| |
N |
Starost (g) |
Ukupno
praćenje (m) |
Trajanje
Th (m) |
Praćenje nakon Th |
Vreme 2 (m) |
Vreme 3 (m) |
| Ispitanici |
106 |
44,27±15,35
Opseg 14-74
Medijana 46 |
49,57±27,53
Medijana 45 |
21,20±14,01
Medijana 17 |
28,38±27,21
Medijana 24 |
5,55±1,98
Medijana 6 |
12,86±3,15
Medijana 12 |
| muškarci |
21 |
50,47±15,23 |
|
|
|
|
|
| žene |
85 |
42,74±15,08 |
|
|
|
|
|
N – broj; g – godine; m – meseci; Th – terapija; Vreme 2 – vreme
do prve kontrole; Vreme 3 – vreme do druge kontrole.
Dijagram 1. Struktura ispitanika prema polu.
Dijagram 2. Struktura ispitanika prema vrsti primenjene medikamentne
tirosupresivne terapije.
MMI – metimazol; PTU – propiltiouracil.
Oko 85% ispitanika na početku bolesti imali su u nekom stepenu
uvećanu tireoidnu žlezdu, a struktura ispitanika prema prisustvu
strume se tokom praćenja, 6 i 12 meseci po započinjanju MTT bitno ne
menja, što je prikazano u dijagramu 3. Najveći broj ispitanika na
početku bolesti (73,6%) ima malu difuznu strumu, dok samo 2,8%
pacijenata ima znatno uvećanu tireoidnu žlezdu. Struktura ispitanika
prema prisustvu i veličini strume se tokom praćenja, 6 i 12 meseci
po započinjanju MTT, ne menja bitno, što je prikazano u tabeli 2.
Prosečan volumen tireoidee kod naših ispitanika na početku bolesti
je 21ml i kretao se u opsegu od 11,2 do 47,6ml. Prosečan volumen
tireoidee 12 meseci po uvođenju MTT je 20ml, opsega 11,3-47,2ml, što
je prikazano u tabeli 3 i dijagramu 4.
Dijagram 3. Struktura ispitanika prema prisustvu
strume.
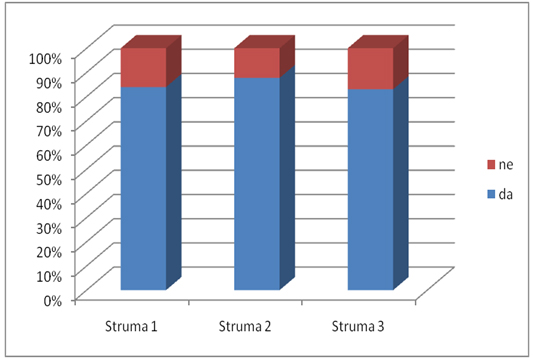
Struma 1 – na početku bolesti; struma 2 – 6 meseci po uvođenju
terapije; struma 3 – 12 meseci po uvođenju terapije.
Tabela 2. Struktura ispitanika prema prisustvu i veličini strume.
|
Struma |
Bez |
0A |
0B |
I |
II |
III |
Ukupno |
| Struma 1 |
N |
17 |
4 |
31 |
43 |
8 |
3 |
106 |
| % |
16,0% |
3,8% |
29,2% |
40,6% |
7,5% |
2,8% |
100% |
| Struma 2 |
N |
13 |
13 |
28 |
40 |
9 |
3 |
106 |
| % |
12,3% |
12,3% |
26,4% |
37,7% |
8,5% |
2,8% |
100% |
| Struma 3 |
N |
18 |
7 |
31 |
39 |
8 |
3 |
106 |
| % |
17,0% |
6,6% |
29,2% |
36,8% |
7,5% |
2,8% |
100% |
Struma 1 – na početku bolesti; struma 2 – 6 meseci po uvođenju
terapije; struma 3 – 12 meseci po uvođenju terapije.
Tabela 3. Prosečan volumen tireoidee izražen u mililitrima kod
ispitanika.
| Volumen (ml) |
Aritmetička sredina |
SD |
Medijana |
Minimum |
Maksimum |
| Volumen 1 |
21,848 |
7,4655 |
21,000 |
11,2 |
47,6 |
| Volumen 3 |
21,663 |
7,2858 |
20,000 |
11,3 |
47,2 |
Volumen 1 – na početku bolesti; volumen 3 – 12 meseci po uvođenju
terapije; SD – standardna devijacija.
Dijagram 4. Prosečan volumen tireoidee izražen u
mililitrima kod ispitanika.
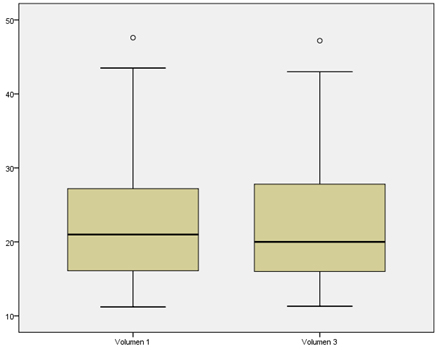
Volumen 1 – na početku bolesti; volumen 3 – 12 meseci po uvođenju
terapije;
y osa na dijagramu – mililitri.
Učestalost prisustva strume na početku bolesti i šest i dvanaest
meseci nakon započinjanja MTT kod pacijenata u remisiji i onih koji
nisu postigli remisiju je slična, a razlike su statistički
nesignifikantne, što je prikazano u tabeli 4. Kada se grupe uporede
prema veličini strume, kako na početku bolesti, tako i šest i
dvanaest meseci po započinjanju MTT, ne nalazi se statistički
značajna razlika u učestalosti, što je prikazano u tabeli 5. Kada se
volumetrijski prikaže zapremina žlezde, prosečna zapremina kod
pacijenata u remisiji i onih koji ne ulaze u remisiju, kako na
početku bolesti, tako i dvanaest meseci po započinjanju MTT, se ne
razlikuje značajno, što je prikazano u tabeli 6 i dijagramu 4.
Najveći broj pacijenata i u jednoj i u drugoj grupi ima malu difuznu
strumu, dok su pacijenti sa velikom strumom retki.
Tabela 4. Uticaj prisustva strume na ishod terapije.
| Struma |
Ishod |
| Remisija |
Bez remisije |
| N |
% |
N |
% |
| Struma 1 |
ne |
8 |
47,1% |
9 |
52,9% |
| da |
54 |
60,7% |
35 |
39,3% |
| Struma 2 |
ne |
6 |
46,2% |
7 |
53,8% |
| da |
56 |
60,2% |
37 |
39,8% |
| Struma 3 |
ne |
10 |
55,6% |
8 |
44,4% |
| da |
52 |
59,1% |
36 |
40,9% |
Struma 1 – na početku bolesti; struma 2 – 6 meseci po
započinjanju terapije; struma 3 – 12 meseci po započinjanju
terapije.
Nema statistički značajne razlike između pacijenata u remisiji i
onih koji nisu postigli remisiju prema prisustvu strume na početku
bolesti, (χ2=1,090; p=0,297), šest meseci po započinjanju terapije,
(χ2=0,929; p=0,335) i dvanaest meseci po započinjanju terapije
(χ2=0,077; p=0,782).
Analizirajući ove podatke po grupama, prema ishodu terapije
Cochrane’s Q testom, utvrđeno je da nema statistički značajne
razlike u prisustvu strume u grupi pacijenata sa remisijom (Q=4,000;
p=0,135), kao ni kod pacijenata koji nisu postigli remisiju
(Q=2,000; p=0,368).
Tabela 5. Uticaj prisustva i veličine strume na ishod terapije.
| Struma |
Ishod |
| Remisija |
Bez remisije |
| N |
% |
N |
% |
| Struma 1 |
bez |
8 |
12,9% |
9 |
20,5% |
| 0A |
1 |
1,6% |
3 |
6,8% |
| 0B |
18 |
29,0% |
13 |
29,5% |
| I |
31 |
50,0% |
12 |
27,3% |
| II |
3 |
4,8% |
5 |
11,4% |
| III |
1 |
1,6% |
2 |
4,5% |
| Struma 2 |
bez |
6 |
9,7% |
7 |
15,9% |
| 0A |
8 |
12,9% |
5 |
11,4% |
| 0B |
16 |
25,8% |
12 |
27,3% |
| I |
27 |
43,5% |
13 |
29,5% |
| II |
4 |
6,5% |
5 |
11,4% |
| III |
1 |
1,6% |
2 |
4,5% |
| Struma 3 |
bez |
10 |
16,1% |
8 |
18,2% |
| 0A |
3 |
4,8% |
4 |
9,1% |
| 0B |
19 |
30,6% |
12 |
27,3% |
| I |
26 |
41,9% |
13 |
29,5% |
| II |
2 |
3,2% |
6 |
13,6% |
| III |
2 |
3,2% |
1 |
2,3% |
Struma 1 – na početku bolesti; struma 2 – 6 meseci po
započinjanju terapije; struma 3 – 12 meseci po započinjanju
terapije.
Nema statistički značajne razlike između pacijenata u remisiji i
pacijenata koji nisu postigli remisiju prema prisustvu i veličini
strume na početku bolesti (Z=-0,931; p=0,352), šest meseci po
započinjanju terapije, (Z=-0,304; p=0,761) i dvanaest meseci po
započinjanju terapije (Z= -0,053; p=0,957).
Na osnovu Friedmanovog testa utvrđeno je da nema statistički
značajne razlike između ispitanika bez obzira na ishod, prema
prisustvu i veličini strume u sva tri merenja (χ2=1,089; p=0,580).
Na osnovu Friedmanovog testa utvrđeno je da nema statistički
značajne razlike između ova tri merenja kod pacijenata u remisiji
(χ2=3,265; p=0,195) u odnosu na pacijente koji nisu postigli
remisiju (χ2=0,255; p=0,880).
Tabela 6. Uticaj volumena tireoidee na ishod terapije.
| Ishod |
Aritmetička sredina |
SD |
Medijana |
Minimum |
Maksimum |
| Remisija |
Volumen 1 (ml) |
21,932 |
6,7553 |
21,800 |
11,2 |
42,9 |
| Volumen 3 (ml) |
21,577 |
6,8695 |
20,000 |
11,3 |
43,0 |
| Bez remisije |
Volumen 1 (ml) |
21,730 |
8,4459 |
19,350 |
12,0 |
47,6 |
| Volumen 3 (ml) |
21,784 |
7,9152 |
19,800 |
12,5 |
47,2 |
| Ukupno |
Volumen 1 (ml) |
21,848 |
7,4655 |
21,000 |
11,2 |
47,6 |
| Volumen 3 (ml) |
21,663 |
7,2858 |
20,000 |
11,3 |
47,2 |
Volumen 1 – na početku bolesti; volumen 3 – 12 meseci po
započinjanju terapije.
SD – standardna devijacija.
Statistička analiza podataka rađena je na transformisanim podacima
koji su dobijeni logaritmovanjem izvornih. Na osnovu rezultata
analize varijanse ponovljenih merenja, utvrđeno je da nema
statistički značajne razlike u prosečnom volumenu na početku bolesti
i dvanaest meseci po započinjanju terapije kod svih ispitanika
zajedno (F=0,202; p=0,654; Eta2part=0,002). Takođe, nema ni
statistički značajnog uticaja volumena na ishod (F=1,517; p=0,221;
Eta2part=0,014), odnosno promena volumena kod pacijenta u remisiji
ne razlikuje se od promena volumena kod pacijenata koji nisu
postigli remisiju. Ne postoji statistički značajna razlika u
volumenu tireoidee na početku bolesti (p=0,678) i volumenu tireoidee
dvanaest meseci po započinjanju terapije (p=0,992), između
pacijenata u remisiji i onih koji nisu postigli remisiju
(dijagram 5).
Dijagram 5. Uticaj volumena tireoidee na ishod
terapije.
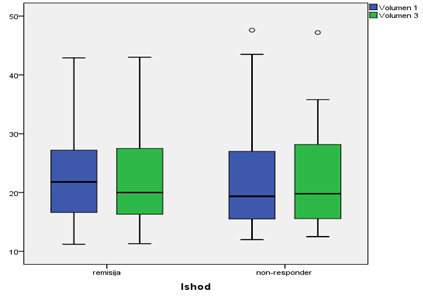
Volumen 1 – na početku bolesti; volumen 3 –12 meseci po započinjanju
terapije; y osa mililitri.
DISKUSIJA
U brojnim istraživanjima prethodnih decenija intenzivno se
tragalo za faktorima koji bi mogli predvideti ishod MTT. U tom
smislu ispitivan je pojedinačni ili udruženi uticaj pola, starosti,
veličine strume, oftalmopatije, nivoa tireoidnih hormona, TRAb i
drugih imunskih, biohemijskih i kliničkih parametara. Međutim, do
danas nisu utvrđeni pouzdani rani prognostički parametri koji bi
ukazivali na ishod MTT [3].
Primećeno je da prisustvo velike strume na početku MTT može
predstavljati loš prognostički znak za ishod terapije. S druge
strane, smanjenje strume tokom lečenja predstavlja povoljan
prognostički znak za ishod MTT [4, 14].
Tireoidna žlezda je jedan od prvih organa istraživanih ultrazvukom.
Prvi izveštaji ultrazvučnog pregleda štitaste žlezde potiču iz
kasnih 1960-tih. Između 1965. i 1970. bilo je sedam publikovanih
članaka posvećenih tireoidnom ultrazvuku. U poslednjih 5 godina,
samo na engleskom jeziku objavljeno je više od 1300 članaka sa ovom
temom. (Saopštenje prof. B. Trbojevića, Škola ultrazvuka, Zlatibor,
2014)
U dugogodišnjem praćenju više stotina pacijenata Soveid i saradnici
uočavaju da je stopa recidiva nakon ukidanja MTT kod pacijenata sa
GB, veća kod pacijenata koji imaju veću strumu, kako na početku
bolesti, tako i na ukidanju MTT [7]. U studiji japanskih autora iz
devedesetih godina, tragano je za vezom između tireoidnog volumena i
prognoze GB lečene medikamentnom tiro-supresivnom terapijom kod 60
pacijenata. Tirodni volumen kod zdravih osoba iznosio je 5,6-20,2ml,
prosečno 12,0±4,0ml. Kod pacijenata sa nelečenom GB, opseg
tireoidnog volumena bio je od 13,3-190,7ml, prosečno 40,2±27,8ml.
Tirodni volumen je značajno korelirao sa serumskom koncentracijom Tg
i TRAb. Tokom medikamentne tirosupresivne terapije, tireoidni
volumen se postepeno smanjivao kod većine pacijenata. Kod pacijenata
koji su ušli u remisiju po prekidu terapije, tireoidni volumen je
bio značajno manji nego pre lečenja. Kod pacijenata kod kojih je
tokom terapije došlo do jatrogenog hipotireoidizma (zbog prekomerne
doze leka), došlo je do povećanja volumena tireoidee. Nivo Tg je
uvek pratio tireoidni volumen. Nakon 12 meseci lečenja, tireoidni
volumen, izražen kao procenat volumena pre lečenja, bio je značajno
manji kod pacijenata u remisiji (77,6±8,9%), nego kod onih koji nisu
ušli u remisiju (92,4±11,6%). Podaci sugerišu da je serijsko
ultrazvučno merenje tireoidnog volumena koristan metod u predviđanju
toka hipertireoidizma kod medikamentno lečenih pacijenata [17].
Slično ovome, Yamaguchi i saradnici u istraživanju na 140 pacijenata
otkrivaju da tireoidni volumen značajno korelira sa nivoom Tg i
imunoglobulini MA koji blokiraju vezivanje TSH na TSH receptor
(TBII), ali ne i sa TSH, TPOAb i TgAb. Tokom terapije, smanjenje
tireoidnog volumena bilo je praćeno smanjenjem nivoa TBII. Autori,
na osnovu rezultata svog istraživanja, sugerišu da TSH receptorska
antitela mogu imati stimulišući efekat na rast tireoidee [18].
Retrospektivna studija brazilskih autora, koja je obuhvatala 80
pacijenata, a koji su praćeni najmanje 12 meseci po prekidu
medikamentne tirosupresivne terapije, sem što pokazuje veoma visok
procenat recidiva bolesti (čak 82,5%), ukazuje i na veličinu strume
kao jedini statistički signifikantan parametar za predviđanje
remisije. Autori visoku stopu recidiva tumače povećanim unosom joda
i lošom terapijskom komplijansom [8].
Brojne kontrolisane prospektivne studije sprovedene u različitim
delovima sveta, sa različitim unosom joda, potvrdile su da je jedna
od odlika na početku GB, udružena sa rizikom recidiva, struma veća
od 40ml. Međutim, prediktivna vrednost ovog pojedinačnog parametra
je veća ukoliko se gleda udruženi uticaj i drugih parametara na
početku bolesti [19].
U istraživanju Nadreba i saradnika, primećeno je da je recidiv GB
nakon prekida MTT unutar dve godineM češći kod ispitanika sa većom
strumom, te se zaključuje da veličina strume na kraju tirosupresivne
terapije može biti prediktor recidiva bolesti [11].
Bojarska i saradnici su takođe istraživali vrednost određivanja
veličine tireoidee kao markera u predviđanju ishoda medikamentne
tirosupresivne terapije kod 100 pacijenata. Veličina tireoidee bila
je značajno veća u grupi pacijenata koji nisu imali adekvatan
odgovor na medikamentnu terapiju [20].
Nasuprot ovome, u studiji na 216 uzastopnih ispitanika sa
novodijagnostikovanom GB, kod kojih je uključena MTT, Cappelli i
saradnici nisu našli da veličina strume na početku bolesti ima
prognostički značaj za predviđanje ishoda MTT [3]. Takođe, i Jonas
sa saradnicima ne nalazi vezu između volumena tireoidee i ishoda MTT
u svom istraživanju [10].
Četiri nedelje nakon prekida medikamentne tirosupresivne terapije
utvrđivan je tireoidni status kod 96 pacijenata. Stopa recidiva
procenjivana je tokom ukupnog postterapijskog praćenja od 2 godine.
Autori ovog istraživanja ne nalaze da volumen tireoidee ima uticaj
na stopu recidiva bolesti [9].
Kod većine naših ispitanika (oko 90%), na početku bolesti struma je
mala ili odsutna (gradus 0A, 0B, 0-I). Tokom MTT, struktura
ispitanika, prema prisustvu i veličini strume, bitno se ne menja.
Prosečan volumen tireoidee na početku bolesti kod naših ispitanika
je oko 21ml. Tokom MTT i dvanaest meseci po započinjanju MTT, nije
primećena bitna promena u veličini tireoidee. Nije primećeno da
postoji značajna razlika u prisustvu i veličini strume, bilo da je
određivana palpacijom, bilo da je merena ehosonografski, između
pacijenata u remisiji i onih koji nisu postigli remisiju.
Mada mnoga dosadašnja istraživanja nalaze da veličina strume može
biti prediktivni faktor za ishod MTT, ipak ima i onih koja ne nalaze
vezu između veličine strume i ishoda MTT. Jedno od tih je i naše
istraživanje. U našoj grupi od 106 uzastopnih ispitanika sa
novootkrivenom GB, samo tri pacijenta imaju volumen tireoidee preko
43ml i samo osam volumen 32-42ml.
Skoro svim do sada pomenutim studijama cilj je bio utvrditi
prediktivne faktore za ishod MTT kod GB, jer skoro polovina
pacijenata ne ulazi u stabilnu kliničku remisiju i ima recidiv
bolesti po prekidu MTT. U većini studija, kao najznačajniji
parametri za predviđanje ishoda MTT, ističu se veličina strume i
nivo TRAb na početku i na ukidanju terapije. Međutim, zaključak
većine autora je da svaki pojedinačni parametar tireoidnog statusa
na početku bolesti nije dovoljan prediktor ishoda, da se
kombinacijom parametara postiže bolja predikcija ishoda, ali i da
nema konsenzusa oko ranih prognostičkih parametara koji bi ukazivali
na verovatnoću dugoročne stabilne remisije GB nakon MTT [3, 21, 22].
ZAKLJUČAK
Većina naših ispitanika na početku bolesti ima malu strumu, a
prisustvo i veličina strume na početku bolesti i tokom medikamentne
tirosupresivne terapije nisu imali značaja za predviđanje remisije.
LITERATURA
- Trbojević B. Tireoidna žlezda. Čip štampa Beograd, 1998.
- Fountoulakis S. and Tsatsoulis A. On the pathogenesis of
autoimmune thyroid disease: a unifying hypothesis. Clinical.
Endocrinology. 2004; 60: 397-409.
- Cappelli C, Gandossi E, Castellano M, Pizzocaro C, A gosti
B, Delbarba A, Pirola I, Martino ED , Rosei EA. Prognostic value
of thyrotropin receptor antibodies (TRAb) in Graves’ disease: a
120 months prospective study. Endocr J 2007; 54: 713-720.
- Leslie J, DeGroot M. D. Graves' Disease and the
Manifestations of Thyrotoxicosis. In: Thyroid disease manager.
Last Revised 20 December 2012.
www.Thyroidmanager.org
- Glinoer D; de Nayer P; Bex M. Effects of l-thyroxine
administration, TSH-receptor antibodies and smoking on the risk
of recurrence in Graves' hyperthyroidism treated with
antithyroid drugs: a double-blind prospective randomized study.
Eur J Endocrinol 2001; 144 (5): 475-83.
- Paunković N, Paunković J, Pavlović O. Values of TSH receptor
autoantibodies in patients with treated Graves' disease. Radiol
Iugosl 1991; 25: 319-23.
- Soveid M, Shaabani A, Ghaedi GH. H, Jafari SM. and Omrani
GH. Prognostic factors in the relapse of Graves disease
following treatment with antithyroid drugs. Iran J. Med. Sci
2003: 28 (3): 106-110.
- Bolanos F, González-Ortiz M, Durón H, Sánchez C. Remission
of Graves' hyperthyroidism treated with methimazole. Rev Invest
Clin. 2002; 54(4): 307-10.
- Quadbeck B, Hoermann R, Roggenbuck U, Hahn S, Mann K,
Janssen OE; Basedow Study Group. Sensitive thyrotropin and
thyrotropin-receptor antibody determinations one month after
discontinuation of antithyroid drug treatment as predictors of
relapse in Graves' disease. Thyroid. 2005; 15 (9): 1047-54.
- Jonas M, Ambroziak U, Bednarczuk T, Nauman J. Predicting a
relapse of Graves' hyperthyroidism in adults during the early
phase of treatment with anti-thyroid drugs. Endokrynol Pol.
2006; 57 (6): 596-604.
- Nedrebo BG, Holm PI, Uhlving S, Sorheim JI, Skeie S, Eide
GE, Husebye ES, Lien EA, Aanderud S. Predictors of outcome and
comparison of different drug regimens for the prevention of
relapse in patients with Graves' disease. Eur J Endocrinol.
2002; 147 (5): 583-9.
- Kaguelidou F, Alberti C, Castanet M, Guitteny MA, Czernichow
P, Léger J; French Childhood Graves' Disease Study Group
Predictors of autoimmune hyperthyroidism relapse in children
after discontinuation of antithyroid drug treatment. J Clin
Endocrinol Metab. 2008; 93 (10): 3817-26.
- Okamoto Y, Tanigawa S, Ishikawa K, Hamada N. TSH receptor
antibody measurements and prediction of remission in Graves'
disease patients treated with minimum maintenance doses of
antithyroid drugs. Endocr J. 2006; 53 (4): 467-72.
- Balasz CS, Leovey A, Szabo M, Bako G: Stimulating effect of
triiodothyronine on cell mediated immunity. Eur J Clin Pharmacol
1980; 17: 19.
- Trbojević B, Žarković M, Artiko V, Beleslin B, Ćirić J,
Ćirić S. i ostali, za radnu grupu za izradu vodiča. Nacinalni
vodič dobre kliničke prakse za poremećaj rada štitaste žlezde.
Ministarstvo zdravlja Republike Srbije, Republička stručna
komisija za izradu vodiča dobre kliničke prakse. 2011.
- Brunn J, Block U, Ruf G, Kumze WP and Scriba PC. Volumetrie
der Schilddrusenlappen mittels Real-time-Sonographiae. Deutch
Medizinische Woschencshrift 1981; 106: 1338-1340
- Sakane S. The prognostic application of thyroid volume
determination in patients with Graves’ disease. Nihon Naibunpi
Gakkai Zasshi 1990; 66 (5): 543-56.
- Yamaguchi Y, Inukai T, Iwashita A, Nishino M, Sholda Y,
Shimomura Y, Ohshima K, Kobayashi S, Kobayashi I. Changes in
thyroid volume during antithyroid drug therapy for Graves’
disease and its relationship to TSH receptor antibodies, TSH and
Tg. Acta Endocrinol 1990; 123 (4): 411-5.
- Orgiazzi J, Madec AM. Reduction of the risk of relapse after
withdrawal of medical therapy for Graves' disease. Thyroid.
2002; 12 (10): 849-53.
- Bojarska-Szmygin A, Janicki K, Pietura R, Janicka L. The
usefulness of thyroid size and TSH receptor antibody (TRAb)
determinations in predicting the effectiveness of tiamazole and
I-131 treatment for Graves-Basedow's disease. Ann Univ Mariae
Curie Sklodowska Med. 2003; 58 (1): 242-7.
- Kamath C, Adlan MA, and Premawardhana L.D. The role of
thyrothrophinreceptor antibody assays in Graves disease. Jour
Thyroid Res. Vol 2012 (2012); 1-8.
- Alfadda A, Malabu U, El-Desouki M, Al-Rubeaan K, Fouda M,
Al-Maatoug M, Sulimani R. Tretman of Graves hyperthyroidism –
prognostic factors for outcome. Saudi Med J, 2007; Vol. 28 (2):
225-230.
|
|
|
|





